Читайте также:
- I. Теория моментов
- II. ОСНОВЫ МОЛЕКУЛЯРНОЙ ФИЗИКИ И ТЕРМОДИНАМИКИ
- Labeling — теория стигматизации
- V. Очистка жидкостей перегонкой
- V1:Теория
- Vi ТЕОРИЯ ЭКОНОМИЧЕСКОГО АНАЛИЗА
- А. МАСЛОУ И ТЕОРИЯ САМОАКТУАЛИЗАЦИИ
- Аналитическая теория личности
- АНГЛИЙСКИЙ ЛИБЕРАЛИЗМ. ТЕОРИЯ УТИЛИТАРИЗМА И.БЕНТАМА. ДЖ.МИЛЛЬ О СВОБОДЕ
- Атомно-молекулярное учение
- Атомно-молекулярное учение. Атом. Молекула. Химический элемент. Простое и сложное вещество. Относительная атомная и молекулярная масса. Моль
- Бихевиористская теория Дж. Уотсона
Вещество находится в жидком состоянии, если средняя кинетическая энергия теплового движения его молекул примерно равна средней потенциальной энергии их взаимодействия.
До настоящего времени законченной количественной теории жидкого состояния нет, на качественном же уровне МКТ может объяснять явления, происходящие с жидкостями.
1. Из-за того, что расстояние между молекулами жидкости малы, увеличиваются силы притяжения молекул друг к другу, поэтому жидкости в отличие от газов обладают собственным объёмом, практически несжимаемы, плотность жидкостей при обычных условиях в сотни и тысячи раз больше плотности газов.
2. Вблизи каждой молекулы другие молекулы располагаются в определённом порядке, в целом в жидкости именно такой порядок не сохраняется, поэтому говорят, что в расположении молекул жидкости имеется ближний порядок и отсутствует дальний порядок.
3. Молекулы жидкости совершают хаотическое движение вблизи некоторого положения равновесия (колебания), изредка переходя в новое состояние равновесия (совершают перескоки), которые происходят случайным образом. Если на жидкость действует сила, например, сила тяжести, то перескоки происходят в направлении силы. Этим объясняется текучесть жидкости.
4. На границе с газом жидкость образует свободную поверхность. Поверхностный слой жидкости – резкая граница, отделяющая жидкость от газа над ней, существует из-за большого различия плотностей жидкости и газа (например, .
Поверхностный слойпредставляет собой подобие упругой плёнки из самой жидкости (можно положить осторожно, не нарушая слоя, иголку или лезвие бритвы на поверхность воды). Благодаря существованию поверхностного слоя возможно образование капли, мыльного пузыря, движение насекомых (водомерки) по поверхности воды.
Основное свойство поверхностного слоя: он стремится сократиться и принять наименьшую площадь поверхности при данном объёме. Из всех тел при данном объёме наименьшая площадь поверхности у шара, вот почему капля жидкости, мыльный пузырь в невесомости имеют форму шара.
МКТ объясняет существование поверхностного слоя так: молекулы на поверхности жидкости находятся в особых условиях по сравнению с молекулами её внутренних слоёв. Внутри жидкости результирующая сила притяжения, действующая на молекулу со стороны соседних молекул, равна нулю. У «поверхностных» молекул соседних молекул «сверху» меньше, чем «снизу». Молекулы поверхностного слоя под действием результирующей силы, втягиваются внутрь жидкости. В результате они оказывают молекулярное давление на жидкость, стягивая её поверхность до минимума. Этот эффект называется поверхностным натяжением.
Поверхностное натяжение обуславливает наличие у молекул поверхностного слоя дополнительной потенциальной энергии – поверхностной энергии.
Дополнительнаяпотенциальная энергия равна той работе, которуюнужно было бы совершить, чтобы молекулам из глубиныподняться к поверхности, преодолевая силу молекулярного давления на поверхности жидкости.
— поверхностная энергия, ,
где — площадь поверхностного слоя, — коэффициент поверхностного натяжения.
Все тела стремятся к положению устойчивого равновесия, которое определяется минимумом потенциальной энергии. Условием устойчивого равновесия жидкости является минимум потенциальной поверхностной энергии. Уменьшение поверхностной энергии достигается сокращением площади поверхностности жидкости, этим объясняется основное свойство поверхностного слоя.
В поверхностном слое действует сила поверхностного натяжения– сила, которая действует вдоль поверхности жидкости, перпендикулярно линии, ограничивающей поверхность и стремящаяся сократить её до минимума.
Например, поверхность жидкости в стакане цилиндрической формы (вид сверху):
— сила поверхностногонатяжения
Опыт показывает, что сила поверхностного натяжения пропорциональна длине линии, ограничивающей поверхность жидкости – .
, где — коэффициент поверхностного натяжения или поверхностное натяжение
Поверхностное натяжение зависит:
1. от природы граничащих сред, для двух граничащих сред величина постоянная, поскольку чаще всего жидкости граничат с воздухом, то поверхностное натяжение зависит от рода жидкости;
2. с повышением температуры поверхностное натяжение уменьшается, т.к. уменьшается плотность жидкости;
3. можно изменить, поменяв химический состав поверхности, например, капнуть на поверхность другую жидкость.
Чем меньше поверхностное натяжение, тем легче жидкость проникает в ткань. Высокая проникающая способность мыльного раствора, позволяющая очищать ткани, объясняется его малым поверхностным натяжением.
Смачивание
Капля воды на стекле растекается, вода смачивает стекло, но не смачивает парафин, промасленную бумагу, воск.
Капля ртути на стекле не растекается и стремится стянуться в шар, ртуть не смачивает стекло, но смачивает медь и цинк.
В сосуде поверхность жидкости искривляется. Мениск —форма поверхности жидкости в сосуде.
У смачивающей жидкости мениск вогнутый:
У не смачивающей жидкости мениск выпуклый:
Смачивание объясняется тем, что молекулы жидкости друг к другу притягиваются слабее, чем к молекулам твёрдого тела.
Не смачивание объясняется тем, что молекулы жидкости друг к другу притягиваются сильнее, чем к молекулам твёрдого тела.
Смачивание –это явление, возникающее вследствие взаимодействия молекул жидкости с молекулами твёрдого тела и приводящее к искривлению поверхности жидкости.
Смачивание поверхности твёрдого тела жидкостью используют, например, при крашении, склеивании, пайке.
Не смачивание учитывают, например, при изготовлении тканей для зонтов, плащей, упаковочного материала для жидких продуктов.
Дата добавления: 2014-11-18 ; Просмотров: 1744 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Нас окружают разнообразные предметы. Мы можем увидеть, что это либо твердые тела, либо жидкости, либо газы. Возникает масса вопросов обо всем, что нас окружает. Ответы на многие вопросы дает молекулярно-кинетическая теория.
Молекулярно-кинетическая теория – это совокупность воззрений, используемых для описания наблюдаемых и измеряемых свойств вещества на основе изучения свойств атомов и молекул данного вещества, их взаимодействия и движения.
Основные положения молекулярно-кинетической теории
Все тела состоят из частиц – атомов, молекул, ионов.
Все частицы находятся в непрерывном хаотическом тепловом движении.
Между частицами любого тела существуют силы взаимодействия – притяжения и отталкивания.
Таким образом, в молекулярно-кинетической теории объектом исследования является система, состоящая из большого количества частиц – макросистема. Для объяснения поведения такой системы законы механики не применимы. Поэтому основным методом исследования является статистический метод изучения свойств вещества.
Для объяснения и предсказания явлений важно знать основные характеристики молекул:
Оценка размера молекулы может быть сделана как размер кубика a в котором содержится одна молекула, исходя из плотности твердых или жидких веществ и массы одной молекулы:
- Масса молекул
Отношение массы вещества m к числу молекул N в данном веществе:
- Относительная молекулярная масса
Отношение массы молекулы (или атома) данного вещества к 1/12 массы атома углерода:
- Количество вещества
Количество вещества равно отношению числа частиц N в теле (атомов – в атомарном веществе, молекул – в молекулярном) к числу молекул в одном моле веществаNА:
- Постоянная Авогадро
Количество молекул, содержащихся в 1 моль вещества.
- Молярная масса
Молярной массой вещества называют массу вещества, взятого в количестве 1 моля.
В Международной системе единиц молярная масса вещества выражается в кг/моль.
- Взаимодействие (количественно на основе опытов)
Для взаимодействия молекул характерно одновременно и притяжение, и отталкивание: на расстояниях r r – притяжение, причем оно быстро убывает. На расстоянии r система двух молекул обладает минимумом потенциальной энергии (сила взаимодействия равна нулю) – это состояние устойчивого равновесия
Молекулярно-кинетическая теория дает возможность понять, почему вещество может находиться в газообразном, жидком и твердом состояниях. С точки зрения МКТ агрегатные состояния различаются по значению среднего расстояния между молекулами и характеру движения молекул друг относительно друга.
Основные положения молекулярно-кинетической теории неоднократно подтверждались различными физическими экспериментами. Например, исследованием:
Б) Броуновского движения
Краткие итоги
Молекулярно-кинетическая теория объясняет строение и свойства тел на основе движения и взаимодействия атомов, молекул и ионов. В основе МКТ лежат три положения, которые полностью подтверждены экспериментально и теоретически:
1) все тела состоят из частиц – молекул, атомов, ионов;
2) частицы находятся в непрерывном хаотическом тепловом движении;
3) между частицами любого тела существуют силы взаимодействия – притяжения и отталкивания.
Молекулярное строение вещества подтверждается непосредственным наблюдением молекул в электронных микроскопах, а также растворением твердых веществ в жидкостях, сжимаемостью и проницаемостью вещества. Тепловое движение – броуновским движением и диффузией. Наличие межмолекулярного взаимодействия прочностью и упругостью твердых тел, поверхностным натяжением жидкостей.
Тепловое расширение с точки зрения молекулярно- кинетической теории
Для простоты ограничимся рассмотрением твердых тел, имеющих кристаллическое строение. Для остальных тел (аморфные и жидкости) молекулярная картина теплового расширения в общих чертах та же. Взаимодействие между частицами, расположенными в узлах кристаллической решетки (ионы, атомы или молекулы), имеет более сложный характер, чем взаимодействие между точечными зарядами. Если на больших расстояниях ионы (например, разноименные) притягиваются, то на достаточно малых расстояниях силы притяжения сменяются быстро растущими силами отталкивания, т.к. при большом сближении электронных оболочек начинают сказываться силы отталкивания между ними.
Зависимость потенциальной энергии взаимодействия U(r) двух соседних частиц от расстояния r между ними позволяет объяснить причину теплового расширения. Для этого достаточно знать лишь приближенный вид потенциальной кривой U(r), которая представлена на рис. 14. Кривая быстро
возрастает от минимального значения в точке r при уменьшении r и сравнительно медленно растет при увеличении r
Из курса механики известно, что сила взаимодействия между частицами F(r) может быть найдена по формуле:
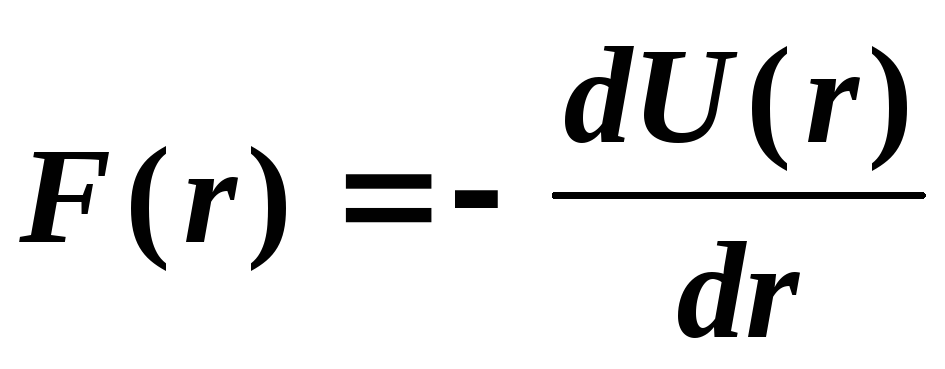
Если сила F(r) положительна, то частицы отталкиваются, если отрицательна, то они притягиваются. Из рис. 14 и формулы (5) нетрудно выяснить, что силы притяжения, действующие на участке r > r сменяются при r r. Изменяется именно среднее расстояние между частицами, а не положение равновесия, которое остается по прежнему в точке r. Увеличение среднего расстояния между частицами обусловливает и увеличение размеров всего тела.
Дальнейшее нагревание приводит к увеличению полной энергии до некоторого значения W2 , при этом колебания совершаются с большей амплитудой около нового среднего положения r2 > r1 и т.д. Грубо говоря, с ростом амплитуды колебаний частицы все сильнее «отталкиваются» друг от друга. Итак, мы видим, что при нагревании тела среднее расстояние между частицами увеличивается, поэтому увеличивается и размер тела.
Если знать форму потенциальной кривой, то можно вычислить коэффициент линейного расширения. Расчеты такого рода дают хорошее согласие с опытом.
Экспериментальная установка состоит из термостата ТС-24 и двух трубок из твердых тел. Через эти трубки протекает вода, нагреваемая термостатом. Скорость протекания воды по трубкам настолько велика, что температуру во всех точках трубок можно считать одинаковой и равной температуре воды в термостате, которая измеряется контрольным термометром. Удлинение трубок l измеряется индикатором, ножка которого упирается в пластину, припаянную к трубке, другой конец трубки фиксируется зажимным винтом. Рабочим участком трубки l считается расстояние от центра винта (зажимного) до той грани пластины, которая соприкасается с ножкой индикатора. Это расстояние измеряется линейкой.
Строение жидких, твёрдых и газообразных тел с точки зрения молекулярно-кинетической теории.
Твёрдые тела являются полной противоположностью газам. В них не происходит свободного передвижения частиц. Молекулы находятся в узлах кристаллической решётки. То есть существует строгий периодический порядок в расположении частиц, составляющих твёрдое тело.
3. Жидкости, в отличие от твёрдых тел, обладают ближним порядком в расположении частиц вещества.
Жидкие тела
В двух предыдущих параграфах мы рассмотрели строение и свойства твёрдых тел – кристаллических и аморфных. Перейдём теперь к изучению строения и свойств жидкостей.
Характерным признаком жидкости является текучесть – способность изменять форму за малое время под действием даже малых сил. Благодаря этому жидкости льются струями, текут ручьями, принимают форму сосуда, в который их нальют.
 |
Способность изменять форму у разных жидкостей выражена по-разному. Взгляните на рисунок. Под действием примерно равных сил тяжести мёду требуется больше времени, чтобы изменить свою форму, чем воде. Поэтому говорят, что эти вещества обладают неодинаковой вязкостью: у мёда она больше, чем у воды. Это объясняется неодинаково сложным строением молекул воды и мёда. Вода состоит из молекул, которые напоминают шарики с бугорками, а мёд состоит из молекул, похожих на ветви дерева. Поэтому при движении мёда «ветви» его молекул зацепляются друг за друга, придавая ему большую вязкость, чем воде.
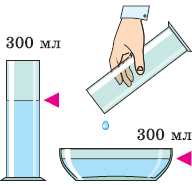 |
Важно: меняя форму, жидкость сохраняет свой объём. Рассмотрим опыт (см. рисунок). Жидкость в мензурке имеет форму цилиндра и объём 300 мл. После переливания в чашу жидкость приняла плоскую форму, но сохранила прежний объём: 300 мл. Это объясняется притяжением и отталкиванием её частиц: в среднем они продолжают удерживаться на прежних расстояниях друг от друга.
Ещё одним общим свойством всех жидкостей является их подчинение закону Паскаля. В 7 классе мы узнали, что он описывает свойство жидкостей и газов передавать оказываемое на них давление во все стороны (см. § 4-в). Теперь заметим, что менее вязкие жидкости делают это быстро, а вязкие – долго.
Строение жидкостей. В молекулярно-кинетической теории считается, что в жидкостях, как и в аморфных телах, нет строгого порядка в расположении частиц, то есть они расположены не одинаково плотно. Промежутки имеют различные размеры, в том числе и такие, что туда может поместиться ещё одна частица. Это позволяет им перескакивать из «густонаселённых» мест в более свободные. Перескоки каждой частицы жидкости происходят очень часто: несколько миллиардов раз в секунду.
Если на жидкость подействует какая-нибудь внешняя сила (например, сила тяжести), движение и перескоки частиц будут происходить в основном в направлении её действия (вниз). Это приведёт к тому, что жидкость примет форму вытягивающейся капли или льющейся струи (см. рисунок). Итак, текучесть жидкостей объясняется перескоками их частиц из одного устойчивого положения в другое.
Перескоки частиц жидкостей происходят часто, однако гораздо чаще их частицы, как и в твёрдых телах, совершают колебания на одном месте, непрерывно взаимодействуя друг с другом. Поэтому даже малое сжатие жидкости приводит к резкому «ожесточению» взаимодействия частиц, что означает резкое повышение давления жидкости на стенки сосуда, в котором её сжимают. Так объясняется передача жидкостями давления, то есть закон Паскаля, и, одновременно, свойство жидкостей противостоять сжатию, то есть сохранять объём.
Заметим, что сохранение жидкостью своего объёма – это условное представление. Имеется в виду, что по сравнению с газами, которые легко сжать даже силой руки ребёнка (например, в воздушном шарике), жидкости можно считать несжимаемыми. Однако на глубине 10 км в Мировом океане вода находится под столь большим давлением, что каждый килограмм воды уменьшает свой объём на 5% – от 1 л до 950 мл. Используя большие давления, жидкости можно сжать и ещё сильнее.
Свойства газа, жидких и твердых тел с точки зрения молекулярно-кинетической теории
Характеристика тепловых явлений в молекулярной физике. Рассмотрение основных положений молекулярно-кинетической теории. Основной порядок взаимодействия молекул. Изучение строения газообразных, жидких и твердых тел. Описание Броуновского движения.
| Рубрика | Физика и энергетика |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 16.01.2015 |
| Размер файла | 358,6 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
ГБОУ НПО АО «Профессиональное училище № 1»
РЕФЕРАТ НА ТЕМУ:
«Свойства газа, жидких и твердых тел с точки зрения молекулярно-кинетической теории»
Выполнил: Акишин Дмитрий Андреевич
Проверил: Жубрева Лидия Николаевна
1. Тепловые явления в молекулярной физике
2. Основные положения молекулярно-кинетической теории
3. Взаимодействие молекул
4. Строение газообразных, жидких и твердых тел
5. Броуновское движение
1. Тепловые явления в молекулярной физике
тепловой броуновский кинетический твердый
Тепловые явления привлекали внимание людей с древних времён. Умение добывать и поддерживать огонь сделало человека относительно независимым от колебаний температуры окружающей среды. Это было одним из величайших изобретений человечества. Изменение температуры оказывает влияние на все свойства тел. Кроме механических свойств, при изменении температуры меняются и другие свойства тел, например сопротивление электрическому току, магнитные свойства и др. Так, если сильно нагреть постоянный магнит, то он перестанет притягивать железные предметы. Все перечисленные выше и многие другие тепловые явления подчиняются определённым законам. Открытие законов тепловых явлений позволяет с максимальной пользой применять эти явления на практике и в технике. Молекулярно-кинетическая теория. Ещё философы древности догадывались о том, что теплота — это вид внутреннего движения. Но только в ХVIII в. Начала развиваться последовательная молекулярно — кинетическая теория. Цель молекулярно-кинетической теории — объяснение свойств макроскопических тел и тепловых процессов, протекающих в них, беспорядочно движущихся частиц. Большой вклад в развитие молекулярно-кинетической теории был сделан М.В. Ломоносовым. Он рассматривал теплоту как вращательное движение частиц, составляющих тела.
2. Основные положения молекулярно-кинетической теории
В основе молекулярно-кинетической теории строения вещества лежат три утверждения: вещество состоит из частиц; эти частицы беспорядочно движутся; частицы взаимодействуют друг с другом. Каждое утверждение строго доказано с помощью опытов. Свойства и поведение всех без исключения тел от инфузории до звезды определяются движением взаимодействующих друг с другом частиц: молекул, атомов или ещё более малых образований — элементарных частиц.
Оценка размеров молекул. Для полной уверенности в реальности молекул надо определить их размеры.
Проще всего это сделать, наблюдая расплывание капельки масла, например оливкового, по поверхности воды. Масло никогда не займёт всю поверхность, если сосуд велик. Нельзя заставить капельку объёмом 1 мм(в кубе) расплыться так, чтобы она заняла площадь поверхности более 0,6 м(в квадрате). Объём V слоя масла равен произведению его площади поверхности S на толщину d слоя, т.е V=Sd. Следовательно, размер молекулы оливкового масла равен: d = ? 1,7 Ч см.
При очень малых размерах молекул число их в любом макроскопическом теле огромно. Подсчитаем приблизительное число молекул в капле воды массой 1 г и, следовательно, объёмом 1.
Диаметр молекулы воды равен примерно 3 Ч . Считая, что каждая молекула воды при плотной упаковке молекул занимает объём капли (1 на объём, приходящийся на одну молекулу:
Размеры атома надо запомнить: D ?см ? м.
3. Взаимодействие молекул
Если молекулы существуют и движутся, то между ними обязательно должны действовать силы. Без этого взаимодействия не было бы ни твёрдых, ни жидких тел. Молекула- это сложная система, состоящая из отдельных заряженных частиц: электронов и атомных ядер. Хотя в целом молекулы электрически нейтральны, тем не менее между ними на малых расстояниях действуют значительные электрические силы: происходит взаимодействие электронов и атомных ядер соседних молекул.
Если молекулы находятся на расстояниях, превышающих их размеры в несколько раз, то силы взаимодействия практически не сказываются. Силы между электрически нейтральными молекулами являются короткодействующими.
На расстояниях, превышающих 2-3 диаметра молекул, действуют силы притяжения. По мере уменьшения расстояния между молекулами сила притяжения сначала увеличиваются, а затем начинает убывать и убывает до нуля, когда расстояние между двумя молекулами становится равным сумме радиусов молекул.
При дальнейшем уменьшении расстояния электронные оболочки атомов начинают перекрываться и между молекулами возникают быстро нарастающие силы отталкивания.
4. Строение газообразных, жидких и твердых тел
Газы. В газах расстояние между атомами или молекулами в среднем во много раз больше размеров самих молекул. Например, при атмосферном давлении объем сосуда в десятки тысяч раз превышает объем находящихся в нем молекул.
Газы легко сжимаются, при этом уменьшается среднее расстояние между молекулами, но молекулы не сдавливают друг друга.
Молекулы с огромными скоростями — сотни метров в секунду -движутся в пространстве. Сталкиваясь, они отскакивают друг от друга в разные стороны подобно бильярдным шарам. Слабые силы притяжения молекул газа не способны удержать их друг возле друга. Поэтому газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объема. Многочисленные удары молекул о стенки сосуда создают давление газа.
Жидкости. Молекулы жидкости расположены почти вплотную друг к другу, поэтому молекула жидкости ведет себя иначе, чем молекула газа. В жидкостях существует так называемый ближний порядок, т. е. упорядоченное расположение молекул сохраняется на расстояниях, равных нескольким молекулярным диаметрам. Молекула колеблется около своего положения, сталкиваясь с соседними молекулами. Лишь время от времени она совершает очередной «прыжок», попадая в новое положение равновесия. В этом положении равновесия сила отталкивания равна силе притяжения, т.е. суммарная сила взаимодействия молекулы равна нулю. Время оседлой жизни молекулы воды, т. е. время ее колебаний около одного определенного положения равновесия при комнатной температуре, равно в среднем 10-11 с. Время же одного колебания значительно меньше (10-12-10-13 с). С повышением температуры время оседлой жизни молекул уменьшается. Характер молекулярного движения в жидкостях, впервые установленный советским физиком Я.И. Френкелем, позволяет понять основные свойства жидкостей. Молекулы жидкости находятся непосредственно друг возле друга. При уменьшении объема силы отталкивания становятся очень велики. Этим и объясняется малая сжимаемость жидкостей. Как известно, жидкости текучи, т. е. не сохраняют своей формы. Объяснить это можно так. Внешняя сила заметно не меняет числа перескоков молекул в секунду. Но перескоки молекул из одного оседлого положения в другое происходят преимущественно в направлении действия внешней силы (рис.8.8). Вот почему жидкость течет и принимает форму сосуда.
Атомы или молекулы твёрдых тел колеблются около определённых положений равновесия, поэтому твёрдые тела сохраняют не только объём ,но и форму
Если соединить центр равновесия атомов или ионов твёрдого тела, то получится правильная пространственная решётка, называемая кристалической
Кристаллы — это твёрдые тела, атомы или молекулы которых занимают определённое, порядочное положение в пространстве. Поэтому кристаллы имеют плоские грани. Например крупинка обычной поваренной соли имеет плоские грани, составляющие друг с другом прямые углы.
Правильная внешняя форма не единственное и даже не самое главное следствие упорядоченного строения кристалла. Главное- это зависимость физических свойств от выбранного в кристалле направления. Например, кусок слюды легко расслаивается в одном из направлений на тонкие пластинки, но разорвать его в направлении, перпендикулярном пластинкам, гораздо труднее. Многие кристаллы по-разному проводят теплоту и электрический ток в различных направлениях. От направления зависят и оптические свойства кристаллов. Так, кристалл кварца по-разному преломляет свет в зависимости от направления падающих на него лучей. Зависимость физических свойств от направления внутри кристалла называют анизотропией. Все кристаллические тела анизотропны.
Монокристаллы и поликристаллы.
Кристаллическую структуру имеют металлы. Если взять большой кусок металла, то на первый взгляд его кристаллическое строении никак не проявляется ни во внешнем виде куска, ни в его физических свойствах
Обычно металл состоит из огромного количества сросшихся друг с другом маленьких кристалликов. Свойства каждого кристаллика зависят от направления, но кристаллики ориентированы по отношению к друг другу беспорядочно. В результате в объеме, значительно превышающем объем отдельных кристалликов, все направления внутри металлов равноправны и свойства металлов одинаковы по всем направлениям.
Твердое тело, состоящее из большого числа маленьких кристалликов, называют поликристаллическим. Одиночные кристаллы называют монокристаллами.
5. Броуновское движение
Броуновское движение- это тепловое движение взвешенных в жидкости( или газе) частиц.
Наблюдения броуновского движения. Английский ботаник Р.Броун (1773-1858) впервые наблюдал это явление 1827 г. Рассматривая в микроскоп взвешенные в воде споры плауна. Позже он рассматривал и другие мельчайшие частицы, в том числе частички камня египетских пирамид. Сейчас для наблюдения броуновского движения используют частички краски гуммируют, которая нерастворима в воде. Эти частички совершают беспорядочное движение. Броуновское движение — тепловое движение, и оно не может прекратиться. С увеличением температуры интенсивность его растёт. Положения частиц, отмеченные точками, определены через равные промежутки времени — 30 с. Броуновское движение можно наблюдать и в газе. Его совершают взвешенные в воздухе частицы пыли или дыма.
Газы — агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь предоставленный им объём. Вещество в газообразном состоянии широко распространено в природе. Газы образуют атмосферу Земли, в значительных количествах содержатся в твёрдых земных породах, растворены в воде океанов, морей и рек.
Жидкость — агрегатное состояние вещества, промежуточное между твёрдым и газообразным состояниями. Ж., сохраняя отдельные черты как твёрдого тела, так и газа, обладает, однако, рядом только ей присущих особенностей, из которых наиболее характерная — текучесть. Подобно твёрдому телу, Ж. сохраняет свой объём, имеет свободную поверхность, обладает определённой прочностью на разрыв при всестороннем растяжении и т. д.
Твёрдое тело — одно из четырёх агрегатных состояний вещества, отличающееся от др. агрегатных состояний стабильностью формы и характером теплового движения атомов, совершающих малые колебания около положений равновесия. Кристаллы характеризуются дальним порядком в расположении атомов. В аморфных телах дальний порядок отсутствует
1. Физика 10 класс Г. Я Мякишев М. «Просвещение» 2007.
2. Арцимович Л. А., Элементарная физика плазмы, 3 изд., М., 2002;
3. Франк-Каменецкий Д. А., Лекции по физике состояний вещества, М., 2003 (переиздание);
4. Френкель Я. И., Собрание избранных трудов, т. 3, М., 2001;
5. Фишер И.3., Статистическая теория жидкостей, М., 2003;
6. Физика простых жидкостей. Экспериментальные исследования, пер. с англ., М., 2002
Размещено на Allbest.ru
Подобные документы
Основные положения атомно-молекулярного учения. Закономерности броуновского движения. Вещества атомного строения. Основные сведения о строении атома. Тепловое движение молекул. Взаимодействие атомов и молекул. Измерение скорости движения молекул газа.
презентация [226,2 K], добавлен 18.11.2013
Анализ теорий, устанавливающих связи между измеряемыми на опыте величинами и свойствами молекул. Идеальный газ как газ, взаимодействие между молекулами которого пренебрежимо мало. Причины возникновения давления газа в молекулярно-кинетической теории.
презентация [151,4 K], добавлен 08.01.2015
Определения молекулярной физики и термодинамики. Понятие давления, основное уравнение молекулярно-кинетической теории. Температура и средняя кинетическая энергия теплового движения молекул. Уравнение состояния идеального газа (Менделеева — Клапейрона).
презентация [972,4 K], добавлен 06.12.2013
Основные понятия и определения молекулярной физики и термодинамики. Основное уравнение молекулярно-кинетической теории. Температура и средняя кинетическая энергия теплового движения молекул. Состояние идеального газа (уравнение Менделеева-Клапейрона).
презентация [1,1 M], добавлен 13.02.2016
Вычисление скорости молекул. Различия в скоростях молекул газа и жидкости. Экспериментальное определение скоростей молекул. Практические доказательства состоятельности молекулярно-кинетической теории строения вещества. Модуль скорости вращения.
презентация [336,7 K], добавлен 18.05.2011
Содержание молекулярно-кинетической теории газов. Химический состав жидкости. Особенности межмолекулярного взаимодействия в данном агрегатном состоянии. Механические и тепловые свойства твердых тел. Практическое применение плазмы — ионизованного газа.
контрольная работа [26,0 K], добавлен 27.10.2010
Характеристика законов Бойля-Мариотта, Бойля-Мариотта, Авогадро. Парциальное давление как давление, которое оказывал бы каждый газ смеси, если бы он один занимал объем, равный объему смеси. Знакомство с положениями молекулярно-кинетической теории газа.
презентация [625,5 K], добавлен 06.12.2016
Изучение корпускулярной концепции описания природы, сущность которой в том, что все вещества состоят из молекул — минимальных частиц вещества, сохраняющих его химические свойства. Анализ молекулярно-кинетической теории газа. Законы для идеальных газов.
контрольная работа [112,2 K], добавлен 19.10.2010
Особенности определения давления газа на стенку сосуда с использованием второго закона Ньютона. Связь этой величины со средней кинетической энергией молекул и их концентрацией. Специфика схематичного вывода основного уравнения упрощенным методом.
презентация [316,6 K], добавлен 19.12.2013
Молекулярная физика как раздел физики, в котором изучаются свойства вещества на основе молекулярно-кинетических представлений. Знакомство с основными особенностями равновесной термодинамики. Общая характеристика молекулярно-кинетической теории газов.
курсовая работа [971,8 K], добавлен 01.11.2013
Работы в архивах красиво оформлены согласно требованиям ВУЗов и содержат рисунки, диаграммы, формулы и т.д.
PPT, PPTX и PDF-файлы представлены только в архивах.
Рекомендуем скачать работу.
Модель строения жидкости в молекулярно-кинетической теории.
Жидкость — вещество в состоянии, промежуточном между твердым и газообразным. Это агрегатное состояние вещества, в котором молекулы (или атомы) связаны между собой настолько, что это позволяет ему сохранять свой объем, но недостаточно сильно, чтобы сохранять и форму.
Свойства жидкостей.
Жидкости легко меняют свою форму, но сохраняют объем. В обычных условиях они принимают форму сосуда, в котором находятся.
Поверхность жидкости, не соприкасающаяся со стенками сосуда, называется свободной поверхностью. Она образуется в результате действия силы тяжести на молекулы жидкости.
Строение жидкостей.
Свойства жидкостей объясняются тем, что промежутки между их молекулами малы: молекулы в жидкостях упакованы так плотно, что расстояние между каждыми двумя молекулами меньше размеров молекул. Объяснение поведения жидкостей на основе характера молекулярного движения жидкости было дано советским ученым Я. И. Френкелем. Оно заключается в следующем. Молекула жидкости колеблется около положения временного равновесия, сталкиваясь с другими молекулами из ближайшего окружения. Время от времени ей удается совершить «прыжок», чтобы покинуть своих соседей из ближайшего окружения и продолжать совершать колебания уже среди других соседей. Время оседлой жизни молекулы воды, т. е. время колебания около одного положения равновесия при комнатной температуре, равно в среднем 10 -11 с. Время одного колебания значительно меньше — 10 -12 – 10 -13 с.
Поскольку расстояния между молекулами жидкости малы, то попытка уменьшить объем жидкости приводит к деформации молекул, они начинают отталкиваться друг от друга, чем и объясняется малая сжимаемость жидкости. Текучесть жидкости объясняется тем, что «прыжки» молекул из одного оседлого положения в другое происходят по всем направлениям с одинаковой частотой. Внешняя сила не меняет заметным образом число «прыжков» в секунду, она лишь задает их преимущественное направление, чем и объясняется текучесть жидкости и то, что она принимает форму сосуда.
Строение газообразных, жидких и твердых тел
Молекулярно-кинетическая теория дает возможность понять, почему вещество может находиться в газообразном, жидком и твердом состояниях.
Газ. В газах расстояние между атомами или молекулами в среднем во много раз больше размеров самих молекул (рис. 10). Например, при атмосферном давлении объем сосуда в десятки тысяч раз превышает объем находящихся в сосуде молекул газа.
Газы легко сжимаются, так как при сжатии газа уменьшается лишь среднее расстояние между молекулами, но молекулы не «сдавливают» друг друга (рис. 11).
Молекулы с огромными скоростями – сотни метров в секунду – движутся в пространстве. Сталкиваясь, они отскакивают друг от друга в разные стороны подобно бильярдным шарам.
Слабые силы притяжения молекул газа не способны удержать их друг возле друга. Поэтому газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объема.
Многочисленные удары молекул о стенки сосуда создают давление газа.
Жидкости. В жидкостям молекулы расположены почти вплотную друг к другу (рис. 12). Поэтому молекула в жидкости ведет себя иначе, чем в газе. Зажатая, как в клетке, другими молекулами, она совершает «бег на месте» (колеблется около положения равновесия, сталкиваясь с соседними молекулами). Лишь время от времени она совершает «прыжок», прорываясь сквозь «прутья клетки», но тут же попадает в новую «клетку», образованную новыми соседями. Время «оседлой жизни» молекулы воды, т. е. время колебаний около одного определенного положения равновесия, при комнатной температуре равно в среднем 10 –11 с. Время же одного колебания значительно меньше (10 –12 – 10 –13 с). С повышением температуры время «оседлой жизни» молекул уменьшается. Характер молекулярного движения а жидкостях, впервые установленный советским физиком Я. И. Френкелем, позволяет понять основные свойства жидкостей.
Френкель Яков Ильич (1894 – 1952) – выдающийся советский физик-теоретик, внесший значительный вклад в самые различные области физики. Я. И. Френкель – автор современной теории жидкого состояния вещества. Им заложены основы теории ферромагнетизма. Широко известны работы Я. И. Френкеля по атмосферному электричеству и происхождению магнитного поля Земли. Первая количественная теория деления ядер урана создана Я. И. Френкелем.
Молекулы жидкости находятся непосредственно друг возле друга. Поэтому при попытке изменить объем жидкости даже на малую величину начинается деформация самих молекул (рис. 13). А для этого нужны очень большие силы. Этим и объясняется малая сжимаемость жидкостей.
Жидкости, как известно, текучи, т. е. не сохраняют своей формы. Объясняется это следующим. Если жидкость не течет, то перескоки молекул из одного «оседлого» положения в другое происходят с одинаковой частотой но всем направлениям (рис. 12). Внешняя сила заметно не изменяет числа перескоков молекул в секунду, но перескоки молекул из одного «оседлого» положения в другое при этом происходят преимущественно в направлении действия внешней силы (рис. 14). Вот почему жидкость течет и принимает форму сосуда.
Твердые тела. Атомы или молекулы твердых тел в отличие от жидкостей колеблются около определенных положений равновесия. Правда, иногда молекулы изменяют положение равновесия, но происходит это крайне редко. Вот почему твердые тела сохраняют не только объем, но и форму.
Есть еще одно важное различие между жидкостями и твердыми телами. Жидкость можно сравнить с толпой, отдельные члены которой беспокойно толкутся на месте, а твердое тело подобно стройной когорте, члены которой хотя и не стоят по стойке «смирно» (вследствие теплового движения), но выдерживают между собой в среднем определенные интервалы. Если соединить центры положений равновесия атомов или ионов твердого тела, то получится правильная пространственная решетка, называемая кристаллической . На рисунках 15 и 16 изображены кристаллические решетки поваренной соли и алмаза. Внутренний порядок в расположении атомов кристаллов приводит к геометрически правильным внешним формам. На рисунке 17 показаны якутские алмазы.
Качественное объяснение основных свойств вещества на основе молекулярно-кинетической теории, как вы видели, не является особенно сложным. Однако теория, устанавливающая количественные соотношения между измеряемыми на опыте величинами (давлением, температурой и др.) и свойствами самих молекул, их числом и скоростью движения, весьма сложна. Мы ограничимся рассмотрением теории газов.
1. Приведите доказательства существования теплового движения молекул. 2. Почему броуновское движение заметно лишь у частиц малой массы? 3. Какова природа молекулярных сил? 4. Как силы взаимодействия между молекулами зависят от расстояния между ними? 5. Почему два свинцовых бруска с гладкими чистыми срезами слипаются, если их прижать друг к другу? 6. В чем состоит различие теплового движения молекул газов, жидкостей и твердых тел?
молекулярно-кинетическая теория
- 1. Введение 3
- 2. Становление МКТ 3
- 3. Частицы вещества 4
- 4. Движение частиц вещества 5
- 5. Взаимодействие частиц вещества 6
- 6. Кристаллические тела 6
- 7. Аморфные тела 7
- 8. Жидкие тела 8
- 9. Газообразные тела 9
- 10. Заключение 9
Список литературы 10
Начиная с XVIII века, постепенно стала складываться система научных представлений о строении вещества, позднее названная молекулярно-кинетической теорией (МКТ). Молекулярно-кинетическая теория базируется на трёх положениях, обобщающих результаты большого количества экспериментальных данных:
Все тела состоят из мельчайших частиц – атомов, молекул и ионов. Таким образом, любое вещество обладает дискретной структурой. Частицы, образующие вещество, находятся в непрерывном хаотическом движении, которое называется тепловым. Атомы, молекулы и ионы взаимодействуют друг с другом.
До сегодняшнего дня мы изучали физику так называемых макроскопических тел (греч. «макрос» – большой). Это все тела, которые нас окружают: дома, машины, вода в стакане, вода в океане и т.д. Нас интересовало, что происходит с этими телами и вокруг них. Теперь нас будет интересовать также и то, что происходит внутри тел. На этот вопрос нам поможет ответить раздел физики, который называется МКТ.
МКТ – молекулярно-кинетическая теория. Она объясняет физические явления и свойства тел с точки зрения их внутреннего микроскопического строения. В основе этой теории лежат три утверждения:
• Все тела состоят из малых частиц, между которыми есть промежутки.
• Частицы тел постоянно и беспорядочно движутся.
• Частицы тел взаимодействуют друг с другом: притягиваются и отталкиваются.
Эти утверждения называются основными положениями МКТ. Все они подтверждены многочисленными экспериментами. При макроскопическом подходе нас интересуют сами тела: их размеры, объем, масса, энергия и так далее. Взгляните на рисунок слева. Например, макроскопически изучая водяные брызги, мы будем измерять их размеры, объем, массу.
При микроскопическом же подходе нас тоже интересуют размеры, объем, масса и энергия. Однако уже не самих тел, а тех частиц, из которых они состоят: молекул, ионов и атомов. Именно это и символизирует верхний рисунок. Но не следует думать, что молекулы, ионы и атомы можно увидеть в лупу. Этот рисунок – всего лишь художественная гипербола. Увидеть эти частицы можно лишь при помощи особых, так называемых электронных, микроскопов.
МКТ не всегда была научной теорией. Зародившись еще до Нашей эры, молекулярная (или, как ее называли прежде, – атомическая) теория оставалась лишь удобной гипотезой больше двух тысяч лет! И только в XX веке она превращается в полноправную физическую теорию. Вот как говорит об этом знаменитый физик Э.Резерфорд:
«Ни один физик или химик не может закрыть глаза перед той огромной ролью, какую в настоящее время играет в науке атомическая гипотеза. … К концу XIX столетия ее идеи пропитали очень большую область физики и химии. Представление об атомах делалось все более и более конкретным. … Простота и польза атомических воззрений при объяснении самых различных явлений физики и химии, естественно, подняли авторитет этой теории в глазах научных работников. Появилась тенденция рассматривать атомическую гипотезу уже не как полезную рабочую гипотезу, для которой очень трудно найти непосредственные и убедительные доказательства, а как один из твердо обоснованных фактов природы.
Но также не было и недостатка в ученых и философах, которые указывали на необоснованность этой теории, на которой, однако, было построено так много. Можно согласиться с полезностью идеи о молекулах для объяснения данных опытов, но какая у нас уверенность в том, что атомы действительно существуют, а не представляют только фикцию, плод нашей фантазии? Нужно, впрочем сказать, что этот недостаток непосредственных доказательств отнюдь не поколебал веру громадного большинства людей науки в зернистое строение материи.
Отрицание атомической теории никогда еще не способствовало и не будет способствовать открытию новых фактов. Большим преимуществом атомической теории является то, что она дает нам, так сказать, ощутимое конкретное представление о материи, которое не только служит нам для объяснения множества явлений, но оказывает также нам громадные услуги как рабочая гипотеза».
Существование промежутков между частицами. Ученые установили, что вода и спирт состоят из мельчайших частиц, называемых молекулами. Они настолько малы, что не видны даже в микроскоп. Тем не менее, известно, что молекулы спирта в 2-3 раза крупнее молекул воды. Поэтому при сливании жидкостей их частицы перемешиваются, и более мелкие частицы воды размещаются в промежутках между более крупными частицами спирта. Заполнение этих промежутков и способствует уменьшению общего объема веществ.
Малость размеров частиц вещества. Ученые установили, что подобно воде и спирту, марганцовка также состоит из мельчайших частиц. Все они настолько малы, что их нельзя увидеть «по одиночке». Именно поэтому окраска раствора и кажется нам равномерной. Если бы частицы марганцовки были крупнее, то вместо равномерной окраски раствора мы увидели бы прозрачную воду с плавающими в ней частичками марганцовки.
Названия частиц вещества. Это очень сложный вопрос. Мельчайшие частицы воды, спирта, сахара называются молекулами. Марганцовка, соль, ртуть состоят из частиц, называемых ионами. Мельчайшие частицы алмаза, фосфора, гелия называются атомами. Разобраться с названиями всех этих частиц вы сможете лишь тогда, когда изучите основы химии. А пока мы будем вам специально сообщать, как называются частицы изучаемого вами вещества. Например, в соленой воде содержатся следующие частицы: молекулы воды, ионы натрия и хлорид-ионы. А в стальном предмете можно обнаружить ионы железа, атомы углерода и другие частицы.
Неизменность частиц вещества. Как вы знаете, большинство веществ в зависимости от внешних условий (давления и температуры) могут быть либо твердыми, либо жидкими, либо газообразными. Возникает вопрос: одинаковы ли частицы одного и того же вещества, но в различных агрегатных состояниях? Специальными исследованиями установлено, что частицы вещества не изменяются при изменении его агрегатного состояния.
Движение частиц вещества
Движение частиц вещества не может быть обнаружено каким-либо прямым наблюдением: это явление нельзя увидеть ни в лупу, ни в микроскоп. Поэтому ниже описанные опыты не являются доказательствами правильности второго положения МКТ. Они лишь наполняют его конкретным смыслом, то есть служат иллюстрациями.
Броуновское движение. Однажды в 1827 г. английский ученый Р.Броун, изучая растения при помощи микроскопа, обнаружил очень необычное явление. Плавающие на воде споры (мелкие семена некоторых растений) при наблюдении за ними в микроскоп скачкообразно двигались без видимых на то причин (см. рисунок). Броун наблюдал это движение несколько дней, однако так и не смог дождаться его прекращения. Он его подробно описал, но объяснить так и не смог. Впоследствии это явление назвали броуновским движением.
Объяснить это явление невозможно, если только не предположить, что молекулы воды находятся в постоянном, никогда не прекращающемся движении. Они беспорядочно сталкиваются друг с другом, с другими молекулами. Наталкиваясь на споры, молекулы вызывают их скачкообразные перемещения, что Броун и наблюдал в микроскоп. А поскольку молекулы в микроскоп не видны, то движение спор казалось Броуну беспричинным.
Диффузия объясняется просто. Частицы веществ, беспорядочно двигаясь, проникают в промежутки друг между другом, что и означает смешивание веществ. Наиболее быстро диффузия происходит в газах. Медленнее – в жидкостях, а в твердых телах – совсем медленно: годами. Известен, например, следующий опыт. Две гладко отшлифованные пластины из золота и свинца пролежали друг на друге около 5 лет. За это время золото и свинец продиффундировали (проникли) друг в друга на глубину около 1 мм.
Скорость движения частиц и температура. Причина диффузии – это самостоятельное движение частиц вещества. Поэтому ускорение диффузии можно объяснить тем, что повышение температуры тела приводит к увеличению скорости движения его частиц. Кстати, броуновское движение при этом также ускоряется.
Итак, при любой температуре наблюдается самостоятельное движение частиц всех веществ – твердых, жидких и газообразных. Поскольку частицы движутся, они обладают кинетической энергией. Эта энергия тем больше, чем выше температура тела.
Взаимодействие частиц вещества
Частицы веществ способны притягиваться друг к другу. Однако это притяжение возникает лишь тогда, когда поверхности тел очень гладкие (для этого и понадобилась зачистка лезвием) и, кроме того, плотно прижаты друг к другу.
Частицы веществ способны отталкиваться друг от друга. Это подтверждается тем, что жидкие, а особенно твердые тела очень трудно сжать. Например, чтобы сдавить резиновый ластик, требуется значительная сила! Ластик гораздо легче изогнуть, чем сдавить.
Притяжение или отталкивание частиц веществ возникает лишь в том случае, если они находятся в непосредственной близости. На расстояниях, чуть больших размеров самих частиц, они притягиваются. На расстояниях, меньших размеров частиц, они отталкиваются. Если же поверхности тел удалены на расстояние, заметно большее, чем размер частиц, то взаимодействие между ними не проявляется никак. Например, нельзя заметить никакого притяжения между свинцовыми цилиндриками, если их сначала не сжать, то есть не сблизить их частицы.
Поскольку частицы вещества взаимодействуют, они обладают потенциальной энергией. Сжимая или растягивая, изгибая или скручивая тело, мы сближаем или удаляем его частицы. Поэтому между ними возникают силы притяжения-отталкивания, которые мы и объединяем термином «сила упругости».
Геологам известно, что в природе встречаются довольно большие монокристаллы (греч. «монос» – один, единственный). Однако большинство кристаллов являются поликристаллами (греч. «полис» – многочисленный). Это значит, что они состоят из многочисленных, сросшихся между собой кристалликов.
Строение монокристаллов. В середине XX века появились особые электронные микроскопы, которые помогли увидеть частицы некоторых веществ. Кроме электронных, можно сделать и рентгеновские фотографии. И все они подтвердят, что частицы кристаллических веществ расположены упорядоченно, образуя множество параллельных рядов. Установлено, что не существует кристаллов без дефектов. Например, в одном из рядов может не хватать нескольких частиц.
Движение частиц кристаллов. В молекулярно-кинетической теории считается, что частицы кристаллических твердых тел непрерывно колеблются около положений равновесия. Размах колебаний частиц невелик по сравнению с размерами самих частиц, поэтому на фотографиях их отклонения незаметны. В модели «кристаллическая решетка» положения равновесия частиц отмечены узлами.
Колебательное движение частиц кристаллов – основное их движение. Однако частицы могут иногда перескакивать с места на место. Этому способствует тот факт, что в кристаллах имеются дефекты. Например, в пустое место в ряду – «дырку» – может перескочить частица из соседнего ряда. В результате образуется новая «дырка». В нее может перескочить частица другого ряда и т.д. Именно благодаря дефектам кристаллического строения твердые тела способны диффундировать друг в друга.
Существуют тела, которые при плавлении не размягчаются, а из твердого состояния превращаются сразу в жидкость. Во время плавления таких тел всегда можно отделить жидкость от еще не расплавившейся (твердой) части тела. Эти тела – кристаллические. Существуют также твердые тела, которые при нагревании постепенно размягчаются, становятся все более текучими. Для таких тел невозможно указать температуру, при которой они превращаются в жидкость (плавятся). Эти тела называют аморфными.
В противоположность кристаллам, которые почти вечно сохраняют собственную форму, аморфные тела даже при невысоких температурах обладают текучестью. Поэтому их можно рассматривать как очень густые и вязкие жидкости.
Строение аморфных тел. Исследования при помощи электронного микроскопа, а также при помощи рентгеновских лучей свидетельствуют, что в аморфных телах не наблюдается строгого порядка в расположении их частиц. Кристаллическое состояние кварца получается, если расплавленный кварц охлаждать медленно. Если же охлаждение расплава будет быстрым, то молекулы не успеют «выстроиться» в стройные ряды, и получится аморфный кварц.
Частицы аморфных тел непрерывно и беспорядочно колеблются. Они чаще, чем частицы кристаллов могут перескакивать с места на место. Этому способствует и то, что частицы аморфных тел расположены неодинаково плотно: между ними имеются пустоты.
Кристаллизация аморфных тел. С течением времени (несколько месяцев, лет) аморфные вещества самопроизвольно переходят в кристаллическое состояние. Например, сахарные леденцы или свежий мед, оставленные в покое в теплом месте, через несколько месяцев становятся непрозрачными. Говорят, что мед и леденцы «засахарились». Разломив леденец или зачерпнув мед ложкой, мы действительно увидим образовавшиеся кристаллики сахара.
Самопроизвольная кристаллизация аморфных тел свидетельствует, что кристаллическое состояние вещества является более устойчивым, чем аморфное. МКТ объясняет это так. Межмолекулярные силы притяжения-отталкивания заставляют частицы аморфного тела перескакивать преимущественно туда, где имеются пустоты. В результате возникает более упорядоченное, чем прежде расположение частиц, то есть образуется поликристалл.
Отличительным признаком жидкости является текучесть – способность изменять форму за малое время под действием даже малой силы. Благодаря этому свойству все жидкости льются в виде струй, разбрызгиваются каплями, принимают форму того сосуда, в который их нальют.
Способность изменять форму у разных жидкостей выражена по-разному. Под действием одной и той же силы (силы тяжести) меду требуется больше времени, чтобы изменить свою форму, чем воде. Говорят, что эти вещества обладают неодинаковой вязкостью: у меда она больше, чем у воды.
Однако, изменяя форму, жидкость не изменяет своего объема. Свойство жидкости сохранять объем иначе называют упругостью жидкости. Еще одним общим свойством всех жидкостей является их способность передавать во все стороны оказываемое на них давление (закон Паскаля). Менее вязкие жидкости делают это быстро, а вязкие – долго. Давление, оказанное на спирт или воду, быстро распространится даже на большое расстояние. А давление, оказанное на густое масло или мед, будет распространяться гораздо медленнее.
Строение жидкостей. В молекулярно-кинетической теории считается, что в жидкостях, как и в аморфных телах, нет строгого порядка в расположении частиц; в разных частях тела они расположены неодинаково плотно. Поэтому межмолекулярные промежутки имеют различные размеры, в том числе и такие, что туда может поместиться еще одна молекула. Это позволяет частицам перескакивать в близлежащие «дырки». Такие перескоки частиц в жидкостях происходят очень часто: несколько миллиардов раз в секунду.
В случае, если на жидкость подействует какая-нибудь внешняя сила, например, сила тяжести, перескоки частиц будут происходить, в основном, в направлении ее действия (то есть вниз). Это приведет к тому, что жидкость примет форму вытягивающейся капли или льющейся струи. Следовательно, текучесть жидкостей объясняется частыми перескоками их частиц из одного устойчивого положения в другое.
В вязких жидкостях, например, меде, перескоки частиц из одного устойчивого положения в другое происходят значительно реже, чем, например, в воде или спирте. Поэтому под действием внешней силы вязкая жидкость будет медленнее изменять свою форму; на это ей на потребуется больше времени. Однако частые ли, редкие ли – любые – перескоки частиц также обуславливают передачу жидкостями давления во всех направлениях (закон Паскаля).
Перескоки частиц жидкостей происходят часто, однако примерно в 100 раз чаще частицы совершают колебания в месте своего последнего перескока. В это время они непрерывно соударяются друг с другом, поэтому даже малое сжатие жидкости приводит к резкому «ожесточению» соударений частиц. Это означает резкое повышение давления жидкости на стенки сосуда, в котором ее сжимают. Другими словами, жидкость будет оказывать сильное сопротивление сжатию. Этим и объясняется упругость жидкости.
Газ – состояние вещества, при котором тело быстро меняет форму и объем под действием даже малой силы. При давлениях, близких к атмосферному, расстояния между частицами газа значительно больше собственных размеров частиц. Частицы газа свободно летают по всему объему сосуда, соударяясь друг с другом и стенками сосуда.
Удары частиц газа о стенки сосуда создают давление газа. Парообразование происходит при любой температуре. При повышении температуры парообразование ускоряется. Парообразование ускоряется также при увеличении площади поверхности тела. Особенно быстро парообразование происходит при кипении, так как жидкость испаряется не только с поверхности, но и внутрь образующихся пузырьков пара.
Пар, находящийся в равновесии со своей жидкостью, называют насыщенным паром. Из всех паров данной жидкости при данной температуре насыщенный пар имеет наибольшую плотность. Давление насыщенного пара не зависит от количества жидкости и пара.
Относительной влажностью воздуха называется физическая величина, равная отношению плотности водяного пара, содержащегося в воздухе, к плотности насыщенного водяного пара при данной температуре. Относительную влажность воздуха обычно выражают в процентах. Гигрометры и психрометры – приборы для измерения относительной влажности воздуха.
Молекулярная гипотеза оставалась лишь гипотезой целых два тысячелетия. Красивой, во многих случаях очень удобной, но – гипотезой. Что же должно было произойти для превращения этой золушки-гипотезы в принцессу-теорию? Важным этапом превращения гипотезы в научную теорию является предсказание фактов, которые могут быть подтверждены экспериментально.
- 1. Богаткина Л.Б. «Об использовании учебников и
учебно-методических пособий по физике в 2004/2005 учебном году» «Физика в школе», 2004, №5, стр.23-28 - 2. Касьянов В.А. «Единый государственный экзамен по физике в России и SAT-II в США» «Физика («Первое сентября»)», 2003, № 40 (23-31 октября), стр.2-6
- 3. Мошейко Л.П. «УМК нового поколения» «Открытая школа», 2004, №4, стр.27-28
- 4. Орлов В.А. «Учебно-методический комплект В.А. Касьянова» «Физика в школе», 2003, №2, стр. 65
- 5. Шабалкина Н. «Выбор без проблем. Преимущества комплекта очевидны» «Учительская газета», 2004, №40 (4.10.2004), стр.11
- 6. Шаронова Н.В. «Сейчас, а не потом! Физика в период модернизации школьного образования» «Учительская газета», 2003, №11-12 (18.03.2003), стр.41
- http://fizclass.ru/osnovnye-polozheniya-molekulyarno-kineticheskoj-teorii-i-ix-opytnoe-obosnovanie/
- http://studfiles.net/preview/3962366/page:11/
- http://otvet.mail.ru/question/190715991
- http://questions-physics.ru/uchebniki/8_klass/zhidkie_tela.html
- http://revolution.allbest.ru/physics/00507166_0.html
- http://www.calc.ru/Model-Stroyeniya-Zhidkosti-V-Molekulyarnokineticheskoy-Teori.html
- http://phscs.ru/physics9/structure
- http://lesnaya.nethouse.ru/articles/38536



