Электролитическая диссоциация — процесс распада электролита на ионы при его растворении или плавлении.
Классическая теория электролитической диссоциации была создана С. Аррениусом и В. Оствальдом в 1887 году. Аррениус придерживался физической теории растворов, не учитывал взаимодействие электролита с водой и считал, что в растворах находятся свободные ионы. Русские химики И. А. Каблукови В. А. Кистяковский применили для объяснения электролитической диссоциации химическую теорию растворов Д. И. Менделеева и доказали, что при растворении электролита происходит его химическое взаимодействие с водой, в результате которого электролит диссоциирует на ионы.
Классическая теория электролитической диссоциации основана на предположении о неполной диссоциации растворённого вещества, характеризуемой степенью диссоциации α, т. е. долей распавшихся молекул электролита. Динамическое равновесие между недиссоциированными молекулами и ионами описывается законом действующих масс .
Вещества, распадающиеся на ионы, называют электролитами. Электролиты – вещества с ионной или сильно ковалентной связью: кислоты, основания, соли. остальные вещества – неэлектролиты; к ним относятся вещества с неполярной или слабо полярной ковалентной связью; например, многие органические соединения.
Основные положения ТЭД (Теории электролитической диссоциации):
Молекулы распадаются на положительно и отрицательно заряженные ионы (простые и сложные).
Под действием электрического тока катионы (положительно заряженные ионы движутся к катоду(-), а анионы (отрицательно заряженные ионы) к аноду(+)
Степень диссоциации зависит от природы вещества и растворителя, концентрации, температуры.
Если степень диссоциации зависит от природы вещества, то можно судить, что существует разграничение между определёнными группами веществ.
Большая степень диссоциации присуща сильным электролитам (большинству оснований, солям, многим кислотам). Стоит учесть, что распад на ионы – обратимая реакция. Так же стоит сказать, что в данной теме не будут разобраны примеры диссоциации двойных и основных солей, их диссоциация описана в теме “соли”.
Примеры сильных электролитов:
NaOH, K2SO4, HClO4
Уравнения диссоциации:
NaOH⇄Na + +OH —
Количественной характеристикой силы электролитов является степень диссоциации (α) – отношение молярной концентрации продиссоциировавшего электролита к его общей молярной концентрации в растворе.
Степень диссоциации выражается в долях единицы или в процентах. Интервал значений – от 0 до 100%.
α = 0% относится к неэлектролитам (диссоциация отсутствует)
У каждой ступени диссоциации своя степень диссоциации.
Например, диссоциация солей CuCl2, HgCl2:
CuCl2⇄Cu 2+ +2Cl — диссоциация протекает полностью
А в случае с хлоридом ртути диссоциация идёт неполностью и то не до конца.
Возвращаясь же к раствору серной кислоты, стоит сказать, что степень диссоциации обеих ступеней разбавленной кислоты гораздо больше, чем у концентрированной. При диссоциации концентрированного раствора очень много молекул вещества и большая концентрация гидроанионов HSO4 — .
У многоосновных кислот и многокислотных оснований диссоциация идёт в несколько ступеней (в зависимости от основности).
Перечислим сильные и слабые кислоты и приступим к уравнениям ионного обмена:
Сильные кислоты ( HCl, HBr, HI, HClO3, HBrO3, HIO3, HClO4, H2SO4, H2SeO4,HNO3, HMnO4, H2Cr2O7)
Химические реакции в растворах и расплавах электролитов протекают с участием ионов. В таких реакциях степени окисления элементов не изменяются, и сами реакции называются реакциями ионного обмена.
Реакции ионного обмена будут протекать до конца (необратимо) , если образуются малорастворимые или практически нерастворимые вещества (они выпадают в осадок), летучие вещества (выделяются в виде газов) или слабые электролиты (например, вода).
Реакции ионного обмена принято писать в три стадии:
1. Молекулярное уравнение
2. Полное ионное уравнение
3. Сокращенное ионное уравнение
При написании обязательно указывать осадки и газы, а так же руководствоваться таблицей растворимости.
Реакции, где все реагенты и продукты получились растворимые в воде, не протекают.
Сокращённое ионное уравнение получается с помощью вычёркивания одинаковых ионов из обеих частей полного ионного уравнения.
Если реакция ионного обмена идёт между двумя солями с образованием осадка, то следует брать два хорошо растворимых реагента. То есть, реакция ионного обмена пойдёт если растворимость реагентов будет выше, чем у одного из продуктов.
Иногда при написании реакций ионного обмена пропускают полное ионное уравнение и сразу пишут сокращенное.
Для получения осадка малорастворимого вещества всегда надо выбирать хорошо растворимые реагенты в их концентрированных растворах.
Например:
2KF+FeCl2→FeF2↓+2KCl
Данные правила подбора реагентов для осаждения продуктов справедливы только для солей.
ЛАБОРАТОРНАЯ РАБОТА 6
ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ. РАСТВОРЫ ЭЛЕКТРОЛИТОВ
Основные понятия теории электролитической диссоциации
Электролиты–это вещества, которые при растворении в полярных растворителях в результате взаимодействия с молекулами последних распадаются на заряженные частицы — ионы. Это явление называется электролитической диссоциацией. К электролитам относятся кислоты, основания и соли. Отношение числа молекул, распавшихся на ионы, к общему числу растворенных молекул электролита называется степенью диссоциации (ά). Степень диссоциации выражают в долях единицы или в процентах.
В зависимости от степени диссоциации электролиты условно разделяют на сильные, средние и слабые. Степень диссоциации сильных электролитов больше 30%, средних — от 2 до 30%, слабых — ниже 2% (в 0,1 н. растворах).
К сильным электролитам относятся: 1) почти все соли (кроме CdCl2, HgCl2, Pb(CH3COO)2, Fe(SCN)3 и некоторых других); 2) кислоты: HHal (кроме НF) , HNO3, H2SO4, HClO4, HCOOH; 3) гидроксиды щелочных и щелочноземельных металлов.
К слабым и средним электролитам относятся: 1) большинство органических кислот; 2) минеральные кислоты: H2CO3, H2S, HCN, HNO2, H2SiO3, H3BO3, HClO, H3PO4, H3PO3, H3AsO4, H3AsO3, H2SO3, НF; 3) большинство оснований металлов (кроме гидроксидов щелочных и щелочноземельных металлов), а также NH4ОН.
При разбавлении раствора степень диссоциации увеличивается. Поэтому при сравнении силы электролитов необходимо брать растворы одинаковой нормальности. Для хорошо растворимых электролитов существует свой предел разбавления, в рамках которого концентрация ионов в единице объема увеличивается с разбавлением вследствие увеличения степени диссоциации. Выше этого предела концентрация ионов уменьшается за счет сильного увеличения объема раствора.
Об относительной силе электролитов можно судить по электропроводности их растворов, а также по химической активности в некоторых реакциях.
Истинная степень диссоциации сильных электролитов в растворах любой концентрации равна 100%. Однако вследствие электростатического притяжения противоположно заряженных ионов, которое особенно значительно в концентрированных растворах, активность ионов снижается и сильный электролит ведет себя так, как если бы он находился в состоянии неполной диссоциации. Поэтому диссоциацию сильных электролитов принято количественно характеризовать кажущейся степенью диссоциации.
Для всех остальных электролитов электролитическая диссоциация является процессом обратимым:
Поэтому в растворах электролитов имеет место равновесие между ионами и недиссоциированными молекулами. Константа равновесия этого обратимого процесса называется константой электролитической диссоциации:
где [К + ] и [А — ] — концентрации в растворе катионов и анионов в моль/л, [KnAm] — концентрация недиссоциированных молекул в моль/л. Для данного электролита значение константы электролитической диссоциации постоянно при определенной температуре и в отличие от степени диссоциации не зависит от концентрации.
Диссоциация электролитов в водных растворах сопровождается гидратацией ионов, т. е. взаимодействием их с полярными молекулами воды. Так, например, в воде по существу нет ионов Zn 2+ или ионов Сг 3+ , а имеются гидратированные комплексные ионы [Zn (Н20)4] 2+ и [Сг (Н20)6] 3+ .
Процесс электролитической диссоциации кислоты следовало бы выражать уравнением: НА + nН2О = Н30 + + А(Н20)n —
Н3О + — ион гидроксония, определяющий общие свойства кислот. Гидратация катионов осуществляется по донорно-акцепторному механизму, а анионов — за счет водородной связи.
На практике обычно пользуются упрощенными уравнениями без учета гидратации ионов:
HN03 ↔ H + + N03 — NaOH ↔ Na + + OH —
Свойства водных растворов кислот и оснований определяются теми ионами, на которые они диссоциируют.
Кислоты можно определить как электролиты, образующие при диссоциации в водных растворах в качестве катионов только ионы водорода, а основания — как электролиты, образующие в качестве анионов только гидроксид-ионы.
Многоосновные кислоты диссоциируют обычно постепенно (ступенчатая диссоциация):
причем по первой ступени степень диссоциации больше, чем по второй.
Ступенчатая диссоциация характерна и для оснований, содержащих несколько гидроксогрупп в молекуле:
1) Mg (OH) ↔ MgOH + + OH — 2) MgOH + ↔ Mg 2+ + OH —
Ступенчатость диссоциации кислот и оснований обусловливает возможность образования кислых и основных солей.
Известны электролиты, которые при диссоциации образуют и ионы водорода, и гидроксид-ионы. Такие соединения называются амфотерными.
Практически амфотерность соединения можно определить по способности его образовывать соли как с кислотами, так и со щелочами. Примером амфотерного электролита может служить гидроксид алюминия Al(OH)3. Уравнения реакций Al(OH)3 с кислотой и с основанием без учёта фактора гидратации могут быть представлены следующим образом.
Характер диссоциации гидроксидов ЭОН зависит от сравнительной степени полярности связей: Э—О и О—Н, которая определяется в основном величинами условных радиусов и зарядов ионов элементов, образующих гидроксид. Если полярность связи Н—О больше полярности связи Э—О, гидроксид диссоциирует по кислотному типу, например:
Если полярность связи Н—О меньше полярности связи Э—О, гидроксид диссоциирует по основному типу, например:
Если полярность связи Н—О примерно равна полярности связи Э—О, то гидроксид диссоциирует по амфотерному типу; например, простейшим амфотерным соединением является вода:
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Сдача сессии и защита диплома — страшная бессонница, которая потом кажется страшным сном. 7964 — 

193.124.117.139 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
18.Характеристики кислот, оснований и солей с точки зрения теории электролитической диссоциации. Амфотерность гидроксидов.
Диссоциация оснований. Согласно теории электролитической диссоциации, основания – это электролиты, которые при диссоциации образуют только один вид анионов – гидроксид-ионы OH : NaOH Na + + OH ; Ca(OH)2 CaOH + + OH ; CaOH + Ca 2+ + OH .
Ступенчатость диссоциации обусловливает возможность образования основных и кислых (см. ниже) солей.
Диссоциация кислот. Кислоты – это электролиты, которые при диссоциации образуют только один вид катионов – катионы водорода H + . HCl H + + Cl ; HNO3 H + + NO3 ; H2SO4 H + + HSO4 — ; HSO4 H + + SO4 2 ; H3PO4 H + + H2PO4 ; H2PO4 H + + HPO4 2 ; HPO4 2 H + + PO4 3 .
Диссоциация амфотерных гидроксидов. Амфотерные гидроксиды дис-социируют в водном растворе как по типу кислоты, так и по типу основания. При их диссоциации одновременно образуются катионы H + и гидроксид-анионы OH : H + + MeO ⇄ MeOH ⇄ Me + + OH .
К ним относятся гидроксиды цинка Zn(OH)2, алюминия Al(OH)3, хрома Cr(OH)3, свинца Pb(OH)2 и др.
1. Средние соли – это электролиты, при диссоциации которых в водных растворах образуются катионы металла и анионы кислотного остатка. Напри-мер, Na2SO4 2 Na + + SO4 2 ; Ca3(PO)4 3 Ca 2+ + 2 PO4 3 .
2.Кислые соли при растворении в воде образуют катион металла и сложный анион из атомов водорода и кислотного остатка: KHSO3 K + + HSO3 ( = 1).
Сложный анион диссоциирует частично: HSO3 ⇄ H + + SO3 2 ( : Al(OH)2Cl Al(OH)2 + + Cl ( = 1).
Сложный катион диссоциирует частично: Al(OH)2 + ⇄ AlOH 2+ + OH ( 2+ ⇄ Al 3+ + OH ( + + Al 3+ + 2 SO4 2 ;
Сложные соли диссоциируют на катион металла и анионы кислотных остатков. Например, ZnClNO3 Zn 2+ + Cl + NO3 ;
19. Окислительно-восстановительные реакции (овр). Степень окисления атомов Основные окислители и восстановители. Составление уравнений овр методами электронного и электронно-ионного баланса.
ОВР-реакции, протекающие с изменением степени окисления.
Окисление – это процесс отдачи электронов при этом происходит понижение степени окисления.
Восстановление – это процесс присоединения электронов, при этом происходит понижение степени окисления.
Реакции, в кот. ок-ль. и восст-ль предс. собой различные ве-ва наз. межмолеклярными. Если ок-ль и восс-ль атомы одной молекулы — внутримолекулярные.
Под степенью окисления (окислительным числом) понимают условный заряд атома в соединении, вычисленный из предположения, что в молекуле все связи ионные. Степень окисления указывает, сколько электронов оттянуто от атома (положительная степень окисления) или притянуто к нему от другого атома (отрицательная степень окисления). Мера удаления или приближения электронов к атому в степени окисления не отражена.Восстановители
а) Металлы как простые вещества: K 0 , Na 0 , Ca 0 , Al 0 и др.
б) Простые анионы неметаллов: S 2 , Cl , J , Br , Se 2 и др.
в) Сложные анионы и молекулы, содержащие электроположитель-ные элементы в промежуточной степени окисления: S +4 O3 2 , N +3 O2 , As +3 O3 3 , Cr +3 O2 , [Fe +2 (CN)6] 4 , C +2 O, N +2 O, S +4 O2 и др.
г) Простые катионы в низшей степени окисления: Fe 2+ , Sn 2+ , Cr 3+ , Cu + , Mn 2+ , As 3+ и др.
д) Некоторые простые вещества:
е) Катод при электролизе.
а) Неметаллы как простые вещества с большой электроотрицательностью: F2, O2, Cl2 и др.
б) Простые катионы в высокой степени окисления: Sn 4+ , Fe 3+ , Cu 2+ и др., а также H + .
г) Сложные ионы и молекулы, содержащие атомы неметаллов в положительной степени окисления: H2S +6 O4, S +6 O3, HOCl +1 , HCl +5 O3,
д) Анод при электролизе.
В соединениях, когда атомы находятся в промежуточной степени окисления, последние могут проявлять как восстановительные, так и окислительные свойства (окислительно-восстановительная двойствен-ность):
Применяют два метода составления уравнений реакций окисления-восстановления:
Электролитическая диссоциация
Самопроизвольный частичный или полный распад растворенных электролитов на ионы называется электролитической диссоциацией. Термин «ионы» введен английским физиком М. Фарадеем (1833). Теория электролитической диссоциации была сформулирована шведским ученым С. Аррениусом (1887) для объяснения свойств водных растворов электролитов. В дальнейшем она развивалась многими учеными на основе учения о строении атома и химической связи. Современное содержание этой теории можно свести к следующим трем положениям:
1. Электролиты при растворении в воде диссоциируют (распадаются) на ионы — положительно и отрицательно заряженные. («Ион» в переводе с греческого означает «странствующий». В растворе ионы беспорядочно движутся в различных направлениях.)
2. Под действием электрического тока ионы приобретают направленное движение: положительно заряженные движутся к катоду, отрицательно заряженные — к аноду. Поэтому первые называются катионами, вторые — анионами. Направленное движение ионов происходит в результате притяжения их противоположно заряженных электродами.
3. Диссоциация — обратимый процесс. Это означает, что наступает такое состояние равновесия, при котором сколько молекул распадается на ионы (диссоциация), столько их вновь образуется из ионов (ассоциация). Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставят знак обратимости.
где KA — молекула электролита, K + — катион, A − — анион.
Учение о химической связи помогает ответить на вопрос, почему электролиты диссоциируют на ионы. Легче всего диссоциируют вещества с ионной связью, так как они уже состоят из ионов (см. Химическая связь). При их растворении диполи воды ориентируются вокруг положительного и отрицательного ионов. Между ионами и диполями воды возникают силы взаимного притяжения. В результате связь между ионами ослабевает, происходит переход ионов из кристалла в раствор. Аналогично диссоциируют и электролиты, молекулы которых образованы по типу ковалентной полярной связи. Диссоциация полярных молекул может быть полной или частичной — всё зависит от степени полярности связей. В обоих случаях (при диссоциации соединений с ионной и полярной связью) образуются гидратированные ионы, т. е. ионы, химически связанные с молекулами воды.
Основоположником такого взгляда на электролитическую диссоциацию был почетный академик И. А. Каблуков. В отличие от теории Аррениуса, не учитывавшей взаимодействия растворенного вещества с растворителем, И. А. Каблуков к объяснению электролитической диссоциации применил химическую теорию растворов Д. И. Менделеева. Он показал, что при растворении происходит химическое взаимодействие растворенного вещества с водой, которое приводит к образованию гидратов, а затем они диссоциируют на ионы. И. А. Каблуков полагал, что в водном растворе содержатся только гидратированные ионы. В настоящее время это представление общепринято. Итак, гидратация ионов — основная причина диссоциации. В других, неводных растворах электролитов химическая связь между частицами (молекулами, ионами) растворенного вещества и частицами растворителя называется сольватацией.
Гидратированные ионы имеют как постоянное, так и переменное число молекул воды. Гидрат постоянного состава образует ионы водорода Н + , удерживающие одну молекулу воды,— это гидратированный протон H + (H2O). В научной литературе его принято изображать формулой H3O + (или OH3 + ) и называть ионом гидроксония.
Поскольку электролитическая диссоциация — процесс обратимый, то в растворах электролитов наряду с их ионами присутствуют и молекулы. Поэтому растворы электролитов характеризуются степенью диссоциации (обозначается греческой буквой а). Степень диссоциации — это отношение числа молекул, распавшихся на ионы, n к общему числу растворенных молекул N:
Степень диссоциации электролита определяется опытным путем и выражается в долях единицы или в процентах. Если α = 0, то диссоциация отсутствует, а если α = 1, или 100%, то электролит полностью распадается на ионы. Различные электролиты имеют различную степень диссоциации. С разбавлением раствора она увеличивается, а при добавлении одноименных ионов (одинаковых с ионами электролита) — уменьшается.
Однако для характеристики способности электролита диссоциировать на ионы степень диссоциации не очень удобная величина, так как она. зависит от концентрации электролита. Более общей характеристикой является константа диссоциации K. Ее легко вывести, применив закон действия масс к равновесию диссоциации электролита (1):
где KA — равновесная концентрация электролита, [K + ] и [A − ] — равновесные концентрации его ионов (см. Равновесие химическое). K от концентрации не зависит. Она зависит от природы электролита, растворителя и температуры. Для слабых электролитов чем больше K (константа диссоциации), тем сильнее электролит, тем больше ионов в растворе.
Сильные электролиты констант диссоциации не имеют. Формально их можно вычислить, но они не будут постоянными при изменении концентрации.
Многоосновные кислоты диссоциируют по ступеням, а значит, такие кислоты будут иметь несколько констант диссоциации — для каждой ступени свою. Например:
Всегда K1>K2>K3, т.е. многоосновная кислота при диссоциации по первой ступени ведет себя как более сильная кислота, чем по второй или третьей.
Ступенчатой диссоциации подвергаются и многокислотные основания. Например:
Pb(OH) + ↔ Pb2 + + OH −
Кислые и основные соли также диссоциируют ступенчато. Например:
Mg(OH)Cl ↔ Mg(OH) + + Cl −
Mg(OH) + ↔ Mg 2+ + OH −
При этом на первой ступени соль полностью распадается на ионы, что обусловлено ионным характером связи между Na + и HSO3 − ; Mg(OH) + и Cl − ; диссоциация по второй ступени незначительная, так как заряженные частицы (ионы) дальнейшей диссоциации подвергаются как очень слабые электролиты.
С точки зрения теории электролитической диссоциации даются определения и описываются свойства таких классов химических соединений, как кислоты, основания, соли.
Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только ионы водорода. Например:
Все общие характерные свойства кислот — кислый вкус, изменение цвета индикаторов, взаимодействие с основаниями, основными оксидами, солями — обусловлены присутствием ионов водорода Н + , точнее Н3O + .
Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы:
Ca(OH) + ↔ Ca 2+ + OH −
Согласно теории электролитической диссоциации все общие щелочные свойства растворов — мылкость на ощупь, изменение цвета индикаторов, взаимодействие с кислотами, ангидридами кислот, солями — обусловлены присутствием гидроксид-ионов OH − .
Правда, имеются электролиты, при диссоциации которых одновременно образуются и ионы водорода, и гидроксид-ионы. Эти электролиты называются амфотерными или амфолитами. К ним относятся вода, гидроксиды цинка, алюминия, хрома и ряд других веществ. Вода, например, в незначительных количествах диссоциирует на ионы H + и OH − :
Следовательно, у нее в равной мере выражены и кислотные свойства, обусловленные наличием ионов водорода H + , и щелочные свойства, обусловленные наличием ионов OH − .
Диссоциацию гидроксида цинка Zn(OH)2 можно выразить уравнением:
Солями называются электролиты, при диссоциации которых образуются катионы металлов (сюда же относят и катион аммония NH4 + ) и анионы кислотных остатков. Например:
Так диссоциируют средние соли. Кислые же и основные соли, как уже отмечалось, диссоциируют ступенчато.
Поскольку все реакции в водных растворах электролитов представляют собой взаимодействие ионов, уравнения этих реакций можно составлять в ионной форме.
Значение теории электролитической диссоциации состоит в том, что она объяснила многочисленные явления и процессы, протекающие в водных растворах электролитов. Однако она не объясняет процессов, протекающих в неводных растворах. Так, если хлорид аммония в водном растворе ведет себя как соль (диссоциирует на ионы NH4 + Cl − ), то в жидком аммиаке проявляет свойства кислоты — растворяет металлы с выделением водорода. Как основание ведет себя азотная кислота, растворенная в жидком фтороводороде или в безводной серной кислоте.
Все эти факторы противоречат теории электролитической диссоциации. Их объясняет протолитическая теория кислот и оснований.
Сам термин «диссоциация» означает распад молекул на несколько более простых частиц. В химии помимо электролитической диссоциации различают термическую диссоциацию. Это обратимая реакция, происходящая при повышении температуры. Например, термическая диссоциация водяного пара:
молекул иода: I2 ↔ 2I
Равновесие термической диссоциации подчиняется закону действия масс.
Тема №33 «Электролитическая диссоциация электролитов в водных растворах и реакции ионного обмена.»
Тема №33 «Электролитическая диссоциация электролитов в водных растворах и реакции ионного обмена.»
Электролитическая диссоциация электролитов в водных растворах и реакции ионного обмена.
Оглавление
Электролиты и неэлектролиты
Из уроков физики известно, что растворы одних веществ способны проводить электрический ток, а других — нет.
Вещества, растворы которых проводят электрический ток, называются электролитами.
Вещества, растворы которых не проводят электрический ток, называются неэлектролитами. Например растворы сахара, спирта, глюкозы и некоторых других веществ не проводят электрический ток.
Электролитические диссоциация и ассоциация
Почему же растворы электролитов проводят электрический ток?
Шведский ученый С. Аррениус, изучая электропроводность различных веществ, пришел в 1877 г. к выводу, что причиной электропроводности является наличие в растворе ионов, которые образуются при растворении электролита в воде.
Процесс распада электролита на ионы называется электролитической диссоциацией.
С. Аррениус, который придерживался физической теории растворов, не учитывал взаимодействия электролита с водой и считал, что в растворах находятся свободные ионы. В отличие от него русские химики И. А. Каблуков и В. А. Кистяков- ский применили к объяснению электролитической диссоциации химическую теорию Д. И. Менделеева и доказали, что при растворении электролита происходит химическое взаимодействие растворенного вещества с водой, которое приводит к образованию гидратов, а затем они диссоциируют на ионы. Они считали, что в растворах находятся не свободные, не «голые» ионы, а гидратированные, т. е. «одетые в шубку» из молекул воды.
Молекулы воды представляют собой диполи (два полюса), так как атомы водорода расположены под углом 104,5°, благодаря чему молекула имеет угловую форму. Молекула воды схематически представлена ниже.
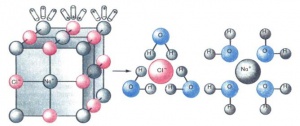
Как правило, легче всего диссоциируют вещества с ионной связью и, соответственно, с ионной кристаллической решеткой, так как они уже состоят из готовых ионов. При их растворении диполи воды ориентируются противоположно заряженными концами вокруг положительных и отрицательных ионов электролита.
Между ионами электролита и диполями воды возникают силы взаимного притяжения. В результате связь между ионами ослабевает, и происходит переход ионов из кристалла в раствор. Очевидно, что последовательность процессов, происходящих при диссоциации веществ с ионной связью (солей и щелочей), будет такой:
1) ориентация молекул (диполей) воды около ионов кристалла;
2) гидратация (взаимодействие) молекул воды с ионами поверхностного слоя кристалла;
3) диссоциация (распад) кристалла электролита на гидратированные ионы.
Упрощенно происходящие процессы можно отразить с помощью следующего уравнения:
Аналогично диссоциируют и электролиты, в молекулах которых ковалентная связь (например, молекулы хлороводорода HCl, смотри ниже); только в этом случае под влиянием диполей воды происходит превращение ковалентной полярной связи в ионную; последовательность процессов, происходящих при этом, будет такой:
1) ориентация молекул воды вокруг полюсов молекул электролита;
2) гидратация (взаимодействие) молекул воды с молекулами электролита;
3) ионизация молекул электролита (превращение ковалентной полярной связи в ионную);
4) диссоциация (распад) молекул электролита на гидратированные ионы.
Схема электролитической диссоциации хлорида натрия на гидратированные ионы
Упрощенно процесс диссоциации соляной кислоты можно отразить с помощью следующего уравнения:
Следует учитывать, что в растворах электролитов хаотически движущиеся гидратированные ионы могут столкнуться и вновь объединиться между собой. Этот обратный процесс называется ассоциацией. Ассоциация в растворах происходит параллельно с диссоциацией, поэтому в уравнениях реакций ставят знак обратимости.
Схема электролитической диссоциации полярной молекулы хлороводорода на гидратированные ионы
Свойства гидратированных ионов отличаются от свойств негидратированных. Например, негидратированный ион меди Cu 2+ — белый в безводных кристаллах сульфата меди (II) и имеет голубой цвет, когда гидратирован, т. е. связан с молекулами воды Cu 2+ • nH2O. Гидратированные ионы имеют как постоянное, так и переменное число молекул воды.
Степень электролитической диссоциации
В растворах электролитов наряду с ионами присутствуют и молекулы. Поэтому растворы электролитов характеризуются степенью диссоциации, которая обозначается греческой буквой а («альфа»).
Степень диссоциации — это отношение числа частиц, распавшихся на ионы (Ng), к общему числу растворенных частиц (Np).
Степень диссоциации электролита определяется опытным путем и выражается в долях или процентах. Если а = 0, то диссоциация отсутствует, а если а = 1, или 100 %, то электролит полностью распадается на ионы. Различные электролиты имеют различную степень диссоциации, т. е. степень диссоциации зависит от природы электролита. Она также зависит и от концентрации: с разбавлением раствора степень диссоциации увеличивается.
По степени электролитической диссоциации электролиты делятся на сильные и слабые.
Сильные и слабые электролиты
Сильные электролиты — это электролиты, которые при растворении в воде практически полностью диссоциируют на ионы. У таких электролитов значение степени диссоциации стремится к единице.
К сильным электролитам относятся:
1) все растворимые соли;
2) сильные кислоты, например: H2SO4, HCl, HNO3;
3) все щелочи, например: NaOH, KOH.
Слабые электролиты — это такие электролиты, которые при растворении в воде почти не диссоциируют на ионы. У таких электролитов значение степени диссоциации стремится к нулю.
К слабым электролитам относятся:
2) водный раствор аммиака NH3 • H2O;
4) некоторые соли.
Константа диссоциации
В растворах слабых электролитов вследствие их неполной диссоциации устанавливается динамическое равновесие между недиссоциированными молекулами и ионами. Например, для уксусной кислоты:
Можно применить к этому равновесию закон действующих масс и записать выражение константы равновесия:
Константу равновесия, характеризующую процесс диссоциации слабого электролита, называют константой диссоциации.
Константа диссоциации характеризует способность электролита (кислоты, основания, воды) диссоциировать на ионы. Чем больше константа, тем легче электролит распадается на ионы, следовательно, тем он сильнее. Значения констант диссоциации для слабых электролитов приводятся в справочниках.
Основные положения теории электролитической диссоциации
1. При растворении в воде электролиты диссоциируют (распадаются) на положительные и отрицательные ионы.
Ионы — это одна из форм существования химического элемента. Например, атомы металла натрия Na 0 энергично взаимодействуют с водой, образуя при этом щелочь (NaOH) и водород Н2, в то время как ионы натрия Na + таких продуктов не образуют. Хлор Cl2 имеет желтозеленый цвет и резкий запах, ядовит, а ионы хлора Cl — бесцветны, не ядовиты, лишены запаха.
Ионы — это положительно или отрицательно заряженные частицы, в которые превращаются атомы или группы атомов одного или нескольких химических элементов в результате отдачи или присоединения электронов.
В растворах ионы беспорядочно передвигаются в различных направлениях.
По составу ионы делятся на простые — Cl — , Na + и сложные — NH4 + , SO2 — .
2. Причиной диссоциации электролита в водных растворах является его гидратация, т. е. взаимодействие электролита с молекулами воды и разрыв химической связи в нем.
В результате такого взаимодействия образуются гидратированные, т. е. связанные с молекулами воды, ионы. Следовательно, по наличию водной оболочки ионы делятся на гидратированные (в раствоpax и кристаллогидратах) и негидратированные (в безводных солях).
3. Под действием электрического тока положительно заряженные ионы движутся к отрицательному полюсу источника тока — катоду и поэтому называются катионами, а отрицательно заряженные ионы движутся к положительному полюсу источника тока — аноду и поэтому называются анионами.
Следовательно, существует еще одна классификация ионов — по знаку их заряда.
Сумма зарядов катионов (Н + , Na + , NH4 + , Cu 2+ ) равна сумме зарядов анионов (Cl — , OH — , SO4 2- ), вследствие чего растворы электролитов (HCl, (NH4)2SO4, NaOH, CuSO4) остаются электронейтральными.
4. Электролитическая диссоциация — процесс обратимый для слабых электролитов.
Наряду с процессом диссоциации (распад электролита на ионы) протекает и обратный процесс — ассоциация (соединение ионов). Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставят знак обратимости, например:
5. Не все электролиты в одинаковой мере диссоциируют на ионы.
Степень диссоциации зависит от природы электролита и его концентрации. Химические свойства растворов электролитов определяются свойствами тех ионов, которые они образуют при диссоциации.
Реакции ионного обмена
Свойства растворов слабых электролитов обусловлены молекулами и ионами, образовавшимися в процессе диссоциации, которые находятся в динамическом равновесии друг с другом.
Запах уксусной кислоты обусловлен наличием молекул CH3COOH, кислый вкус и изменение окраски индикаторов связаны с наличием в растворе ионов H + .
Свойства растворов сильных электролитов определяются свойствами ионов, которые образуются при их диссоциации.
Например, общие свойства кислот, такие как кислый вкус, изменение окраски индикаторов и др., обусловлены наличием в их растворах катионов водорода (точнее, ионов оксония H3O + ). Общие свойства щелочей, такие как мылкость на ощупь, изменение окраски индикаторов и др. связаны с присутствием в их растворах гидроксид-ионов OH — , а свойства солей — с распадом их в растворе на катионы металла (или аммония) и анионы кислотных остатков.
Согласно теории электролитической диссоциации все реакции в водных растворах электролитов являются реакциями между ионами. Этим обусловлена высокая скорость многих химических реакций в растворах электролитов.
Реакции, протекающие между ионами, называют ионными реакциями, а уравнения этих реакций — ионными уравнениями.
Реакции ионного обмена в водных растворах могут протекать:
1. Необратимо, до конца.
2. Обратимо, то есть протекать одновременно в двух противоположных направлениях. Реакции обмена между сильными электролитами в растворах протекают до конца или практически необратимы, когда ионы, соединяясь друг с другом, образуют вещества:
б) малодиссоциирующие (слабые электролиты);
Приведем несколько примеров молекулярных и сокращенных ионных уравнений:
Реакция необратима, т. к. один из ее продуктов — нерастворимое вещество.
Реакция нейтрализации необратима, т. к. образуется малодиссоциирующее вещество — вода.
Реакция необратима, т. к. образуется газ CO2 и малодиссоциирующее вещество — вода.
Если среди исходных веществ и среди продуктов реакции имеются слабые электролиты или малорастворимые вещества, то такие реакции являются обратимыми, т. е. до конца не протекают.
В обратимых реакциях равновесие смещается в сторону образования наименее растворимых или наименее диссоциированных веществ.
Равновесие смещается в сторону образования более слабого электролита — H2O. Однако до конца такая реакция протекать не будет: в растворе остаются недиссоциированные молекулы уксусной кислоты и гидроксид-ионы.
Если исходные вещества — сильные электролиты, которые при взаимодействии не образуют нерастворимых или малодиссоциирующих веществ или газов, то такие реакции не протекают: при смешивании растворов образуется смесь ионов.
Справочный материал для прохождения тестирования:
Электролиты и неэлектролиты.
Проводимость веществами электрического тока или отсутствие проводимости можно наблюдать с помощью простого прибора.
Он состоит из угольных стержней (электродов), присоединенных проводами к электрической сети. В цепь включена электрическая лампочка, которая показывает присутствие или отсутствие тока в цепи. Если опустить электроды в раствор сахара ,то лампочка не загорается. Но она ярко загорится, если их опустить в раствор хлорида натрия.
Вещества, распадающиеся на ионы в растворах или расплавах и потому проводящие электрический ток, называются электролитами.
Вещества, которые в тех же условиях на ионы не распадаются и электрический ток не проводят, называются неэлектролитами.
К электролитам относятся кислоты, основания и почти все соли.
К неэлектролитам относятся большинство органических соединений, а также вещества, в молекулах которых имеются только ковалентные неполярные или малополярные связи .
Электролиты — проводники второго рода. В растворе или расплаве они распадаются на ионы, благодаря чему и протекает ток. Очевидно, чем больше ионов в растворе, тем лучше он проводит электрический ток. Чистая вода электрический ток проводит очень плохо.
Различают сильные и слабые электролиты.
Сильные электролиты при растворении вводе полностью диссоциируют на ионы.
К ним относятся:
1) почти все соли;
2) многие минеральные кислоты, например Н2SO4, HNO3, НСl, HBr, HI, НМnО4, НСlО3, НСlО4;
3) основания щелочных и щелочноземельных металлов.
Слабые электролиты при растворении в воде лишь частично диссоциируют на ионы.
К ним относятся:
1) почти все органические кислоты;
3) многие основания металлов (кроме оснований щелочных и щелочноземельных металлов), а также NH4OH, который можно изображать как гидрат аммиака NH 3∙H 2O.
К слабым электролитам относится вода.
Слабые электролиты не могут дать большой концентрации ионов в растворе.
Основные положения теории электролитической диссоциации.
Распад электролитов на ионы при растворении их в воде называется элекролитической диссоциацией.
Так, хлорид натрия NaСl при растворении в воде полностью распадается на ионы натрия Na + и хлорид-ионы Cl — .
Вода образует ионы водорода Н + и гидроксид-ионы ОН — лишь в очень незначительных количествах.
Для объяснения особенностей водных растворов электролитов шведским ученым С. Аррениусом в 1887 г. была предложена теория электролитической диссоциации . В дальнейшем она была развита многими учеными на основе учения о строении атомов и химической связи.
Современное содержание этой теории можно свести к следующим трем положениям :
1. Электролиты при растворении в воде распадаются (диссоциируют) на ионы — положительные и отрицательные.
Ионы находятся в более устойчивых электронных состояниях, чем атомы. Они могут состоять из одного атома — это
( Na + , Mg 2+ , Аl 3+ и т.д.) — или из нескольких атомов — это
2. Под действием электрического тока ионы приобретают направленное движение: положительно заряженные ионы движутся к катоду, отрицательно заряженные — к аноду. Поэтому первые называются катионами , вторые — анионами .
Направленное движение ионов происходит в результате притяжения их противоположно заряженными электродами.
3. Диссоциация — обратимый процесс: параллельно с распадом молекул на ионы ( диссоциация ) протекает процесс соединения ионов (ассоциация).
Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставят знак обратимости. Например, уравнение диссоциации молекулы электролита КA на катион К + и анион А — в общем виде записывается так:
Теория электролитической диссоциации является одной из основных теорий в неорганической химии и полностью согласуется с атомно-молекулярным учением и теорией строения атома.
Степень диссоциации.
Одним из важнейших понятий теории электролитической диссоциации Аррениуса является понятие
о степени диссоциации.
Степенью диссоциации (а) называется отношение числа молекул, распавшихся на ионы (n’), к общему числу растворенных молекул (n):
Степень диссоциации электролита определяется опытным путем и выражается в долях единицы или в процентах. Если α = 0, то диссоциация отсутствует, а если α = 1 или 100%, то электролит полностью распадается на ионы. Если же α = 20%, то это означает, что из 100 молекул данного электролита 20 распалось на ионы.
Различные электролиты имеют различную степень диссоциации. Опыт показывает, что она зависит от концентрации электролита и от температуры. С уменьшением концентрации электролита, т.е. при разбавлении его водой, степень диссоциации всегда увеличивается. Как правило, увеличивает степень диссоциации и повышение температуры. По степени диссоциации электролиты делят на сильные и слабые.
Рассмотрим смещение равновесия, устанавливающегося между недиссоциированными молекулами и ионами при электролитической диссоциации слабого электролита — уксусной кислоты:
При разбавлении раствора уксусной кислоты водой равновесие сместится в сторону образования ионов, — степень диссоциации кислоты возрастает. Наоборот, при упаривании раствора равновесие смещается в сторону образования молекул кислоты — степень диссоциации уменьшается.
Из этого выражения очевидно, что α может изменяться от 0 (диссоциации нет) до 1 (полная диссоциация). Степень диссоциации часто выражают в процентах. Степень диссоциации электролита может быть определена только экспериментальным путем, например по измерению температуры замерзания раствора, по электропроводности раствора и т. д.
Механизм диссоциации
Легче всего диссоциируют вещества с ионной связью. Как известно, эти вещества состоят из ионов. При их растворении диполи воды ориентируются вокруг положительного и отрицательного ионов. Между ионами и диполями воды возникают силы взаимного притяжения. В результате связь между ионами ослабевает, происходит переход ионов из кристалла в раствор. При этом образуются
, т.е. ионы, химически связанные с молекулами воды.
Аналогично диссоциируют и электролиты, молекулы которых образованы по типу полярной ковалентной связи (полярные молекулы). Вокруг каждой полярной молекулы вещества также ориентируются диполи воды, которые своими отрицательными полюсами притягиваются к положительному полюсу молекулы, а положительными полюсами — к отрицательному полюсу. В результате этого взаимодействия связующее электронное облако (электронная пара) полностью смещается к атому с большей электроотрицательностью, полярная молекула превращается в ионную и затем легко образуются гидратированные ионы:
Диссоциация полярных молекул может быть полной или частичной.
Таким образом , электролитами являются соединения с ионной или полярной связью — соли , кислоты и основания . И диссоциировать на ионы они могут в полярных растворителях.
Константа диссоциации.
Константа диссоциации. Более точной характеристикой диссоциации электролита является константа диссоциации, которая от концентрации раствора не зависит.
Выражение для константы диссоциации можно получить, если записать уравнение реакции диссоциации электролита АК в общем виде:
Поскольку диссоциация является обратимым равновесным процессом, то к этой реакции применим закон действующих масс, и можно определить константу равновесия как:
где К — константа диссоциации, которая зависит от температуры и природы электролита и растворителя, но не зависит от концентрации электролита.
Диапазон констант равновесия для разных реакций очень большой — от 10 -16 до 10 15 . Например, высокое значение К для реакции
означает, что если в раствор, содержащий ионы серебра Ag + ,внести металлическую медь, то в момент достижения равновесия концентрация ионов меди [Cu 2+ ] намного больше, чем квадрат концентрации ионов серебра [Ag + ] 2 . Напротив, низкое значение Кв реакции
говорит о том, что к моменту достижения равновесия растворилось ничтожно малое количество иодида серебра AgI.
Обратите особое внимание на форму записи выражений для константы равновесия.
Если концентрации некоторых реагентов существенно не изменяются в процессе реакции, то они не записываются в выражение для константы равновесия
(такие константы обозначаются К 1 ).
Так, для реакции меди с серебром неправильным будет выражение:
Правильной будет следующая форма записи:
Это объясняется тем, что концентрации металлических меди и серебра введены в константу равновесия. Концентрации меди и серебра определяются их плотностью и не могут быть изменены. Поэтому эти концентрации нет смысла учитывать при расчете константы равновесия.
Аналогично объясняются выражения констант равновесия при растворении AgCl и AgI
Произведение растворимости. Константы диссоциации малорастворимых солей и гидроксидов металлов называются произведением растворимости соответствующих веществ (обозначается ПР).
Для реакции диссоциации воды
выражение константы будет:
, а не
Объясняется это тем, что концентрация воды во время реакций в водных растворах изменяется очень незначительно. Поэтому принимается, что концентрация [Н2О] остается постоянной и вводится в константу равновесия.
Кислоты, основания и соли с позиций электролитической диссоциации.
С помощью теории электролитической диссоциации дают определения и описывают свойства кислот, оснований и солей.
Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода.
Диссоциация многоосновной кислоты протекает главным образом по первой ступени , в меньшей степени по второй и лишь в незначительной степени — по третьей . Поэтому в водном растворе , например , фосфорной кислоты наряду с молекулами Н3РО4 имеются ионы (в последовательно уменьшающихся количествах) Н2РО 2- 4, НРО 2- 4 и РО 3- 4
НРО 2- 4 ↔ Н+ PО З- 4 (третья ступень)
Основностъ кислоты определяется числом катионов водорода, которые образуются при диссоциации.
Так , НCl, HNO3 — одноосновные кислоты — образуется один катион водорода;
Н3 РО4, Н3 АsО4 — трехосновные , так как образуются соответственно два и три катиона водорода.
Из четырех атомов водорода, содержащихся в молекуле уксусной кислоты СН3СООН , только один , входящий в карбоксильную группу — СООН, способен отщепляться в виде катиона Н + , — уксусная кислота одноосновная.
Двух — и многоосновные кислоты диссоциируют ступенчато (постепенно).
Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы.
Основания,растворимые в воде называются щелочами . Их немного . Это основания щелочных и щелочноземельных металлов : LiOH, NaОН, КОН, RbОН, СsОН, FrОН и Са(ОН)2, Sr(ОН)2, Ва(ОН)2, Rа(ОН)2, а также NН4ОН . Большинство оснований в воде малорастворимо.
Кислотность основания определяется числом его гидроксильных групп ( гидроксогрупп ). Например, NН4ОН — однокислотное основание , Са(ОН)2— двухкислотное , Fе(ОН)3 — трехкислотное и т . д . Двух- и многокислотные основания диссоциируют ступенчато
Ca(ОН)2 ↔ Са(ОН) + + OH — (первая ступень)
Ca(OH) + ↔ Ca 2+ + OH — (вторая ступень)
Однако имеются электролиты , которые при диссоциации одновременно образуют катионы водорода, и гидроксид — ионы. Эти электролиты называются амфотерными или амфолитами. К ним относятся вода, гидроксиды цинка, алюминия, хрома и ряд других веществ. Вода, например, диссоциирует на ионы Н + и ОН — (в незначительных количествах):
Следовательно, у нее в равной мере выражены и кислотные свойства, обусловленные наличием катионов водорода Н + , и щелочные свойства, обусловленные наличием ионов ОН — .
Диссоциацию амфотерного гидроксида цинка Zn(ОН)2 можно выразить уравнением
Солями называются электролиты, при диссоциации которых образуются катионы металлов а также катион аммония (NH4) и анионы кислотных остатков
Так диссоциируют средние соли . Кислые же и основные соли диссоциируют ступенчато. У кислых солей вначале отщепляются ионы металлов, а затем катионы водорода. Например:
У основных солей вначале отщепляются кислотные остатки, а затем гидроксид-ионы .
- http://studopedia.ru/9_27582_osnovnie-ponyatiya-teorii-elektroliticheskoy-dissotsiatsii.html
- http://studfiles.net/preview/2180772/page:8/
- http://yunc.org/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D0%B4%D0%B8%D1%81%D1%81%D0%BE%D1%86%D0%B8%D0%B0%D1%86%D0%B8%D1%8F
- http://www.chem-mind.com/2017/04/23/%D1%82%D0%B5%D0%BC%D0%B0-%E2%84%9633-%D1%8D%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BB%D0%B8%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F-%D0%B4%D0%B8%D1%81%D1%81%D0%BE%D1%86%D0%B8%D0%B0%D1%86/
- http://examchemistry.com/content/lesson/himreakcii/eldissociaciya.html