Получить ответ, удовлетворительно объясняющий природу и механизм химической связи, оказалось возможным только после появления квантово-механической теории строения атома, так как при образовании связи проявляются специфические для микрообъектов свойства электронов.
С точки зрения квантовой механики при образовании химической связи между атомами их электронные орбитали перекрываются. В результате в межъядерной области создается повышенная электронная плотность по сравнению с электронной плотностью в изолированных атомах, которая как бы стягивает ядра в единую устойчивую систему.
В силу особенностей электронных состояний между ядрами может образовываться не повышение электронной плотности, а, наоборот, уменьшение ее до нуля. В этом случае химическая связь не образуется.
Причины устойчивости многоатомной частицы заключается в понижении энергии при ее образовании. Рассмотрим, например, изменение энергии при сближении двух атомов водорода, находящихся на бесконечно большом расстоянии (r=¥) друг от друга. Потенциальную энергию при r=¥ примем равной нулю.
Рассматриваемая система состоит из двух протонов и двух электронов. Между частицами возникает два типа сил: силы отталкивания между электронами двух атомов и протонами атомов и силы притяжения между протонами и электронами.
Если спины электронов антипараллельны, то при сближении атомов происходит уменьшение потенциальной энергии системы и при силы притяжения становятся равными силам отталкивания, а энергия системы принимает свое минимальное значение . При дальнейшем сближении атомов силы отталкивания будут больше сил притяжения и потенциальная энергия системы начинает резко возрастать. Графическая зависимость потенциальной энергии системы из двух атомов водорода от межъядерного расстояния, называемая ПОТЕНЦИАЛЬНОЙ КРИВОЙ.
Таким образом, при сближении двух атомов водорода с электронами, обладающими антипараллельными спинами, на расстояние система имеет минимальную энергию и, следовательно, в этом случае образуется устойчивая химическая связь.
В случае, когда спины параллельны, квантово-механические расчеты по уравнению Шредингера показывают, что потенциальная энергия системы при любом расстоянии между сближающимися атомами больше, чем сумма энергий двух отдельных атомов и образование химической связи невозможно. Потенциальная кривая в данном случае выглядит иначе.
В заключение отметим, что в рамках нашей модели ядро атома не закрепляется неподвижно в точке 0. Оно колеблется между точками и . В реальной же двухядерной молекуле колеблются оба ядра, достигая определенных предельных состояний. Молекулы все время как бы растягиваются и сжимаются. При этом — среднее расстояние между ядрами, а — минимальная энергия молекулы с учетом колебания ядер.
А. ШИШЛОВА. по материалам журналов «Успехи физических наук» и «Scientific american».
Чтобы понять, какие трудности испытывает современная квантовая механика, нужно вспомнить, чем она отличается от классической, ньютоновской механики. Ньютон создал общую картину мира, в которой механика выступала как универсальный закон движения материальных точек или частиц — маленьких комочков материи. Из этих частиц можно было построить любые объекты. Казалось, что механика Ньютона способна теоретически объяснить все природные явления. Однако в конце прошлого века выяснилось, что классическая механика неспособна объяснить законы теплового излучения нагретых тел. Этот, казалось бы, частный вопрос привел к необходимости пересмотреть физические теории и потребовал новых идей.
В 1900 году появилась работа немецкого физика Макса Планка, в которой эти новые идеи и появились. Планк предположил, что излучение происходит порциями, квантами. Такое представление противоречило классическим воззрениям, но прекрасно объясняло результаты экспериментов (в 1918 году эта работа была удостоена Нобелевской премии по физике). Спустя пять лет Альберт Эйнштейн показал, что не только излучение, но и поглощение энергии должно происходить дискретно, порциями, и сумел объяснить особенности фотоэффекта (Нобелевская премия 1921 года). Световой квант — фотон, по Эйнштейну, имея волновые свойства, одновременно во многом напоминает частицу (корпускулу). В отличие от волны, например, он либо поглощается целиком, либо не поглощается вовсе. Так возник принцип корпускулярно-волнового дуализма электромагнитного излучения.
В 1924 году французский физик Луи де Бройль выдвинул достаточно «безумную» идею, предположив, что все без исключения частицы — электроны, протоны и целые атомы обладают волновыми свойствами. Год спустя Эйнштейн отозвался об этой работе: «Хотя кажется, что ее писал сумасшедший, написана она солидно», а в 1929 году де Бройль получил за нее Нобелевскую премию.
На первый взгляд, повседневный опыт гипотезу де Бройля отвергает: в окружающих нас предметах ничего «волнового» как будто нет. Расчеты, однако, показывают, что длина дебройлевской волны электрона, ускоренно го до энергии 100 электрон-вольт, равна 10 -8 сантиметра. Эту волну нетрудно обнаружить экспериментально, пропустив поток электронов сквозь кристалл. На кристаллической решетке произойдет дифракция их волн и возникнет характерная полосатая картинка. А у пылинки массой 0,001 грамма при той же скорости длина волны де Бройля будет в 10 24 раз меньше, и обнаружить ее никакими средствами нельзя.
Волны де Бройля непохожи на механические волны — распространяющиеся в пространстве колебания материи. Они характеризуют вероятность обнаружить частицу в данной точке пространства. Любая частица оказывается как бы «размазанной» в пространстве, и существует отличная от нуля вероятность обнаружить ее где угодно. Классическим примером вероятностного описания объектов микромира служит опыт по дифракции электронов на двух щелях. Прошедший через щель электрон регистрируется на фотопластинке или на экране в виде пятнышка. Каждый электрон может пройти либо через правую щель, либо через левую совершенно случайным образом. Когда пятнышек становится очень много, на экране возникает дифракционная картина. Почернение экрана оказывается пропорциональным вероятности появления электрона в данном месте.
Идеи де Бройля углубил и развил австрийский физик Эрвин Шредингер. В 1926 году он вывел систему уравнений — волновых функций, описывающих поведение квантовых объектов во времени в зависимости от их энергии (Нобелевская премия 1933 года). Из уравнений следует, что любое воздействие на частицу меняет ее состояние. А поскольку процесс измерения параметров частицы неизбежно связан с воздействием, возникает вопрос: что же регистрирует измерительный прибор, вносящий непредсказуемые возмущения в состояние измеряемого объекта?
Таким образом, исследование элементарных частиц позволило установить, по крайней мере, три чрезвычайно удивительных факта, касающихся общей физической картины мира.
Во-первых, оказалось, что процессами, происходящими в природе, управляет чистый случай. Во-вторых, далеко не всегда существует принципиальная возможность указать точное положение материального объекта в пространстве. И, в-третьих, что, пожалуй, наиболее странно, поведение таких физических объектов, как «измерительный прибор», или «наблюдатель», не описывается фундаментальными законами, справедливыми для прочих физических систем.
Впервые к таким выводам пришли сами основоположники квантовой теории — Нильс Бор, Вернер Гейзенберг, Вольфганг Паули. Позднее данная точка зрения, получившая название Копенгагенской интерпретации квантовой механики, была принята в теоретической физике в качестве официальной, что и нашло свое отражение во всех стандартных учебниках.
Вполне возможно, однако, что подобные заключения были сделаны слишком поспешно. В 1952 году американский физик-теоретик Дэвид Д. Бом создал глубоко проработанную квантовую теорию, отличную от общепринятой, которая так же хорошо объясняет все известные ныне особенности поведения субатомных частиц. Она представляет собой единый набор физических законов, позволяющий избежать какой-либо случайности в описании поведения физических объектов, а также неопределенности их положения в пространстве. Несмотря на это, бомовская теория до самого последнего времени почти полностью игнорировалась.
Чтобы лучше представить себе всю сложность описания квантовых явлений, проведем несколько мысленных экспериментов по измерению спина (собственного момента количества движения) электрона. Мысленных потому, что создать измерительный прибор, позволяющий точно измерять обе компоненты спина, пока что не удалось никому. Столь же безуспешными оказываются попытки предсказать, какие именно электроны поменяют свой спин в ходе описанного эксперимента, а какие нет.
Эти эксперименты включают в себя измерение двух компонент спина, которые условно будем называть «вертикальным» и «горизонтальным» спинами. Каждая из компонент в свою очередь может принимать одно из значений, которые мы также условно назовем «верхним» и «нижним», «правым» и «левым» спинами соответственно. Измерение основано на пространственном разделении частиц с разными спинами. Приборы, осуществляющие разделение, можно представить себе как некие «черные ящики» двух типов — «горизонтальный» и «вертикальный» (рис. 1). Известно, что разные компоненты спина свободной частицы совершенно независимы (физики говорят — не коррелируют между собой). Однако в ходе измерения одной компоненты значение другой может измениться, причем совершенно неконтролируемым образом (2).
Пытаясь объяснить полученные результаты, традиционная квантовая теория пришла к выводу, что необходимо полностью отказаться от детерминистского, то есть полностью определяющего состояние
объекта, описания явлений микромира. Поведение электронов подчиняется принципу неопределенности, согласно которому компоненты спина не могут быть точно измерены одновременно.
Продолжим наши мысленные эксперименты. Будем теперь не только расщеплять пучки электронов, но и заставим их отражаться от неких поверхностей, пересекаться и снова соединяться в один пучок в специальном «черном ящике» (3).
Результаты этих экспериментов противоречат обычной логике. Действительно, рассмотрим поведение какого-либо электрона в случае, когда поглощающая стенка отсутствует (3 А). Куда он будет двигаться? Допустим, что вниз. Тогда, если первоначально электрон имел «правый» спин, он так и останется правым до конца эксперимента. Однако, применив к этому электрону результаты другого эксперимента (3 Б), мы увидим, что его «горизонтальный» спин на выходе должен быть в половине случаев «правым», а в половине — «левым». Явное противоречие. Мог ли электрон пойти вверх? Нет, по той же самой причине. Быть может, он двигался не вниз, не вверх, а как-то по-другому? Но, перекрыв верхний и нижний маршруты поглощающими стенками, мы на выходе не получим вообще ничего. Остается предположить, что электрон может двигаться сразу по двум направлениям. Тогда, имея возможность фиксировать его положение в разные моменты времени, в половине случаев мы находили бы его на пути вверх, а в половине — на пути вниз. Ситуация достаточно парадоксальная: материальная частица не может ни раздваиваться, ни «прыгать» с одной траектории на другую.
Что говорит в данном случае традиционная квантовая теория? Она просто объявляет все рассмотренные ситуации невозможными, а саму постановку вопроса об определенном направлении движения электрона (и соответственно о направлении его спина) — некорректной. Проявление квантовой природы электрона в том и заключается, что ответа на данный вопрос в принципе не существует. Состояние электрона представляет собой суперпозицию, то есть сумму двух состояний, каждое из которых имеет определенное значение «вертикального» спина. Понятие о суперпозиции — один из основополагающих принципов квантовой механики, с помощью которого вот уже более семидесяти лет удается успешно объяснять и предсказывать поведение всех известных квантовых систем.
Для математического описания состояний квантовых объектов используется волновая функция, которая в случае одной частицы просто определяет ее координаты. Квадрат волновой функции равен вероятности обнаружить частицу в данной точке пространства. Таким образом, если частица находится в некой области А, ее волновая функция равна нулю всюду, за исключением этой области. Аналогично частица, локализованная в области Б, имеет волновую функцию, отличную от нуля только в Б. Если же состояние частицы оказывается суперпозицией пребывания ее в А и Б, то волновая функция, описывающая такое состояние, отлична от нуля в обеих областях пространства и равна нулю всюду вне их. Однако, если мы поставим эксперимент по определению положения такой частицы, каждое измерение будет давать нам только одно значение: в половине случаев мы обнаружим частицу в области А, а в половине — в Б ( 4). Это означает, что при взаимодействии частицы с окружением, когда фиксируется только одно из состояний частицы, ее волновая функция как бы коллапсирует, «схлопывается» в точку.
Одно из основных утверждений квантовой механики заключается в том, что физические объекты полностью описываются их волновыми функциями. Таким образом, весь смысл законов физики сводится к предсказанию изменений волновых функций во времени. Эти законы делятся на две категории в зависимости от того, предоставлена ли система самой себе или же она находится под непосредственным наблюдением и в ней производятся измерения.
В первом случае мы имеем дело с линейными дифференциальными «уравнениями движения», уравнениями детерминистскими, которые полностью описывают состояние микрочастиц. Следовательно, зная волновую функцию частицы в какой-то момент времени, можно точно предсказать поведение частицы в любой последующий момент. Однако при попытке предсказать результаты измерений каких-либо свойств той же частицы нам придется иметь дело уже с совершенно другими законами — чисто вероятностными.
Возникает естественный вопрос: как отличить условия применимости той или другой группы законов? Создатели квантовой механики указывают на необходимость четкого разделения всех физических процессов на «измерения» и «собственно физические процессы», то есть на «наблюдателей» и «наблюдаемых», или, по философской терминологии, на субъект и объект. Однако отличие между этими категориями носит не принципиальный, а чисто относительный характер. Тем самым, по мнению многих физиков и философов, квантовая теория в такой интерпретации становится неоднозначной, теряет свою объективность и фундаментальность. «Проблема измерения» стала основным камнем преткновения в квантовой механике. Ситуация несколько напоминает знаменитую апорию Зенона «Куча». Одно зерно — явно не куча, а тысяча (или, если угодно, миллион) — куча. Два зерна — тоже не куча, а 999 (или 999999) — куча. Эта цепочка рассуждений приводит к некоему количеству зерен, при котором понятия «куча — не куча» станут неопределенными. Они будут зависеть от субъективной оценки наблюдателя, то есть от способа измерений, хотя бы и на глаз.
Все окружающие нас макроскопические тела предполагаются точечными (или протяженными) объектами с фиксированными координатами, которые подчиняются законам классической механики. Но это означает, что классическое описание можно продолжить вплоть до самых малых частиц. С другой стороны, идя со стороны микромира, следует включать в волновое описание объекты все большего размера вплоть до Вселенной в целом. Граница между макро- и микромиром не определена, и попытки ее обозначить приводят к парадоксу. Наиболее четко указывает на него так называемая «задача о кошке Шредингера» — мысленный эксперимент, предложенный Эрвином Шредингером в 1935 году (5).
В закрытом ящике сидит кошка. Там же находятся флакон с ядом, источник излучения и счетчик заряженных частиц, подсоединенный к устройству, разбивающему флакон в момент регистрации частицы. Если яд разольется, кошка погибнет. Зарегистрировал счетчик частицу или нет, мы не можем знать в принципе: законы квантовой механики подчиняются законам вероятности. И с этой точки зрения, пока счетчик не произвел измерения, он находится в суперпозиции двух состояний — «регистрация — нерегистрация». Но тогда в этот момент и кошка оказывается в суперпозиции состояний жизни и смерти.
В действительности, конечно, реального парадокса здесь быть не может. Регистрация частицы — процесс необратимый. Он сопровождается коллапсом волновой функции, вслед за чем срабатывает механизм, разбивающий флакон. Однако ортодоксальная квантовая механика не рассматривает необратимых явлений. Парадокс, возникающий в полном согласии с ее законами, наглядно показывает, что между квантовым микромиром и классическим макромиром имеется некая промежуточная область, в которой квантовая механика не работает.
Итак, несмотря на несомненные успехи квантовой механики в объяснении экспериментальных фактов, в настоящий момент она едва ли может претендовать на полноту и универсальность описания физических явлений. Одной из наиболее смелых альтернатив квантовой механики и стала теория, предложенная Дэвидом Бомом.
Задавшись целью построить теорию, свободную от принципа неопределенности, Бом предложил считать микрочастицу материальной точкой, способной занимать точное положение в пространстве. Ее волновая функция получает статус не характеристики вероятности, а вполне реального физического объекта, некоего квантовомеханического поля, оказывающего мгновенное силовое воздействие. В свете этой интерпретации, например, «парадокс Эйнштейна-Подольского-Розена» (см. «Наука и жизнь» № 5, 1998 г.) перестает быть парадоксом. Все законы, управляющие физическими процессами, становятся строго детерминистскими и имеют вид линейных дифференциальных уравнений. Одна группа уравнений описывает изменение волновых функций во времени, другая — их воздействие на соответствующие частицы. Законы применимы ко всем физическим объектам без исключения — и к «наблюдателям», и к «наблюдаемым».
Таким образом, если в какой-то момент известны положение всех частиц во Вселенной и полная волновая функция каждой, то в принципе можно точно рассчитать положение частиц и их волновые функции в любой последующий момент времени. Следовательно, ни о какой случайности в физических процессах не может быть и речи. Другое дело, что мы никогда не сможем обладать всей информацией, необходимой для точных вычислений, да и сами расчеты оказываются непреодолимо сложными. Принципиальное незнание многих параметров системы приводит к тому, что на практике мы всегда оперируем некими усредненными величинами. Именно это «незнание», по мнению Бома, заставляет нас прибегать к вероятностным законам при описании явлений в микромире (подобная ситуация возникает и в классической статистической механике, например в термодинамике, которая имеет дело с огромным количеством молекул). Теория Бома предусматривает определенные правила усреднения неизвестных параметров и вычисления вероятностей.
Вернемся к экспериментам с электронами, изображенным на рис. 3 А и Б. Теория Бома дает им следующее объяснение. Направление движения электрона на выходе из «вертикального ящика» полностью определяется исходными условиями — начальным положением электрона и его волновой функцией. В то время как электрон движется либо вверх, либо вниз, его волновая функция, как это следует из дифференциальных уравнений движения, расщепится и станет распространяться сразу в двух направлениях. Таким образом, одна часть волновой функции окажется «пустой», то есть будет распространяться отдельно от электрона. Отразившись от стенок, обе части волновой функции воссоединятся в «черном ящике», и при этом электрон получит информацию о том участке пути, где его не было. Содержание этой информации, например о препятствии на пути «пустой» волновой функции, может оказать существенное воздействие на свойства электрона. Это и снимает логическое противоречие между результатами экспериментов, изображенных на рисунке. Необходимо отметить одно любопытное свойство «пустых» волновых функций: будучи реальными, они тем не менее никак не влияют на посторонние объекты и не могут быть зарегистрированы измерительными приборами. А на «свой» электрон «пустая» волновая функция оказывает силовое воздействие независимо от расстояния, причем воздействие это передается мгновенно.
Попытки «исправить» квантовую механику или объяснить возникающие в ней противоречия предпринимали многие исследователи. Построить детерминистскую теорию микромира, например, пытался де Бройль, который был согласен с Эйнштейном, что «Бог не играет в кости». А видный отечественный теоретик Д. И. Блохинцев считал, что особенности квантовой механики проистекают из-за невозможности изолировать частицу от окружающего мира. При любой температуре выше абсолютного нуля тела излучают и поглощают электромаг нитные волны. С позиций квантовой механики это означает, что их положение непрерывно «измеряется», вызывая коллапс волновых функций. «С этой точки зрения никаких изолированных, предоставленных самим себе «свободных» частиц не существует, — писал Блохинцев. — Возможно, что в этой связи частиц и cреды и скрывается природа той невозможности изолировать частицу, которая проявляется в аппарате квантовой механики».
И все-таки — почему же интепретация квантовой механики, предложенная Бомом, до сих пор не получила должного признания в научном мире? И как объяснить почти повсеместное господство традиционной теории, несмотря на все ее парадоксы и «темные места»?
Долгое время новую теорию не хотели рассматривать всерьез на основании того, что в предсказании исхода конкретных экспериментов она полностью совпадает с квантовой механикой, не приводя к существен но новым результатам. Вернер Гейзенберг, например, считал, что «для любого опыта его (Бома) результаты совпадают с копенгагенской интерпретацией. Отсюда первое следствие: интерпретацию Бома нельзя опровергнуть экспериментом. » Некоторые считают теорию ошибочной, так как в ней преимущественная роль отводится положению частицы в пространстве. По их мнению, это противоречит физической реальности, ибо явления в квантовом мире принципиально не могут быть описаны детерминистскими законами. Существует немало и других, не менее спорных аргументов против теории Бома, которые сами требуют серьезных доказательств. Во всяком случае, ее пока что действительно никому не удалось полностью опровергнуть. Более того — работу над ее совершенствованием продолжают многие, в том числе отечественные, исследователи.
34. Молекулы с точки зрения квантовой теории
При сближении атомы, начиная с некоторых расстояний, будут взаимодействовать между собой. Волновые функции наиболее удаленных от ядра электронов начинают перекрываться, что приводит к появлению сил притяжения или отталкивания. Под действием сил притяжения атомы будут объединяться в молекулы. Молекула – наименьшая частица вещества, обладающая его основными химическими свойствами и состоящая из атомов, соединенных между собой химическими связями.
В самом общем виде причина возникновения химической связи состоит в понижении электронной энергии образующейся молекулы по сравнению с суммой электронных энергий исходных атомов. Электронная энергия молекулы определяется взаимодействием каждого электрона с каждым электроном, каждого ядра с каждым ядром и каждого электрона с каждым ядром. Хотя все электронные взаимодействия в молекулах носят обычный электростатический характер, т. е. по своей природе являются кулоновскими, но вследствие волновых свойств электронов представляют собой взаимодействия не точечных зарядов, а электронных облаков. Это обстоятельство автоматически учитывается при решении уравнения Шрёдингера. Электронная энергия молекулы, так же как и электронная энергия атомов, имеет дискретные значения. Однако полная энергия молекулы, в отличие от полной энергии атома, включает в себя не только электронную энергию, но и энергии колебательного движения ядер и вращательного движения молекулы относительно ее центра масс, которые также являются квантованными. Это необходимо учитывать при анализе молекулярных спектров излучения и поглощения.
35. Основные типы химических и межмолекулярных связей. Ионная связь
Атомы в молекулах и кристаллах удерживаются почти полностью силами электростатического притяжения между отрицательно заряженными электронами и положительно заряженными ядрами. Роль сил магнитного происхождения весьма незначительна, а гравитационными силами вообще можно пренебречь. Взаимодействие атомов, возникающее в результате частичного или полного обобществления электронов и сопровождающееся уменьшением полной энергии молекул и кристаллов по сравнению с полной энергией их атомов в свободном состоянии, когда атомы удалены друг от друга на бесконечные расстояния, называется химической связью, а разность этих двух энергий –энергией химической связи.
Различают следующие основные типы химических связей:
1) ионная, или гетерополярная;
2) ковалентная, или гомеополярная;
К основным типам межмолекулярных связей относят связь Ван дер Ваальса и водородную связь. Кратко рассмотрим каждый из названных типов связей.
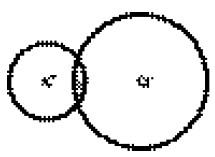
Ионная связь обусловлена электростатическим взаимодействием противоположно заряженных ионов. К числу молекул с ионной связью можно отнести хлориды калия, натрия, окисел магния и прочее, а также кристаллы с аналогичным химическим составом. За счет электростатического притяжения ионы сближаются, их внешние электронные оболочки начинают перекрываться (рис. 1), что приводит к возникновению сил отталкивания.
Рис. 1. Область перекрытия ионов K+ и Cl-, аппроксимированных сферами резко ограниченных радиусов в молекуле KCl
Отталкивание объясняется взаимодействием электронных оболочек ионов с учетом принципа Паули. Этот тип отталкивания является основным во всех молекулах, кроме самых легких (например, H2). Отталкивание связано также с электростатическим взаимодействием ядер, но для всех молекул, за исключением самых легких, оно не является основным. На некотором расстоянии между ядрами силы притяжения уравновешиваются силами отталкивания, при этом энергия молекулы принимает минимальное значение, что соответствует устойчивому состоянию молекулы.
Квантово-механическое рассмотрение химической связи.
Ковалентная связь
Получить ответ, удовлетворительно объясняющий природу и механизм химической связи, оказалось возможным только после появления квантово-механической теории строения атома, так как при образовании связи проявляются специфические для микрообъектов свойства электронов.
С точки зрения квантовой механики при образовании химической связи между атомами их электронные орбитали перекрываются. В результате в межъядерной области создается повышенная электронная плотность по сравнению с электронной плотностью в изолированных атомах, которая как бы стягивает ядра в единую устойчивую систему (рис.1, а). В силу особенностей электронных состояний между ядрами может происходить не повышение электронной плотности, а, наоборот, уменьшение ее до нуля. В этом случае химическая связь не образуется (рис. 1, б). Причины устойчивости многоатомной частицы заключаются в понижении энергии ее образования. Рассмотрим, например, изменение энергии при сближении двух атомов водорода, находящихся на бесконечно большом расстоянии (r = ∞) друг от друга. Потенциальную энергию Е при г = ∞ примем равной нулю.
| Рис.1 Взаимодействие между атомами водорода, приводящее к образованию связи (а) и не приводящее к образованию связи (б) |
Система состоит из двух протонов и двух электронов. Между частицами возникает два типа сил: силы отталкивания между электронами двух атомов и протонами атомов и силы притяжения между протонами и электронами.
Если спины электронов антипараллельны, то при сближении атомов происходит уменьшение потенциальной энергии системы и при r= rсилы притяжения становятся равными силам отталкивания, а энергия системы принимает свое минимальное значение. При дальнейшем сближении атомов силы отталкивания будут больше сил притяжения и потенциальная энергия системы начинает резко возрастать. Графическая зависимость потенциальной энергии системы из двух атомов водорода от межъядерного расстояния, называемая ПОТЕНЦИАЛЬНОЙ КРИВОЙ, представлена на рис.2.
Таким образом, при сближении двух атомов водорода с электронами, обладающими антипараллельными спинами, на расстояние rсистема имеет минимальную энергию и, следовательно, в этом случае образуется устойчивая химическая связь (рис. 2, а).
В случае, когда спины параллельны, квантово-механические расчеты по уравнению Шредингера показывают, что потенциальная энергия системы при любом расстоянии между сближающимися атомами больше, чем сумма энергий двух отдельных атомов и образование химической связи невозможно. Потенциальная кривая в данном случае выглядит иначе (рис. 2, б).
В заключение отметим, что в рамках этой модели ядро атома не закрепляется неподвижно в точке О, а постоянно колеблется. В реальной же двухъядерной молекуле колеблются оба ядра, достигая определенных предельных состояний. Молекулы все время как бы растягиваются и сжимаются. При этом го — среднее расстояние между ядрами, а Еmin— минимальная энергия молекулы с учетом колебания ядер.
 |
Рис 2. потенциальная кривая
Количественные характеристики химической связи
Химическая связь характеризуется рядом параметров. Чаще всего говорят об ее энергии и длине. Если молекула состоит из трех и более атомов, то к перечисленным параметрам добавляют еще один — валентные углы.
ЭНЕРГИЕЙ СВЯЗИ называют ту энергию, которую необходимо затратить для ее разрыва. При этом молекула должна находиться в основном (невозбужденном) состоянии и при 0 о К. Эта величина определяет прочность связи. Чем больше энергия, затрачиваемая на разрыв связи, тем прочнее связь. Единица измерения энергии связи — кДж/моль. Например, энергия связи Н—Н в молекуле водорода равна 436 кДж/моль. Если в молекуле несколько одинаковых связей, то, очевидно, для разрушения каждой следующей потребуется различная энергия и в таком случае говорят о средней энергии связи.
Величина энергии химических связей в большинстве соединений колеблется в пределах 100-1000кДж/моль. Энергия связи в ряду однотипных молекул постепенно изменяется. Например, энергия связи Н-Г в ряду гало-геноводородов HF, HC1, HBr, HI уменьшается с 565,7 кДж/моль у HF, до 294,7 кДж/моль у HI. Зная энергию связей в молекуле, можно судить также о ее реакционной способности и производить различные термохимические расчеты.
ДЛИНОЙ СВЯЗИ называют среднее расстояние между ядрами, отвечающее минимуму энергии системы. На рис. 2. длина связи между атомами водорода измеряется отрезком гo. Современными методами исследования структуры веществ можно определить длины связей с точностью, которую допускает принцип неопределенности.
В ряду аналогичных по составу молекул длины связей также изменяются закономерно. Например, в ряду HF, НС1, HBr, HI длина связи увеличивается с возрастанием размера атома и соответственно равна 0,091; 0,127; 0,141; 0,160нм. Вмолекулах, близких по химической природе, одного гомологического ряда, длины связей между ядрами элементов мало различаются и могут считаться практически постоянными (например, длины связей С — С в предельных углеводородах и т. д.).
Кроме того, на длину связи влияет ее кратность, которая определяется числом электронных пар, связывающих два атома. С увеличением кратности связей происходит их упрочнение, межъядерные расстояния уменьшаются. Так, длина связи С—С равна 0,154 нм, С = С — 0,135 нм и С ≡ С — 0,121 нм.
ВАЛЕНТНЫЕ УГЛЫ. Это углы между связями в молекуле. Их схематически можно представить как углы между прямыми линиями, соединяющими ядра атомов в молекуле. Эти воображаемые прямые, проведенные через два ядра, называют линиями связи. Величины валентных углов зависят от природы атомов и характера связи. Простые двухатомные молекулы всегда имеют линейную структуру. Трехатомные и более сложные молекулы могут обладать различными конфигурациями. Например, в молекуле воды угол между линиями связи Н—О равен 104,5°, а в сходной молекуле сероводорода валентный угол между связями составляет 92°.
Все рассмотренные параметры химической связи можно определить экспериментально при исследовании молекулярных спектров веществ. Их также, в большинстве случаев, можно найти в справочнике.
Для описания и расчета ковалентной связи широко используются два метода — метод валентных связей (МВС) и метод молекулярных орбиталей (ММО).
Метод валентных связей
Основные положения метода валентных связей, базирующиеся на квантово-механической теории строения атома, были разработаны Вальтером Гейтлером и Фритцем Лондоном в 1928 году. В последующем значительный вклад в развитие этого метода внесли Лайнус Полинг и Джон Слейтер. С точки зрения этого метода:
1. В образовании связи участвуют только электроны внешней электронной оболочки атома (валентные электроны).
2. Химическая связь образуется двумя валентными электронами различных атомов с антипараллельными спинами. При этом происходит перекрывание электронных орбиталей и между атомами появляется область с повышенной электронной плотностью, обусловливающая связь между ядрами атомов. Таким образом, в основе МВС лежит образование двухэлектронной, двухцентровой связи.
3. Химическая связь осуществляется в том направлении, в котором обеспечивается наибольшее перекрывание атомных орбиталей.
4. Из нескольких связей данного атома наиболее прочной будет связь, которая получилась в результате наибольшего перекрывания атомных орбиталей.
5. При образовании молекул электронная структура (кроме внешней электронной оболочки) и химическая индивидуальность каждого атома в основном сохраняются.
Известны два механизма образования общих электронных пар: обменный и донорно-акцепторный.
ОБМЕННЫЙ МЕХАНИЗМ объясняет образование ковалентной химической связи участием в ней двух электронов с антипараллельными спинами (по одному от каждого атома).
ДОНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ предполагает образование ковалентной химической связи за счет неподеленной пары (не участвовавшей ранее в образовании связи) одного из связывающихся атомов и вакантной орбитали другого атома. Например, при сближении молекулы аммиака и иона водорода неподеленная пара электронов атома азота занимает вакантную орбиталь иона водорода. Это приводит к образованию общей электронной пары и, следовательно, к образованию химической связи между ними. Первый атом называют ДОНОРОМ, второй — АКЦЕПТОРОМ. Вещества, в которых есть химические связи донорно-акцепторного происхождения, широко распространены среди неорганических соединений. Большая часть таких соединений относится к так называемым комплексным соединениям.
Метод молекулярных орбиталей (ММО)
Метод валентных связей в большинстве случаев позволяет получать правдивую информацию о структуре и свойствах различных молекул и ионов. Однако имеется ряд экспериментальных фактов, которые не могут быть объяснены на основании этого метода. Так, не удается объяснить магнитные свойства ряда веществ (О2, В2 и др.) и существование молекул с нечетным числом электронов (NО и др.).
Эти и другие факты способствовали созданию иного квантово-механического метода описания ковалентной химической связи — МЕТОДА МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ (ММО). Основы ММО разработаны Робертом Малликеном и Фридрихом Хундом (1928-1930 гг.).
В методе МО подход к рассмотрению структуры молекулы близок к тому, которым мы пользовались при рассмотрении строения атома. Метод основан на следующих положениях:
Молекула рассматривается как единая система ядер и электронов, а не как совокупность атомов, сохраняющих некоторую индивидуальность. Она образуется, если энергия такой системы ниже, чем энергия исходных атомов.
Подобно тому как электроны в атомах располагаются на атомных орбиталях (АО), общие электроны в молекуле располагаются на молекулярных орбиталях (МО). Совокупность молекулярных орбиталей, занятых электронами, определяет электронную конфигурацию молекулы.
Существует несколько приближенных методов расчета молекулярных орбиталей. Наиболее простой называется методом линейной комбинации атомных орбиталей (МЛК АО). С точки зрения МЛК АО молекулярную орбиталь рассматривают как линейную комбинациюсоответствующих атомных орбиталеи в изолированных атомах, ядра которых входят в состав молекулы.
4. В образовании молекулярной орбитали участвуют только те АО, которые имеют близкую по величине энергию и приблизительно одинаковую симметрию относительно оси связи.
5. При взаимодействии двух атомных орбиталеи в результате их линейной комбинации образуются две молекулярных орбитали с большей и меньшей энергиями, чемэнергия исходных АО. В результате сложения АО образуется МО с повышенной межъядерной электронной плотностью (меньшей энергией). Такую орбиталь называютсвязывающей. В случае вычитания АО образуется МО с пониженной межъядерной электронной плотностью
(большей энергией), называемая разрыхляющей. Сумма энергии образовавшихся МО в первом приближении равна сумме энергий АО, из которых они образовались.
6. Число всех образовавшихся МО равно сумме АО исходных атомов. При этом число связывающих и разрыхляющих МО одинаково у гомоядерных молекул (содержащих одинаковые ядра) или равно числу участвующих в
образовании связи АО того атома, у которого их меньше.
7. Молекулярные орбитали по аналогии с атомными обозначаются греческими буквами s, p, d. Каждая МОхарактеризуется набором трех квантовых чисел. В соответствии с принципом Паули на молекулярной орбитали, как и на атомной, не может быть больше двух электронов.
8. Все имеющиеся в молекуле электроны распределяются по МО с соблюдением тех же принципов и правил, что и при заполнении электронами орбиталеи в отдельных атомах (принцип наименьшей энергии, принцип Паули, правило Хунда). Электрон, находящийся на связывающей орбитали, увеличивает энергию связи, а электрон, находящийся на разрыхляющей орбитали, ее уменьшает.
9. Стабильность молекулы определяется разностью числа связывающих и разрыхляющих электронов. Если эта разность равна нулю, частица не образуется. Для того, чтобы можно было сопоставить число связей по МВС и
ММО, используют понятие порядок связи (кратность). Порядок связи (N) равен разности между числом электронов, находящихся на связывающих орбиталях, и числомэлектронов на разрыхляющих орбиталях, деленной на 2.
Он может принимать целые или дробные положительныезначения.
Сравнение методов валентных связей и молекулярных орбиталей
Вначале отметим, что методы валентных связей и молекулярных орбиталей являются приближенными. Каждый метод имеет свои преимущества и недостатки.
Метод МО позволяет описывать и прогнозировать свойства молекулы, зависящие от состояния в них отдельных электронов, такие как устойчивость и неустойчивость. Так, например, с точки зрения ММО, устойчив молекулярный ион Щ и, наоборот, неустойчивы Не2, Ве2. С позиций метода ВС это необъяснимо.
В рамках метода МО хорошо объясняются и прогнозируются магнитные свойства молекул, также необъяснимые с позиций МВС. Однако в рассмотренном простейшем варианте ММО не способен передавать насыщаемость ко-валентной связи (т. е. состав молекулы). Для МВС этот недостаток менее характерен. Расчет геометрической структуры и определение важнейших параметров молекулы с помощью ММО является трудной математической задачей, для решения которой необходимы мощные ЭВМ.
Из сказанного выше можно сделать вывод о том, что наиболее общим и последовательным методом для описания строения молекул является метод молекулярных орбиталей. Тем не менее, метод валентных связей дает возможность, основываясь на небольшом числе предположений, связывать между собой в стройную систему важнейшие опытные данные, и применение этого метода во многих случаях более наглядно и вполне оправдано. Спор о том, какой из методов вернее, беспредметен. Правильнее считать, что они взаимно дополняют друг друга.
Свойства ковалентной связи
Ковалентная связь обладает рядом важных свойств. К их числу относятся: насыщаемость и направленность.
НАСЫЩАЕМОСТЬ — характерное свойство ковалентной связи. Она проявляется в способности атомов образовывать ограниченное число ковалентных связей. Это связано с тем, что одна орбиталь атома может принимать участие в образовании только одной ковалентной химической связи. Данное свойство определяет состав молекулярных химических соединений. Так, при взаимодействии атомов водорода образуется молекула Н2, а не Н3. С точки зрения МВС третий атом водорода не может присоединиться, так как спин его электрона окажется параллельным спину одного из спаренных электронов в молекуле. Способность к образованию того или иного числа ковалентных связей у атомов различных элементов ограничивается получением максимального числа неспаренных валентных электронов.
НАПРАВЛЕННОСТЬ — свойство ковалентной связи, определяющее геометрическую структуру молекулы. Причина направленности связи заключается в том, что перекрывание электронных орбиталей возможно только при их определенной взаимной ориентации, обеспечивающей наибольшую электронную плотность в области их перекрывания. В этом случае образуется наиболее прочная химическая связь.
Полярность связей и молекул
В молекулах положительные заряды ядер скомпенсированы отрицательными зарядами электронов. Однако положительные и отрицательные заряды могут быть пространственно разделены. Предположим, что молекула состоит из атомов разных элементов (НС1, СО и т. д.). В этом случае электроны смещены к атому с большей электроотрицательностью и центры тяжести положительных и отрицательных зарядов не совпадают, образуется электрический диполь — система из двух равных по величине и противоположных по знаку зарядов q, находящихся на расстоянии l, называемом длиной диполя. Длина диполя — векторная величина. Ее направление условно принято от отрицательного заряда к положительному. Такие молекулы называют полярными молекулами или диполями.
Полярность молекулы тем больше, чем больше абсолютная величина заряда и длина диполя. Мерой полярности служит произведение q . l, называемое электрическим моментом диполя μ: μ = q . l.
Единицей измерения μ служит Дебай (Д). 1 Д = 3,3 . 10 -30 Кл . м.
В молекулах, состоящих из двух одинаковых атомов μ = 0. Их называют неполярными. Если такая частица попадает в электрическое поле, то в ней под действием поля произойдет поляризация — смещение центров тяжести положительных и отрицательных зарядов. В частице возникает электрический момент диполя, называемый наведенным диполем.
Дипольный момент двухатомной молекулы АВ можно отождествить с дипольным моментом связи А—В в ней. Если общая электронная пара смещена к одному из атомов, то электрический момент диполя связи не равен нулю. Связь в этом случае называется полярной ковалентной связью. Если электронная пара симметрично расположена относительно атомов, то связь называется неполярной.
В многоатомной молекуле определенный электрический момент диполя можно приписать каждой связи. Тогда электрический момент диполя молекулы может быть представлен как векторная сумма электрических моментов диполя отдельных связей. Существование или отсутствие момента диполя у молекулы связано с ее симметрией. Молекулы, имеющие симметричное строение, неполярны (μ = 0). К ним относятся двухатомные молекулы с одинаковыми атомами (Н2, С12 и др.), молекула бензола, молекулы с полярными связями BF3, A1F3, CO2, ВеС12 и др.
Электрический момент диполя молекулы является важным молекулярным параметром. Знание величины μ может указать на геометрическую структуру молекулы. Так, например, полярность молекулы воды указывает на ее угловую структуру, а отсутствие момента диполя СО2 — на ее линейность.
Ионная связь
Предельным случаем ковалентной полярной связи является ионная связь. Если электроотрицательности атомов различаются очень сильно (например, атомов щелочных металлов и галогенов), то при их сближении валентные электроны одного атома полностью переходят на второй атом. В результате этого перехода оба атома становятся ионами и принимают электронную структуру ближайшего благородного газа. Например, при взаимодействии атомов натрия и хлора, они превращаются в ионы Na + и Сl — , между которыми возникает электростатическое притяжение. Ионная связь может быть описана в рамках методов ВС и МО, однако обычно ее рассматривают с помощью классических законов электростатики.
Молекулы, в которых существует в чистом виде ионная связь, встречаются в парообразном состоянии вещества. Ионные кристаллы состоят из бесконечных рядов чередующихся положительных и отрицательных ионов, связанных электростатическими силами. При растворении ионных кристаллов или их плавлении в раствор или расплав переходят положительные и отрицательные ионы.
Следует отметить, что ионные связи обладают большой прочностью, поэтому для разрушения ионных кристаллов необходимо затратить большую энергию. Этим объясняется тот факт, что ионные соединения имеют высокие температуры плавления.
В отличие от ковалентной связи ионная не обладает свойствами насыщаемости и направленности. Причина этого состоит в том, что электрическое поле, создаваемое ионами, имеет сферическую симметрию и действует одинаково на все ионы. Поэтому количество ионов, окружающих данный ион, и их пространственное расположение определяются только величинами зарядов ионов и их размерами.
Рассматривая ионную связь, необходимо иметь в виду, что при электростатическом взаимодействии между ионами происходит их деформация, называемая поляризацией. На рис. 2.1, а изображены два взаимодействующие электростатически нейтральных иона и сохраняющие идеально сферическую форму. На рис. 2.1, б показана поляризация ионов, которая приводит к уменьшению эффективного расстояния между центрами положительных и отрицательных зарядов. Чем больше поляризация ионов, тем меньше степень ионности связи, т. е. тем больше ковалентный характер связи между ними. В кристаллах поляризация оказывается невысокой, т. к. ионы симметрично окружены ионами противоположного знака и ион подвергается одинаковому воздействию во всех направлениях.
 |
| Рис 2.1. Поляризация ионов |
Металлическая связь
Особенностью всех металлов является их высокая электропроводность и теплопроводность. Эти свойства свидетельствуют о том, что валентные электроны способны свободно перемещаться в пределах кристаллической решетки. Простейшая модель строения металла выглядит так: в узлах кристаллической решетки находятся положительные ионы металла, которые прочно связаны электронным газом. Валентные электроны одновременно находятся на всех доступных орбиталях соседних атомов, осуществляя между ними связь. Такая нелокализованная связь называется металлической. Эта связь является достаточно прочной, т. к. большинство металлов имеет высокую температуру плавления. Указанная модель объясняет также свойственные металлам ковкость (способность расплющиваться в тонкие листы) и пластичность (способность вытягиваться в проволоку). Эти свойства обусловлены тем, что подвижный электронный газ позволяет плоскостям, состоящим из положительных ионов, скользить одна по другой.
Более строгую интерпретацию металлической связи позволяет дать метод молекулярных орбиталей. Напомним, что при взаимодействии двух атомных орбиталей образуются две молекулярные орбитали: связывающая и разрыхляющая. Происходит расщепление энергетического уровня на два. Если взаимодействуют одновременно четыре атома металла, образуются четыре молекулярные орбитали. При одновременном взаимодействии N частиц, содержащихся в кристалле, образуется N молекулярных орбиталей, причем величина N может достигать огромных значений, сравнимых с числом Авогадро (6 • 10 23 ). Молекулярные орбитали, образованные атомными орбиталями одного подуровня, находятся настолько близко, что практически сливаются, образуя определенную энергетическую зону.
Рассмотрим в качестве примера электронную структуру кристалла лития. Прежде всего, вспомним электронную конфигурацию молекулы Li2, образовавшуюся издвух изолированных атомов. При взаимодействии N ls-орбиталей в кристалле лития образуется внутренняя энергетическая зона, полностью занятая электронами. Эти электроны не принимают участия в металлической связи. Атом лития имеет один валентный электрон на 2s-орбитали. При взаимодействии N атомов лития 2s -орбитали, на которых находятся валентные электроны, образуют валентную зону. Нижняя часть валентной зоны, образованная связывающими 2s -орбиталями, заполнена электронами, которые перемещаются по кристаллу хаотически. Достаточно близко расположенная верхняя часть, образованная разрыхляющими 2s-opбиталями, электронами не занята. При наложении даже незначительной разности потенциалов электроны возбуждаются и переходят в верхнюю часть валентной зоны, где перемещаются в направлении поля, перенося электрические заряды через весь кристалл. Верхнюю часть валентной зоны называют зоной проводимости. Таким образом, у металлов валентная зона сливается с зоной проводимости. Это связано с тем, что число валентных электронов в атомах металлов относительно невелико и всегда недостаточно для заполнения всех валентных орбиталей.
В атомах неметаллов число валентных электронов велико и валентная зона кристалла практически заполнена электронами. Зона проводимости в кристаллах, содержащих атомы или ионы неметаллов, образуется за счет орбиталей, имеющих намного большую энергию по сравнению с валентными орбиталями, т. е. принадлежащих к следующему электронному уровню. В таких кристаллах между валентной зоной и зоной проводимости находится запрещенная зона. Электроны не могут перемещаться вдоль кристалла, даже если к нему приложить высокое напряжение — такие вещества называются изоляторами или диэлектриками.
Промежуточное положение между проводниками электрического тока и диэлектриками занимают полупроводники (кремний, германий,многие сложные вещества). Особенность полупроводников состоит в том, что у них сравнительно небольшая ширина запрещенной зоны. Поэтому даже при незначительном нагревании электроны переходят в зону проводимости и вещество проводит электрический ток. В некоторых случаях переход электронов в зону проводимости происходит при освещении — возникает фотопроводимость.
В диэлектриках ширина запрещенной зоны более 3 эВ, а в полупроводниках она составляет 0,1—3 эВ.
Под действием внешнего электрического поля на диэлектрик часть его электронов, получив достаточное количество энергии, может переброситься из полностью заполненной валентной зоны в зону проводимости и участвовать в переносе электричества. При этом в валентной зоне появится эквивалентное число так называемых дырок (вакантных мест), имеющих положительный заряд. Они также могут участвовать в переносе тока. Такая проводимость называется электронно-дырочной.
Последнее изменение этой страницы: 2016-12-29; Нарушение авторского права страницы
- http://www.nkj.ru/archive/articles/10957/
- http://studfiles.net/preview/844680/page:17/
- http://infopedia.su/15x1dbf.html