Разделы: Химия
Цель урока: расширить и углубить представления учащихся о химических свойствах кислот.
1. Образовательная: изучить химические свойства кислот с позиции теории электролитической диссоциации.
2. Развивающие (формирование и развитие образовательных компетенций):
а) учебно-познавательных: развитие навыков самостоятельной познавательной деятельности; умения ставить познавательную задачу (целеполагание), умения добывать знания, выделять главное, обобщать, делать выводы, проводить самопроверку и самооценку;
б) коммуникативных: навыков работы в паре, взаимодействия с другими людьми, умения ответить на поставленный вопрос;
в) информационных: проводить материальное и знаковое моделирование, выделять существенные признаки химических реакций, извлекать необходимую информацию из проводимого эксперимента; оформлять и представлять результаты своей работы.
3. Воспитательные: воспитывать сознательное отношение к учебному труду, чувство ответственности, развивать интерес к знаниям.
4. Здоровьесберегающие: закрепить навыки безопасного обращения с реактивами.
Планируемые результаты обучения
В результате изучения данного материала учащиеся должны:
а) определение понятий – электролиты, неэлектролиты, электролитическая диссоциация, кислоты;
б) химические свойства кислот с позиции теории электролитической диссоциации.
Уметь (владеть способами познавательной деятельности):
а) составлять уравнения электролитической диссоциации кислот, оснований, солей;
б) уравнения реакций ионного обмена;
в) проводить реакции ионного обмена, подтверждающие химические свойства кислот, соблюдая правила безопасного обращения с реактивами и выявлять признаки наблюдаемых химических реакций;
г) пользоваться таблицей растворимости.
На доске (слева) записаны этапы урока.
Этапы урока:
- Целеполагание.
- Химическая разминка.
- Лабораторный опыт.
- «Воспоминание о лете».
На доске (центральной части) записаны число и тема урока.
На доске (справа) — «Химический цветок» (на лепестках цветка написать формулы веществ: Аu, Zn, CuO, CO2, NaOH, KCl, Na2SiO3, и слова: фенолфталеин, лакмус; при помощи магнитов прикрепить на доску в виде цветка; в центре которого формула серной кислоты). В начале урока «Химический цветок» не виден.
Подготовка к уроку
Оборудование и реактивы:
- Слайды по теме: «Кислоты», проектор.Все слайды находятся в приложении.
- Лабораторный опыт № 23. Оборудование и реактивы: в ячейках платы: 1, 2-я ячейки – пустые, в 3-ей – магний, 4-ой – медь, 5-ой – СаО, 6-ой – Сu(OH)2.
- Бутыльки c растворами веществ: НСl, Н2SO4; метилоранж, лакмус, фенолфталеин; АgNO3; ВаCl2.
- Выставка (на отдельном столике): ваза с фруктами, кефир, щавель, газированная вода, уксус.
- На столе учителя: магний, соляная кислота, порошок мела в стаканчике, клей канцелярский, спички, металлический штатив, пробирки, палочка, стаканчик.
- «Химический цветок».
- Карточки с формулами кислот для «химической разминки».
- На перемене перед уроком организовать работу магазина.
В ассортименте кислоты:
угольная,
молочная,
аскорбиновая,
лимонная,
ортофосфорная.
Продавцы-учащиеся продают газированную воду, кефир, аскорбиновую кислоту, карамель, желе, пепси-колу. Плата за покупку – выполнение задания (назвать вещества, написанные на карточках, ответить на вопрос по ТЭД).
9) Картинки для оформления «магазина»:
На столах учащихся:
- Оборудование и реактивы к лабораторному опыту.
- Инструкционные карты, листы самопроверки к лабораторному опыту.
- Лист учёта знаний учащихся по теме: «Электролитическая диссоциация».
- Сигнальные карты (карточки из бумаги красного и зелёного цвета, ученик ставит карточку красного цвета, если он испытывает затруднения и ему требуется помощь учителя и зелёную, если он выполнил работу и готов дальше работать самостоятельно).
Дорогие ребята, уважаемые гости, здравствуйте! Вы любите фрукты (слайд №1)?
— А какой вкус у фруктов?
— Чем объясняется кислый вкус фруктов и других продуктов?
Овощи и фрукты содержат органические кислоты: лимонную, яблочную, щавелевую, фумаровую, аскорбиновую и др. Они играют определённую роль в пищеварении, а, следовательно, в нашей жизни. Мы же сегодня поговорим о неорганических кислотах, которые очень важны для человека, так как он использует их в своей практической деятельности, несмотря на то, что с большинством кислот надо обращаться крайне осторожно. Назову некоторые продукты и материалы, при производстве которых используются кислоты: красители, лаки, эмали, минеральные удобрения, инсектициды, пластмассы, волокна, искусственная кожа, каучуки, резина, лекарственные вещества, маргарин, ароматические вещества, пищевые добавки, средства косметики, парфюмерии и многое другое.
Мы же поговорим о кислотах в узком аспекте, потому что тема нашего урока: «Химические свойства кислот с позиции теории электролитической диссоциации» (слайд №2).
Великий Шекспир когда-то сказал: «От кислых яблок сразу скисну», я же пожелаю вам, себе самой и, прежде всего нашим гостям не скиснуть от наших ответов!
II. (1). Целеполагание
Определим цель и задачи урока.
Цель урока: расширить и углубить наши представления о кислотах, ведь они так важны для человека. Сформулировать задачи урока, я надеюсь, поможете мне вы, используя лист учёта знаний по теме. Прошу вас выделить в каждом разделе пункты, которые, на ваш взгляд, соответствуют теме нашего урока.
(Листы учёта знаний по теме ученики получают перед изучением каждой темы, это помогает сделать процесс обучения целенаправленным, учит учащихся выделять главное при изучении темы, осуществлять целеполагание в системе).
Лист учёта знаний учащегося по теме:
«Электролитическая диссоциация» (заполняет ученик)
Знания, умения
Самооценка
хорошо
знаю
Я буду знать:
электролиты, неэлектролиты, электролитическая диссоциация; кислоты, основания, химическое равновесие,
качественные реакции
веществ с ионной связью на примере хлорида натрия
Качественные реакции на анионы
Химические свойства кислот, оснований, солей с точки зрения ТЭД и ОВр
Я буду уметь:
Составлять уравнения ЭД кислот, оснований и солей
Пользоваться таблицей растворимости
Составлять уравнения реакций ионного обмена
Решать задачи «на избыток»
Проводить реакции ионного обмена, соблюдая правила безопасного обращения с реактивами
Решать экспериментальные задачи, используя знания химических свойств веществ и знания качественных реакций на анионы
ОУУН
Планировать свою учебную деятельность
Активно участвовать в организации работы в паре
Осуществлять самоконтроль и давать самооценку своей деятельности
Уметь выделять главное, делать выводы
Слушать объяснение учителя
Работать с дополнительной литературой
Отвечать на вопросы в соответствии с их характером
Составлять и использовать таблицы
Вести записи в тетради в соответствии с требованиями
(Учащиеся выделяют пункты: I — 1,4; II — 2,3,5; III — 2,3,4,5,7,8. Учитель корректирует.)
Прочтём ещё раз тему урока и расшифруем каждое слово в этом непростом для «нехимического» взгляда предложении.
— Что такое диссоциация?
— Что такое электролиты?
— На какие ионы распадаются кислоты в растворах?
— Какое определение даёт эта теория кислотам? (Слайд №3.)
— Что значит «описать химические свойства кислот»?
Нам предстоит большая и серьёзная работа. Этапами сегодняшнего урока являются:
1. Целеполагание.
2. Химическая разминка.
3. Лабораторный опыт.
4. «Воспоминание о лете».
Итак, первый этап пройден.
— Понятны ли вам тема, цель и задачи урока?
Тогда переходим к химической разминке.
III. Подготовка к восприятию нового материала
2. Химическая разминка
а) Работа с карточками, словарная работа. Учитель показывает карточки с формулами кислот, солей, ионов – ученики называют вещества или ионы.
б) Упражнение на синтез знаний (слайд №4).
Перед нами ряды формул или названий веществ, ответьте на вопрос.
— Как назвать их одним словом (психологи называют это «синтезом»)? (Кислоты, индикаторы, металлы, основные оксиды, основания, соли.)
— Какова логическая взаимосвязь указанных понятий с кислотами? (Кислоты взаимодействуют с ними, а именно: с индикаторами, металлами, основными оксидами, основаниями, солями.)
Сейчас нам предстоит проделать эти реакции и объяснить их с новой точки зрения – с позиции теории электролитической диссоциации.
(На экране появляется слайд №5.)
IV. (3). Лабораторный опыт № 3 (23)
Тема: «Химические свойства кислот с позиции теории электролитической диссоциации».
Работа с инструкционной картой
Прочитайте тему лабораторного опыта, уясните цель.
Расскажу вам о Юстусе Либихе, знаменитом учёном-химике ХIХ века. «Вот как описывает Карл Фогт – химик, работавший вместе с Либихом один случай. Входит Либих, у него в руках склянка с притёртой пробкой. «Ну-ка, обнажите руку», — говорит он Фогту и влажной пробкой прикасается к руке. «Не правда, ли, жжёт? – невозмутимо спрашивает Либих. – Я только что добыл безводную муравьиную кислоту». Как вы думаете, правильно ли обращался Либих с кислотами? Конечно, неправильно; после этой пробы у Фогта долго болела рука, и остался белый шрам на руке.
— А вы знаете, как обращаться с кислотами и другими реактивами? (Ученики проговаривают правила обращения с реактивами.)
Будьте предельно осторожны, берегите глаза! Кому понятны техника безопасности, название опыта, цель и ход работы поднимите руки.
В качестве напутствия я хотела бы привести слова Козьмы Пруткова: «Бросая в воду камешки, гляди на круги, ими образуемые, иначе такое бросание обратится пустою забавою…».
Проводя опыт, сделайте выводы и найдите ответ на вопросы, изображенные на экране (слайд №5).
— Как объясняет ТЭД химические свойства кислот?
— Почему у кислот есть общие свойства? Это самый главный вопрос сегодняшнего урока.
Лабораторный опыт № 3
Тема: «Химические свойства кислот с позиции теории электролитической диссоциации».
Цели:
- проделать реакции, характерные для кислот на примере серной кислоты,
- сделать вывод о химических свойствах кислот,
- закрепить навыки безопасного обращения с реактивами.
Действие кислот на индикаторы
Раствор серной кислоты налейте в три ячейки. В первую ячейку добавьте раствор фиолетового лакмуса, во вторую — раствор метилоранжа, в третью – раствор фенолфталеина. Что вы наблюдаете?
Уровень 1. Вставьте пропущенные слова в предложении: «Кислоты изменяют окраску индикаторов: фиолетового лакмуса – в ………………………………………, метилоранжа – ……………………………. …., фенолфталеин остаётся…………………………………..…….
Уровень 2. Напишите уравнение диссоциации серной кислоты.
Взаимодействие кислот с металлами
В четвёртой ячейке лежит магний, в пятой – медь. Добавьте в эти ячейки раствор серной кислоты. Что вы наблюдаете? Сравните результаты.
Уровень 1. Запишите уравнения практически осуществимых реакций в молекулярном и ионном видах.
Вывод. Кислоты взаимодействуют с металлами, стоящими в электрохимическом ряду напряжений металлов до………………………………………………………………………. ….
Уровень 2. Запишите уравнения практически осуществимых реакций в молекулярном и ионном видах:
а) магний + серная кислота —>
б) медь + серная кислота —>
Взаимодействие кислот с основными оксидами
Опыт взаимодействия оксида меди (II) с серной кислотой будет демонстрировать учитель на видео, вам нужно предположить: растворится ли оксид меди (II) в серной кислоте?
Уровень 1. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что формулы оксидов пишутся в молекулярном виде).
Уровень 2. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что оксиды — неэлектролиты).
Оксид меди (II) + серная кислота >
Взаимодействие кислот с основаниями
В седьмой ячейке находится гидроксид меди (II), добавьте к нему серную кислоту, перемешайте стеклянной палочкой. Что наблюдаете?
Уровень 1. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что нерастворимые основания не распадаются на ионы).
Уровень 2. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что нерастворимые основания не распадаются на ионы).
Гидроксид меди (II) + серная кислота >
Взаимодействие кислот с солями
Уровень 1. В пустую ячейку налейте несколько капель серной кислоты. Добавьте 2- 3 капли раствора хлорида бария. Что наблюдаете? Какое вещество выпадает в осадок? (Воспользуйтесь таблицей растворимости). Запишите уравнение реакции в молекулярном и ионном видах. (Обратите внимание на то, что формулы нерастворимых веществ записываются в молекулярном виде).
Вывод. Кислоты взаимодействуют с солями при условии, что образуется…………………. …………………………………………или выделяется ………………………………………….
Уровень 2. Проведите реакцию раствора серной кислоты и раствора хлорида бария. Каков признак реакции? Запишите уравнение реакции между исходными веществами в молекулярном и ионном видах.
Ответьте на вопросы (устно):
1. Каковы общие свойства кислот?
2. Как объяснить тот факт, что кислоты имеют общие свойства?
(Учащиеся выполняют лабораторный опыт, используя инструкционные карты. Часть из них исследует свойства серной кислоты, другая – свойства соляной кислоты (инструкционная карта аналогична). Каждый ученик выбирает уровень задания в соответствии со своими возможностями. В зависимости от подготовленности класса, выводы обсуждаются после каждого опыта или в конце работы в целом. Можно организовать взаимопроверку, проверку с помощью слайдов, листов самопроверки или учащиеся вызываются к доске, им предлагается написать уравнения некоторых реакций (проверку осуществляют ученики совместно с учителем). Учитель оказывает индивидуальную помощь и корректирует деятельность учащихся.)
Надеюсь, что вы нашли ответы на поставленные вопросы.
1. Каковы химические свойства кислот?
а) с индикаторами;
б) с металлами, стоящими в электрохимическом ряду напряжений до водорода, при этом образуется соль и выделяется водород. (Учитель может продемонстрировать слайд и опыт «Взаимодействие магния с соляной кислотой», доказать, что выделившийся газ – водород.)
в) с основными оксидами с образованием соли и воды.
г) с основаниями с образованием соли и воды.
д) с солями более летучих или слабых кислот.
(Обсуждаются результаты опытов взаимодействия соляной кислоты с нитратом серебра (I), хлорида бария с серной кислотой. Если позволяет время, проводится демонстрация опыта «Взаимодействие силиката натрия с соляной кислотой» или «Взаимодействие карбоната кальция с соляной кислотой».)
2. Почему кислоты обладают сходными свойствами?
Внимательно посмотрите на ионные уравнения проделанных вами реакций.
— Под действием каких ионов происходят все рассмотренные реакции? (Под действием ионов водорода. Кислоты обладают сходными свойствами потому, что в растворах кислот при их диссоциации всегда образуются катионы водорода.)
4. «Воспоминания о лете»
В нашей лаборатории расцвёл цветок необычайной красоты – на его лепестках – формулы веществ. Вспомним о лете. Летом вы, наверное, гадали на ромашке «любит – не любит», так и сегодня мы погадаем «взаимодействует – не взаимодействует» данное вещество с серной кислотой? (На лепестках формулы: Аu, Zn, CuO, CO2, NaOH, KCl, Na2SiO3 и слова: фенолфталеин, лакмус). Отрываем ненужные лепестки, остаются: Zn, CuO, NaOH, Na2SiO3, лакмус.
— Расположите лепестки в логической последовательности (лакмус, Zn, CuO, NaOH, Na2SiO3).
VI. Домашнее задание
1) Напишите уравнения реакций взаимодействия данных веществ (Zn, CuO, NaOH, Na2SiO3) с серной кислотой. Все уравнения составьте в молекулярном и ионном виде.
2) Подготовьтесь к презентации и защите проектов по теме «Что мы знаем о кислотах?».
На следующем уроке будет презентация и защита проектов по теме: «Что мы знаем о кислотах?». Надеюсь, что вы основательно подготовили свои проекты и использовали при этом различные источники информации. (Задание учащимся дается заранее и сдаётся не позднее, чем за 3 недели до урока, за это время учитель направляет, помогает и корректирует действия учащихся).
VII. Подведение итогов урока
Подведём итог урока.
— Как вы считаете, достигли ли мы поставленной цели?
В листках учёта заполните графу «самооценка».
Благодарю вас за работу на уроке и хочу привести слова Д.И. Менделеева: «Сами трудясь, вы сделаете многое для себя и для близких, а если в труде успеха не будет, будет неудача, не беда – попробуйте ещё».
На перемене приглашаю вас посетить магазин «Кислоты» и ещё раз убедиться в том, что кислоты кислые на вкус!
Слайды 14 — 15 могут быть использованы в том случае, если позволит время урока.
Слайды 16 — 21 могут быть использованы для самопроверки.
Материал может быть использован на уроках химии в 8 классе – по теме: «Кислоты», в 9 классе – по теме: «Химические свойства кислот с позиции теории электролитической диссоциации».
1. Мартыненко Б.В. Кислоты – основания. — М. Просвещение, 1989.
2. Аликберова Л.Ю. Занимательная химия. — М.:Аст-Пресс, 1999.
3. Савина Л.А. Я познаю мир. Химия. — М.: АСТ, 1998.
4. Шиленков Р.В. Тетрадь для учебной работы по химии. – Первое сентября. Химия. №3, 2005.
5. При создании слайдов была использована информация сети Интернет и электронной энциклопедии Кирилла и Мефодия «Уроки химии. 8- 9 класс».
Для кислот характерны следующие общие свойства:
а) способность взаимодействовать с основаниями с образованием солей;
б) способность изменять цвета индикаторов, в частности, вызывать красную окраску лакмуса;
При диссоциации любой кислоты образуются ионы водорода. Поэтому все свойства, которые являются общими для водных растворов кислот, мы должны объяснить присутствием гидратированных ионов водорода. Это они вызывают красный цвет лакмуса, сообщают кислотам кислый вкус и т.д. С устранением ионов водорода, например, при нейтрализации, исчезают и кислотные свойства. Поэтому теория электролитической диссоциации определяет кислоты как электролиты, диссоциирующие в растворах с образованием ионов водорода.
Одноосновные кислоты диссоциируют в одну ступень:
HNO3H + + N .
Многоосновные кислоты диссоциируют ступенчато:
;
;
При составлении уравнений диссоциации следует помнить, что суммы зарядов в левой и правой частях уравнения должны быть одинаковыми.
Для водных растворов оснований характерны следующие общие свойства:
А) Способность взаимодействовать с кислотами с образованием солей;
б) способность изменять цвет индикаторов иначе, чем их изменяют кислоты (например, они вызывают синюю окраску лакмуса);
в) своеобразный «мыльный» вкус
Поскольку общими для всех растворов оснований является присутствие в них гидроксид-ионов, то ясно, что носителем основных свойств является гидроксид-ион. Поэтому с точки зрения теории электролитической диссоциации основания – это электролиты, диссоциирующие в растворах с отщеплением гидроксид-ионов.
Однокислотные основания диссоциируют в одну ступень:
.
Многокислотные основания диссоциируют ступенчато:
,
.
Существуют гидроксиды, способные вступать во взаимодействие и образовывать соли не только с кислотами, но и с основаниями. К таким гидроксидам принадлежит гидроксид цинка. При взаимодействии его, например, с соляной кислотой получается хлорид цинка
,
А при взаимодействии с гидроксидом натрия при недостатке воды – цинкат натрия:
.
Гидроксиды, обладающие этим свойством, называются амфотерными гидроксидами или амфотерными амфолитами – амфолитами. К таким гидроксидам кроме гидроксида цинка относятся гидроксиды алюминия, хрома(III),железа(III), меди(II), олова(IV) и другие.
Явление амфотерности объясняется тем, что в молекулах амфотерных электролитов прочность связи между металлом и кислородом незначительно отличается от прочности связи между кислородом и водородом. Диссоциация таких молекул, возможна, следовательно, по местам обеих связей. Например, диссоциацию гидроксида цинка можно выразить схемой:
Таким образом, в растворе амфотерного электролита существует сложное равновесие, в котором участвуют продукты диссоциации как по типу кислоты, так и по типу основания.
Таких ионов, которые были бы общими для водных растворов всех солей, нет, поэтому соли и не обладают общими свойствами.
С точки зрения ТЭД соли – это электролиты, которые при растворении в воде диссоциируют на катионы металла и анионы кислотного остатка.
Средние соли диссоциируют в одну ступень
Кислые соли диссоциируют ступенчато: сначала отщепляются все катионы металла, а затем – по одному – ионы водорода.
Основные соли диссоциируют ступенчато: сначала отщепляются все ионы кислотных остатков, а затем – по одному – гидроксид-ионы.
,
,
.
Таким образом, при составлении уравнений диссоциации следует помнить: катионы водорода и гидроксид-ионы диссоциируют ступенчато, а катионы металлов и анионы кислотных остатков – сразу, в одну ступень.
| | | следующая страница ==> | |
| Сильные электролиты. Активность электролитов | | | Реакции ионного обмена |
Дата добавления: 2014-05-03 ; просмотров: 2 .
Свойства кислот оснований и солей с точки зрения ТЭД (теории электролитической диссоциации). Амфотерность.
Основания. Название «основание» первоначально было отнесено к веществам, которые в реакциях с кислотами образуют соли. К основаниям принадлежат гидроксиды многих металлов.
Примеры: NaOH — гидроксид натрия (едкий натр), KOH — гидроксид калия (едкое кали), Ca(OH)2 — гидроксид кальция (гашёная известь).
Основания, которые хорошо растворяются в воде, называются щелочами, К ним относятся гидроксиды щелочных и щелочно-земельных металлов. С точки зрения теории электролитической диссоциации основания-это вещества, диссоциирующие в водном растворе с образованием анионов одного вида — гидроксид — ионов ОН-.
В общем виде уравнение электролитической диссоциации основания имеет вид:
Основание -> Катион основания + Гидроксид — ион
NaOH 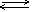
Ba(OH)2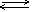
NH3·H2O 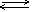
Кислоты. Кислоты исторически получили своё название из-за кислого вкуса водных растворов тактх веществ, как хлороводород или уксусная кислота. С точки зрения теории электролитической диссоциации кислоты-это вещества, диссоциирующие в водном растворе с образованием катионов одного вида — катионов водорода Н+.
В общем виде уравнение электролитической диссоциации кислоты имеет вид:
Кислота -> Катион водорода + Анион кислотного остатка
H2SO4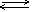
CH3COOH 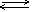
Соли. С точки зрения теории электролитической реакции соли — это вещества, которые в водном растворе диссоциируют с образованием катионов основания и анионов кислотного остатка.
В общем виде уравнение электролитической диссоциации солей имеет следующий вид:
Соль -> Катион основания + Анион кислотного остатка
BaCl2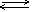
K2CO3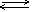
Амфотерность — способность некоторых химических веществ и соединений проявлять в зависимости от условий как кислотные, так и основные свойства.
Амфотерность как химическое свойство вещества может проявляться по-разному:
1. В рамках теории электролитической диссоциации это способность вещества к электролитической диссоциации как по механизму кислот (с отщеплением ионов гидроксония, H + ), так и по механизму оснований (отщепление гидроксид-ионов, OH – ). Электролиты, которые в растворе ионизируются одновременно по кислотному и основному типам называются амфолитами. Если обозначить амфотерный электролит формулой XOH, то его диссоциацию можно описать схемой:
H + + XO − ⇄ XOH ⇄ X + + OH −
Например, кислотно-основные свойства азотистой кислоты определяются равновесными процессами диссоциации с образованием нитрит-аниона и нитрозильного катиона:
HNO2 ⇄ NO + + OH − Kb ≈ 10 − 7
Идеальным амфолитом будет вода:
Также к числу идеальных амфолитов относят гидроксид галлия Ga(OH)3, вторые и третьи константы диссоциации которого по кислотному и основному типам практически одинаковы.
2. В рамках протолитической теории Брёнстеда-Лоури проявление амфотерности рассматривается как способность протолита выступать донором и акцептором протона. Например, для воды амфотерность проявляется как автопротоли:
Амфолитами также будут вещества, имеющие в своём составе функциональные группы, способные быть донорами и акцепторами протонов. Например, к амфотерным органическим электролитам относятся белки, пептиды и аминокислоты. Так аминокислоты имеют в своём составе, по крайней мере, карбоксильную группу –COOH и аминогруппу –NH2. В растворе эти группы подвергаются частичной ионизации:
H2N — CH(R) — COOH + H2O ⇄ [ H3N — CH(R) — COOH ] + + OH −
Таким образом, молекула аминокислоты находится в двух равновесных формах, заряженной (цвиттер-ион) и незаряженной. В этих комбинациях R–COOH и R–NH3 + являются потенциальными кислотами (донорами протонов, катионов), а R–COO– и R–NH2 – сопряженными потенциальными основаниями (акцепторами протонов, катионов).
3. Амфотерность может проявляться как способность вещества к взаимодействию как с кислотами, так и с основаниями. Это характерно для оксидов, гидроксидов и комплексных соединений некоторых p-элементов и большинства d-элементов в промежуточных степенях окисления. Амфотерность в той или иной степени является общим свойством гидроксидов. Например, для соединений хрома (III) известны реакции:
Не соответствуют действительности традиционные представления о проявлении амфотерности гидроксидов как диссоциации по кислотному и основному типам. В общем виде амфотерное поведение нерастворимых гидроксидов хрома (III), алюминия, цинка может описано как реакции ионного обмена ионов среды с лигандами H2O и OH – . Например, для Al(OH3) ионные равновесия могут быть записаны следующим образом:
4. В ряде случаев важным косвенным признаком амфотерности является способность элемента образовывать два ряда солей, катионного и анионного типа. Например, для цинка: ZnCl2, [Zn(H2O)4]SO4 (катионные) и Na2ZnO2, Na2(Zn(OH)4) (анионные).
Окислительно-восстановительные реакции. Понятие «степень окисления». Типы окислительно-восстановительных реакций (привести примеры).
Окислительно-восстановительные реакции, также редокс— это встречно-параллельные химические реакции, протекающие с изменением степеней окисления и не более 2-х атомов, входящих в состав реагирующих веществ (или ионов веществ), реализующимся путём перераспределения электронов между атомом-окислителем (акцептором) и атомом-восстановителем (донором).
В процессе окислительно-восстановительной реакции восстановитель отдаёт электроны, то есть окисляется; окислитель присоединяет электроны, то есть восстанавливается. Причём любая окислительно-восстановительная реакция представляет собой единство двух противоположных превращений — окисления и восстановления, происходящих одновременно и без отрыва одного от другого.[2]
Окисление — процесс отдачи электронов с увеличением степени окисления.
При окислении вещества в результате отдачи электронов увеличивается его степени окисления. Атомы окисляемого вещества называются донорами электронов, а атомы окислителя — акцепторами электронов.
В некоторых случаях при окислении молекула исходного вещества может стать нестабильной и распасться на более стабильные и более мелкие составные части (см. Свободные радикалы). При этом некоторые из атомов получившихся молекул имеют более высокую степень окисления, чем те же атомы в исходной молекуле.
Окислитель, принимая электроны, приобретает восстановительные свойства, превращаясь в сопряжённый восстановитель:
окислитель +e− ↔ сопряжённый восстановитель.
Восстановление — процесс присоединения электронов атомом вещества, при этом его степень окисления понижается.
При восстановлении атомы или ионы присоединяют электроны. При этом происходит понижение степени окисления элемента. Примеры: восстановление оксидов металлов до свободных металлов при помощи водорода, углерода, других веществ; восстановление органических кислот в альдегиды и спирты; гидрогенизация жиров и др.
Восстановитель, отдавая электроны, приобретает окислительные свойства, превращаясь в сопряжённый окислитель:
восстановитель -e− ↔ сопряжённый окислитель.
Несвязанный, свободный электрон является сильнейшим восстановителем.
Окислитель и его восстановленная форма, либо восстановитель и его окисленная форма составляет сопряжённую окислительно-восстановительную пару, а их взаимопревращения являются окислительно-восстановительными полуреакциями.
В любой окислительно-восстановительной реакции принимают участие две сопряжённые окислительно-восстановительные пары, между которыми имеет место конкуренция за электроны, в результате чего протекают две полуреакции: одна связана с присоединением электронов, то есть восстановлением, другая — с отдачей электронов, то есть окислением.
Степень окисления (окислительное число, формальный заряд) — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов: она не является истинным зарядом атома в молекуле.
Представления о степени окисления элементов положены в основу и используются при классификации химических веществ, описании их свойств, составлении формул соединений и их международных названий (номенклатуры). Но особенно широко оно применяется при изучении окислительно-восстановительных реакций.
Понятие степень окисления часто используют в неорганической химии вместо понятия валентность.
Последнее изменение этой страницы: 2017-02-05; Нарушение авторского права страницы
2.Свойства кислот, оснований и солей с точки зрения теории электролитической диссоциации.
способность взаимодействовать с основаниями с образованием солей
способность взаимодействовать с некоторыми металлами с выделением водорода
способность изменять цвет индикатора (красная окраска лакмуса)
Согласно теории электролитической диссоциации кислоты – это электролиты, диссоциирующие в растворах с образованием ионов (катионов) водорода и анионов кислотного остатка.
Именно ионы водорода вызывают красный цвет лакмуса и сообщают кислотам кислый вкус.
способность взаимодействовать с кислотами с образованием солей
способность изменять цвет индикатора иначе, чем их изменяют кислоты (синяя окраска лакмуса)
своеобразный «мыльный вкус»
Согласно теории электролитической диссоциации основания – это электролиты, диссоциирующие в растворах с образованием аниона гидроксила и катиона металла.
Носителем щелочных свойств является анион гидроксила.
Соли при электролитической диссоциации распадаются на катион металла и анион кислотного остатка. Так как таких ионов, которые были бы общими для водных растворов всех солей нет, поэтому соли и не обладают общими свойствами.
3.Реакции нейтрализации
А) при нейтрализации любой сильной кислоты любым сильным основанием на каждую грамм-молекулу образующейся воды выделяется около 13,8 ккал теплоты.
Это говорит о том, что подобные реакции сводятся к одному процессу. Рассмотрим одну из этих реакций. Перепишем уравнение первой реакции, записывая сильные электролиты в ионной форме, а слабые — в молекулярной, поскольку они находятся в растворе преимущественно в виде молекул.

В ходе реакции ионы Na + и 
Таким образом, реакции нейтрализации любой сильной кислоты любым сильным основанием сводятся к одному и тому же процессу – к образованию молекул воды из ионов водорода и гидроксила.
Реакция образования воды из ионов обратима
Но так как вода слабый электролит и диссоциирует в ничтожно малой степени, то равновесие в этой реакции сильно смещено в сторону образования молекул. Поэтому практически реакция нейтрализации сильной кислоты сильным основанием протекает до конца.
В дальнейшем мы будем широко пользоваться ионно-молекулярной формой записи уравнений реакций с участием электролитов.
При составлении ионно-молекулярных уравнений надо знать, какие соли растворимы в воде и какие практически нерастворимы.
Общие данные о растворимости важнейших солей обычно приведены в таблицах во всех учебниках химии.
Б) нейтрализация слабой кислоты сильным основанием
Здесь сильные электролиты – NaOH и соль, а слабые – кислота и вода:
Так как только ионы натрия не претерпевают изменений, то ионно-молекулярное уравнение имеет вид:
В) нейтрализация сильной кислоты слабым основанием
Здесь в виде ионов мы должны записать кислоту и образующуюся соль, а в виде молекул – гидроксид аммония и воду:
Не изменяются только ионы 
Г) нейтрализация слабой кислоты слабым основанием
В этой реакции все вещества, кроме образующейся соли, слабые электролиты. Поэтому ионно-молекулярная форма имеет вид:
Реакции нейтрализации сильных кислот сильными основаниями протекают практически до конца. Реакции нейтрализации, в которых хотя бы одно из исходных веществ – слабый электролит, и при которых молекулы малодиссоциирующих веществ имеются не только в правой, но и в левой части ионно-молекулярного уравнения, протекают не до конца. Они доходят до состояния равновесия, при котором соль существует с кислотой и основанием, из которых она образована. Поэтому уравнения подобных реакций правильнее записывать как обратимые реакции.
При растворении твердого тела в воде растворение прекращается, когда получается насыщенный раствор, т.е. когда между растворяемым веществом и находящимися в растворе молекулами того же вещества устанавливается равновесие.
При растворении электролита, например соли, в раствор переходят не молекулы, а ионы; следовательно и равновесие в насыщенном растворе устанавливается между твердой солью и перешедшими в раствор ионами.
Например, в насыщенном растворе сульфата кальция устанавливается равновесие
твердая соль ионы в растворе
Если обозначим концентрацию катионов кальция 

ПРCaSO4=[Ca 2+ ][SO
Урок химии на тему «Химические свойства кислот с точки зрения теории электролитической диссоциации» (8 класс)
за привлеченного слушателя на курсы профессиональной переподготовки
Тема урока: «Химические свойства кислот с точки зрения теории электролитической диссоциации».
Цель урока: расширить и углубить представления учащихся о химических свойствах кислот.
1. Образовательная: изучить химические свойства кислот с позиции теории электролитической диссоциации.
2. Развивающие (формирование и развитие образовательных компетенций):
а) учебно-познавательных: развитие навыков самостоятельной познавательной деятельности; умения ставить познавательную задачу (целеполагание), умения добывать знания, выделять главное, обобщать, делать выводы, проводить самопроверку и самооценку;
б) коммуникативных: навыков работы в паре, взаимодействия с другими людьми, умения ответить на поставленный вопрос;
в) информационных: проводить материальное и знаковое моделирование, выделять существенные признаки химических реакций, извлекать необходимую информацию из проводимого эксперимента; оформлять и представлять результаты своей работы.
3. Воспитательные: воспитывать сознательное отношение к учебному труду, чувство ответственности, развивать интерес к знаниям.
Планируемые результаты обучения
В результате изучения данного материала учащиеся должны:
а) определение понятий – электролиты, неэлектролиты, электролитическая диссоциация, кислоты;
б) химические свойства кислот с позиции теории электролитической диссоциации.
Уметь (владеть способами познавательной деятельности):
а) составлять уравнения электролитической диссоциации кислот, оснований, солей;
б) уравнения реакций ионного обмена;
в) проводить реакции ионного обмена, подтверждающие химические свойства кислот, соблюдая правила безопасного обращения с реактивами и выявлять признаки наблюдаемых химических реакций;
г) пользоваться таблицей растворимости.
Подготовка к уроку
Оборудование и реактивы:
Презентация по теме: «Кислоты», проектор.
Оборудование и реактивы: пробирки, магний, медь, С u О, Сu(OH) 2 .
Склянки c растворами веществ: НСl, Н 2 SO 4 ; метилоранж, лакмус, фенолфталеин; АgNO 3 ; ВаCl 2 .
На столе учителя: магний, соляная кислота, порошок мела в стаканчике, клей канцелярский, спички, металлический штатив, пробирки, палочка, стаканчик.
На столах учащихся:
Оборудование и реактивы к лабораторному опыту.
Инструктивные карты, листы самопроверки к лабораторному опыту.
Лист учёта знаний учащихся по теме: «Электролитическая диссоциация».
Дорогие ребята, уважаемые гости, здравствуйте! Вы любите фрукты (слайд №2)?
— А какой вкус у фруктов?
— Чем объясняется кислый вкус фруктов и других продуктов?
Овощи и фрукты содержат органические кислоты: лимонную, яблочную, щавелевую, , аскорбиновую и др. Они играют определённую роль в пищеварении, а, следовательно, в нашей жизни. Мы же сегодня поговорим о неорганических кислотах, которые очень важны для человека, так как он использует их в своей практической деятельности, несмотря на то, что с большинством кислот надо обращаться крайне осторожно.
Сегодня мы поговорим о кислотах в узком аспекте, потому что тема нашего урока: «Химические свойства кислот с точки зрения теории электролитической диссоциации» (слайд №3). Великий Шекспир когда-то сказал: « От кислых яблок сразу скисну» , я же пожелаю вам никогда не скисать, а учиться преодолевать любые трудности.
II. (1). Целеполагание
Определим цель и задачи урока.
Цель урока: расширить и углубить наши представления о кислотах, ведь они так важны для человека. Сформулировать задачи урока, я надеюсь, поможете мне вы, используя лист учёта знаний по теме. Прошу вас выделить в каждом разделе пункты, которые, на ваш взгляд, соответствуют теме нашего урока.
Лист учёта знаний учащегося по теме:
«Электролитическая диссоциация» (заполняет ученик)
электролиты, неэлектролиты, электролитическая диссоциация; кислоты, основания .
Механизм электролитической диссоциации веществ с ионной связью на примере хлорида натрия
Химические свойства кислот, оснований, солей с точки зрения ТЭД и ОВР
Составлять уравнения ЭД кислот, оснований и солей
Пользоваться таблицей растворимости
Составлять уравнения реакций ионного обмена
Проводить реакции ионного обмена, соблюдая правила безопасного обращения с реактивами
Решать экспериментальные задачи, используя знания химических свойств веществ.
Умения и навыки
С помощью учителя
Планировать свою учебную деятельность
Активно участвовать в организации работы в паре
Осуществлять самоконтроль и давать самооценку своей деятельности
Уметь выделять главное, делать выводы
Слушать объяснение учителя
Работать с дополнительной литературой
Отвечать на вопросы в соответствии с их характером
Составлять и использовать таблицы
Вести записи в тетради в соответствии с требованиями
Прочтём ещё раз тему урока и расшифруем каждое слово в этом непростом для «нехимического» взгляда предложении.
— Что такое диссоциация?
— Что такое электролиты?
— На какие ионы распадаются кислоты в растворах?
— Какое определение даёт эта теория кислотам? Какие признаки классификации кислот вам известны?
Работа с тренажёром ОМ S модуля.
— Что значит «описать химические свойства кислот»?
— Понятны ли вам тема, цель и задачи урока?
III. Подготовка к восприятию нового материала
Химическая разминка. Даны вещества: H 2 SO 4 ; CuO ; железо, Na 2 O ; лакмус; Н 3 PO 4 ; кальций; HClO 4 ; фенолфталеин; HCl ; FeO ; Fe ( OH ) 3 ; метилоранж; хром; NaOH ; Mg (ОН) 2. Распределите их на логические группы. Слайд № 5,6.
— Как назвать их одним словом (психологи называют это «синтезом»)? (Кислоты, индикаторы, металлы, основные оксиды, основания, соли.)
— Какова логическая взаимосвязь указанных понятий с кислотами? (Кислоты взаимодействуют с ними, а именно: с индикаторами, металлами, основными оксидами, основаниями, солями.)
Просмотр ОМ S модуля «Химические свойства кислот»
Сейчас нам предстоит проделать эти реакции и объяснить их с новой точки зрения – с позиции теории электролитической диссоциации.
(На экране появляется слайд №9.)
Тема: «Химические свойства кислот с точки зрения теории электролитической диссоциации».
Работа с инструктивной картой
Прочитайте тему лабораторного опыта, уясните цель.
Расскажу вам о Юстусе Либихе, знаменитом учёном-химике ХIХ века. «Вот как описывает Карл Фогт – химик, работавший вместе с Либихом один случай. Входит Либих, у него в руках склянка с притёртой пробкой. «Ну-ка, обнажите руку», — говорит он Фогту и влажной пробкой прикасается к руке. «Не правда, ли, жжёт? – невозмутимо спрашивает Либих. – Я только что добыл безводную муравьиную кислоту». Как вы думаете, правильно ли обращался Либих с кислотами? Конечно, неправильно; после этой пробы у Фогта долго болела рука, и остался белый шрам на руке.
— А вы знаете, как обращаться с кислотами и другими реактивами? (Ученики проговаривают правила обращения с реактивами.)
Будьте предельно осторожны, берегите глаза! Кому понятны техника безопасности, название опыта, цель и ход работы поднимите руки.
При описании наблюдений следите за речью, чтобы не попасть в копилку «ляпов». Например. «Болтаю, болтаю — сплошная муть». «Соль состоит из атомов кислорода и кислотных останков». «Кислота имеет кислый вкус, поэтому она имеет кислотный остаток». «Химическая реакция и пламя спиртовки находятся друг с другом в довольно близких отношениях».
В качестве напутствия я хотела бы привести слова Козьмы Пруткова: «Бросая в воду камешки, гляди на круги, ими образуемые, иначе такое бросание обратится пустою забавою…». Слайд№10
Проводя опыт, сделайте выводы и найдите ответ на вопросы, изображенные на экране (слайд №5).
— Как объясняет ТЭД химические свойства кислот?
— Почему у кислот есть общие свойства? Это самый главный вопрос сегодняшнего урока.
Тема: «Химические свойства кислот с точки зрения теории электролитической диссоциации».
проделать реакции, характерные для кислот на примере серной кислоты,
сделать вывод о химических свойствах кислот,
закрепить навыки безопасного обращения с реактивами.
Опыт 1. Действие кислот на индикаторы
Раствор серной кислоты налейте в три пробирки. В первую добавьте раствор фиолетового лакмуса, во вторую — раствор метилоранжа, в третью – раствор фенолфталеина. Что вы наблюдаете?
Уровень 1. Вставьте пропущенные слова в предложении: «Кислоты изменяют окраску индикаторов: фиолетового лакмуса – на ………………………………………, метилоранжа – ……………………………. …., фенолфталеин остаётся—————————.
Уровень 2. Напишите уравнение диссоциации серной кислоты.
Опыт 2. Взаимодействие кислот с металлами
В пробирки, где находится магний и медь добавьте раствор серной кислоты. Что вы наблюдаете? Сравните результаты.
Задания. Уровень 1. Запишите уравнения практически осуществимых реакций в молекулярном и ионном видах. М g + …. H 2 SO 4 =… + Н 2
Вывод. Кислоты взаимодействуют с металлами, стоящими в электрохимическом ряду напряжений металлов до ————
Уровень 2. Запишите уравнения практически осуществимых реакций в молекулярном и ионном видах:
а) магний + серная кислота =……………………
б) медь + серная кислота =
Опыт 3. Взаимодействие кислот с основными оксидами
Опыт взаимодействия оксида меди (II) с серной кислотой будет демонстрировать учитель на видео, вам нужно предположить: растворится ли оксид меди (II) в серной кислоте?
Задания. Уровень 1. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что формулы оксидов пишутся в молекулярном виде).
Вывод. Кислоты взаимодействуют с …………………….…………. ………..…, при этом получаются ………………………. … и …….….….………..……………………
Уровень 2. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что оксиды — неэлектролиты).
Оксид меди (II) + серная кислота =
Опыт 4. Взаимодействие кислот с основаниями
Получите гидроксид меди (II). Для этого добавьте к раствору сульфата меди( II ) раствор гидроксида натрия. К образовавшемуся осадку добавьте серную кислоту, перемешайте встряхиванием. Что наблюдаете?
Задания. Уровень 1. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что нерастворимые основания не распадаются на ионы).
Вывод. Кислоты взаимодействуют с ………………… при этом получаются ……………………………………………….. и ————
Уровень 2. Запишите уравнение реакции в молекулярном и ионном видах. (Не забудьте, что нерастворимые основания не распадаются на ионы).
Гидроксид меди (II) + серная кислота =
Опыт 5. Взаимодействие кислот с солями
Уровень 1. В пустую пробирку налейте несколько капель серной кислоты. Добавьте 2- 3 капли раствора хлорида бария. Что наблюдаете? Какое вещество выпадает в осадок? (Воспользуйтесь таблицей растворимости). Запишите уравнение реакции в молекулярном и ионном видах. (Обратите внимание на то, что формулы нерастворимых веществ записываются в молекулярном виде).
Вывод. Кислоты взаимодействуют с солями при условии, что образуется…………………. …………………………………………или выделяется ———————-
Уровень 2. Проведите реакцию раствора серной кислоты и раствора хлорида бария. Каков признак реакции? Запишите уравнение реакции между исходными веществами в молекулярном и ионном видах.
Ответьте на вопросы (устно):
1. Каковы общие свойства кислот?
2. Как объяснить тот факт, что кислоты имеют общие свойства?
Надеюсь, что вы нашли ответы на поставленные вопросы.
1. Каковы химические свойства кислот?
а) с индикаторами;
б) с металлами, стоящими в электрохимическом ряду напряжений до водорода, при этом образуется соль и выделяется водород. (Учитель может продемонстрировать слайд и опыт «Взаимодействие магния с соляной кислотой», доказать, что выделившийся газ – водород.) Работа с учебником.
в) с основными оксидами с образованием соли и воды.
г) с основаниями с образованием соли и воды.
д) с солями более летучих или слабых кислот.
2. Почему кислоты обладают сходными свойствами?
Внимательно посмотрите на ионные уравнения проделанных вами реакций.
— Под действием каких ионов происходят все рассмотренные реакции? (Под действием ионов водорода. Кислоты обладают сходными свойствами потому, что в растворах кислот при их диссоциации всегда образуются катионы водорода.)
Выполнить упражнение №6 на стр. 142 в рабочей тетради авт. О.С. Габриелян.
VI. Домашнее задание
1) Выполнить задания в рабочей тетради стр. 142-143 №7,8.
2) Составьте сводную таблицу химических свойств с примерами уравнений реакций.
VII. Подведение итогов урока
Подведём итог урока.
— Как вы считаете, достигли ли мы поставленной цели?
В листках учёта заполните графу «самооценка».
Благодарю вас за работу на уроке и хочу привести слова Д.И. Менделеева:
«Сами трудясь, вы сделаете многое для себя и для близких, а если в труде успеха не будет, будет неудача, не беда – попробуйте ещё».
- http://refac.ru/svojstva-kislot-osnovanij-i-solej-s-tochki-zreniya-teorii-elektroliticheskoj-dissociacii/
- http://infopedia.su/17x4d38.html
- http://studfiles.net/preview/7015876/page:5/
- http://infourok.ru/urok-himii-na-temu-himicheskie-svoystva-kislot-s-tochki-zreniya-teorii-elektroliticheskoy-dissociacii-klass-2381992.html

















