Идеальная жидкость, т.е. жидкость, движущаяся без трения, является абстрактным понятием. Всем реальным жидкостям и газам в большей или меньшей степени присуща вязкость или внутреннее трение. Вязкость (внутреннее трение) наряду с диффузией и теплопроводностью относится к явлениям переноса и наблюдается только в движущихся жидкостях и газах. Вязкость проявляется в том, что возникающее в жидкости или газе движение после прекращения действия причин, его вызвавших, постепенно прекращается.
Вязкость (внутреннее трение) — одно из явлений переноса, свойство текучих тел (жидкостей и газов) оказывать сопротивление перемещению одной их части относительно другой. В результате происходит рассеяние в виде тепла энергии, затрачиваемой на это перемещение.
Механизм внутреннего трения в жидкостях и газах заключается в том, что хаотически движущиеся молекулы переносят импульс из одного слоя в другой, что приводит к выравниванию скоростей — это описывается введением силы трения. Вязкость твёрдых тел обладает рядом специфических особенностей и рассматривается обычно отдельно.
Молекулярно-кинетическая теория объясняет вязкость движением и взаимодействием молекул.
В жидкостях, где расстояния между молекулами много меньше, чем в газах, вязкость обусловлена в первую очередь межмолекулярным взаимодействием, ограничивающим подвижность молекул. В жидкости молекула может проникнуть в соседний слой лишь при образовании в нём полости, достаточной для перескакивания туда молекулы. На образование полости (на «рыхление» жидкости) расходуется так называемая энергия активации вязкого течения. Энергия активации уменьшается с ростом температуры и понижением давления. В этом состоит одна из причин резкого снижения вязкости жидкостей с повышением температуры и роста её при высоких давлениях. При повышении давления до нескольких тыс. атмосфер вязкость увеличивается в десятки и сотни раз. Строгая теория вязкости жидкостей, в связи с недостаточной разработанностью теории жидкого состояния, ещё не создана.
Вязкость отдельных классов жидкостей и растворов зависит от температуры, давления и химического состава.
Вязкость жидкостей зависит от химической структуры их молекул. В рядах сходных химических соединений (насыщенные углеводороды, спирты, органические кислоты и т.д.) Вязкость изменяется закономерно — возрастает с возрастанием молекулярной массы. Высокая вязкость смазочных масел объясняется наличием в их молекулах циклов. Две жидкости различной вязкости, которые не реагируют друг с другом при смешивании, обладают в смеси средним значением вязкости. Если же при смешивании образуется химическое соединение, то вязкость смеси может быть в десятки раз больше, чем вязкость исходных жидкостей.
Возникновение в жидкостях (дисперсных системах или растворах полимеров) пространственных структур, образуемых сцеплением частиц или макромолекул, вызывает резкое повышение вязкости. При течении «структурированной» жидкости работа внешней силы затрачивается не только на преодоление вязкости, но и на разрушение структуры.
В газах расстояния между молекулами существенно больше радиуса действия молекулярных сил, поэтому Вязкость газов определяется главным образом молекулярным движением. Между движущимися относительно друг друга слоями газа происходит постоянный обмен молекулами, обусловленный их непрерывным хаотическим (тепловым) движением. Переход молекул из одного слоя в соседний, движущийся с иной скоростью, приводит к переносу от слоя к слою определённого импульса. В результате медленные слои ускоряются, а более быстрые замедляются. Работа внешней силы F, уравновешивающей вязкое сопротивление и поддерживающей установившееся течение, полностью переходит в теплоту. Вязкость газа не зависит от его плотности (давления), так как при сжатии газа общее количество молекул, переходящих из слоя в слой, увеличивается, но зато каждая молекула менее глубоко проникает в соседний слой и переносит меньший импульс (закон Максвелла).
Вязкость — важная физико-химическая характеристика веществ. Значение вязкости приходится учитывать при перекачивании жидкостей и газов по трубам (нефтепроводы, газопроводы). Вязкость расплавленных шлаков весьма существенна в доменном и мартеновском процессах. Вязкость расплавленного стекла определяет процесс его выработки. По вязкости во многих случаях судят о готовности или качестве продуктов или полупродуктов производства, поскольку вязкость тесно связана со структурой вещества и отражает те физико-химические изменения материала, которые происходят во время технологических процессов. Вязкость масел имеет большое значение для расчёта смазки машин и механизмов и т.д.
Прибор для измерения вязкости называется вискозиметром.
Не нашли то, что искали? Воспользуйтесь поиском:
Явление — внутреннее трение
Явление внутреннего трения ( вязкости) связано с возникновением сил трения между двумя слоями газа или жидкости, перемещающимися параллельно друг другу с различными по величине скоростями. Причиной внутреннего трения является перенос молекулами количества движения из одного слоя газа в другой. [1]
Явление внутреннего трения в газах и жидкостях состоит в возникновении сил трения между двумя смежными слоями среды, движущимися параллельно относительно друг друга. [2]
Явление внутреннего трения описывается следующим образом. [3]
Явление внутреннего трения ( вязкости) связано с возникновени-нием сил трения между слоями газа или жидкости, перемещающимися параллельно друг другу с различными по величине скоростями. Со стороны слоя, движущегося быстрее, на более медленно движущийся слой действует ускоряющая сила. Наоборот, медленно перемещающийся слой тормозит более быстро движущиеся слои газа. Силы трения, которые при этом возникают, направлены по касательной к поверхности соприкосновения слоев. С точки зрения кинетической теории газов, причиной внутреннего трения является наложение упорядоченного движения слоев газа с различными скоростями v и хаотического теплового движения молекул, интенсивность которого зависит от температуры. Благодаря тепловому движению молекулы переходят из слоя В ( рис. 11.12), движущегося со скоростью v2, в слой А движущийся со скоростью YI. [4]
Явление внутреннего трения ( вязкости) наблюдается в телах при всех агрегатных состояниях, но большое практическое значение это явление имеет для жидкостей и газов. [5]
Явление внутреннего трения заключается во взаимодействии слоев текущего газа. [6]
Для явления внутреннего трения справедлив закон И. [7]
Благодаря явлению внутреннего трения на слой воздуха, примыкающий к пластинке ( адсорбированный пластинкой), действует со стороны движущихся слоев сила трения. [8]
Под явлением внутреннего трения , или вязкости, подразумевается возникновение сил трения между слоями исследуемого вещества, движущимися друг относительно друга с разными по величине скоростями. [9]
В явлении внутреннего трения молекулы , переходя из одного слоя движущегося газа в другой, не сразу приобретают в среднем скорость этого слоя. [10]
На явлении внутреннего трения газов , при котором движение одного элементарного слоя газа передается другому, и явлении внешнего трения, благодаря которому движущаяся твердая стенка увлекает непосредственно прилегающий к ней слой газа, основано устройство так называемого молекулярного насоса. [12]
При рассмотрении явления внутреннего трения у золей было обращено внимание на структурную вязкость, которая отвечает, как показали работы Шведова упругости, характерного для твердого тела. [14]
С точки зрения кинетической теории явление внутреннего трения заключается в переносе молекулами количества движения от слоев, движущихся с большей-скоростью, к слоям, движущимся с меньшей скоростью. Это приращение количества движения и определяет силу, действующую между слоями. [15]
Вязкость газов по молекулярно-кинетической теории (мкт)
Рассмотрим два слоя газа, движущиеся с разными скоростями (рис. 1). Если температура газа всюду одинакова, то средняя скорость движения молекул также одинакова, обозначим ее И. По МКТ она зависит от массы молекул и температуры газа:

Где Т — Масса молекулы, Т — температура газа, K – постоянная Больцмана.
Так как молекула может двигаться по шести независимым направлениям в пространстве, то площадку S За единицу времени пересечет 

Так как V(Z) есть непрерывная функция координаты Z, можно считать, что V2=V(Z+λ,), а V1=V(Z-λ). Если размеры сосуда, в котором находится газ, много больше средней длины свободного пробега, то, полагая λ малым изменением аргумента функции V(Z), можно записать следующие приближенные равенства:

Если подставить эти выражения в формулу (7) и учесть, что по второму закону Ньютона изменение импульса равно импульсу силы (DР=FDT), то из определения понятия коэффициента внутреннего трения с учетом того, что произведение массы молекулы на их концентрацию есть плотность газа (ρ=Пт), для вязкости получается выражение:

Это выражение можно преобразовать. По молекулярно-кинетической теории средняя длина свободного пробега молекул

Где D — эффективный диаметр молекулы.
Подставив (8) и (9) в выражение для вязкости, получим

Видим, что вязкость зависит от массы молекулы Т, ее диаметра D И от температуры T, а от давления и плотности газа не зависит.
Вязкости некоторых веществ (в МкПа·с)
Внутреннее трение с точки зрения мкт
Молекулярная физика и термодинамика – это по существу две разные по своим подходам, но тесно связанные науки, занимающиеся одним и тем же – изучением макроскопических свойств физических систем, но совершенно разными методами.
В основе молекулярной физики или молекулярно-кинетической теории лежат определенные представления о строении вещества. Для установления законов поведения макроскопических систем, состоящих из огромного числа частиц, в молекулярной физике используются различные модели вещества, например, модели идеального газа.
Молекулярная физика является статистической теорией, т. е. теорией, которая рассматривает поведение систем, состоящих из огромного числа частиц (атомов, молекул), на основе вероятностных моделей. Она стремится на основе статистического подхода установить связь между экспериментально измеренными макроскопическими величинами (давление, объем, температура и т.д.) и микроскопическими характеристиками частиц, входящих в состав системы (масса, импульс, энергия и т.д.).
В отличие от молекулярно-кинетической теории, термодинамика при изучении свойств макроскопических систем не опирается ни на какие представления о молекулярной структуре вещества. Термодинамика является наукой феноменологической . Она делает выводы о свойствах вещества на основе законов, установленных на опыте, таких, как закон сохранения энергии. Термодинамика оперирует только с макроскопическими величинами (давление, температура, объем и т.п.), которые вводятся на основе физического эксперимента.
Оба подхода – термодинамический и статистический – не противоречат, а дополняют друг друга. Только совместное использование термодинамики и молекулярно-кинетической теории может дать наиболее полное представление о свойствах систем, состоящих из большого числа частиц.
Молекулярно-кинетическая теория
3.1. Основные положения МКТ
Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химических веществ.
В основе молекулярно-кинетической теории лежат три основных положения:
Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов («элементарных молекул»). Молекулы химического вещества могут быть простыми и сложными, т.е. состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы.
Атомы и молекулы находятся в непрерывном хаотическом движении.
Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
 | |||||||||||||||||||||||
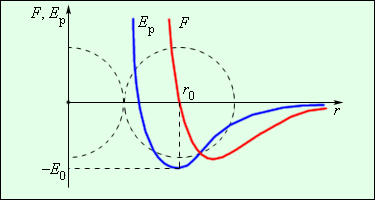
| Рисунок 3.1.1. Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение . Это тепловое движение мельчайших микроскопических частиц, взвешенных в жидкости или газе. Оно было открыто английским ботаником Р. Броуном в 1827 г. Броуновские частицы движутся под влиянием беспорядочных ударов молекул. Из-за хаотического теплового движения молекул эти удары никогда не уравновешивают друг друга. В результате скорость броуновской частицы беспорядочно меняется по модулю и направлению, а ее траектория представляет собой сложную зигзагообразную кривую (рис. 3.1.1). Теория броуновского движения была создана А. Эйнштейном в 1905 г. Экспериментально теория Эйнштейна была подтверждена в опытах французского физика Ж. Перрена, проведенных в 1908–1911 гг. Главный вывод теории А. Эйнштейна состоит в том, что квадрат смещения броуновской частицы от начального положения, усредненный по многим броуновским частицам, пропорционален времени наблюдения . Это соотношение выражает так называемый диффузионный закон . Как следует из теории коэффициент пропорциональности монотонно возрастает с увеличением температуры. Постоянное хаотичное движение молекул вещества проявляется также в другом легко наблюдаемом явлении – диффузии . Диффузией называется явление проникновения двух или нескольких соприкасающихся веществ друг в друга. Наиболее быстро процесс протекает в газе, если он неоднороден по составу. Диффузия приводит к образованию однородной смеси независимо от плотности компонентов. Так, если в двух частях сосуда, разделенных перегородкой, находятся кислород O2 и водород H2, то после удаления перегородки начинается процесс взаимопроникновения газов друг в друга, приводящий к образованию взрывоопасной смеси – гремучего газа. Этот процесс идет и в том случае, когда легкий газ (водород) находится в верхней половине сосуда, а более тяжелый (вислород) – в нижней. Значительно медленнее протекают подобные процессы в жидкостях. Взаимопроникновение двух разнородных жидкостей друг в друга, растворение твердых веществ в жидкостях (например, сахара в воде) и образование однородных растворов – примеры диффузионных процессов в жидкостях. В реальных условиях диффузия в жидкостях и газах маскируется более быстрыми процессами перемешивания, например, из-за возникновения конвекционных потоков. Наиболее медленно процесс диффузии протекает в твердых телах. Однако, опыты показывают, что при контакте хорошо очищенных поверхностей двух металлов через длительное время в каждом из них обнаруживается атомы другого металла. Диффузия и броуновское движение – родственные явления. Взаимопроникновение соприкасающихся веществ друг в друга и беспорядочное движение мельчайших частиц, взвешенных в жидкости или газе, происходят вследствие хаотичного теплового движения молекул. Силы, действующие между двумя молекулами, зависят от расстояния между ними. Молекулы представляют собой сложные пространственные структуры, содержащие как положительные, так и отрицательные заряды. Если расстояние между молекулами достаточно велико, то преобладают силы межмолекулярного притяжения. На малых расстояниях преобладают силы отталкивания. Зависимости результирующей силы и потенциальной энергии взаимодействия между молекулами от расстояния между их центрами качественно изображены на рис. 3.1.2. При некотором расстоянии сила взаимодействия обращается в нуль. Это расстояние условно можно принять за диаметр молекулы. Потенциальная энергия взаимодействия при минимальна. Чтобы удалить друг от друга две молекулы, находящиеся на расстоянии , нужно сообщить им дополнительную энергию . Величина называется глубиной потенциальной ямы или энергией связи .
|
- http://www.ngpedia.ru/id626321p1.html
- http://naparah.com/fizika/09181681.html
- http://physics.ru/courses/op25part1/content/chapter3/section/paragraph1/theory.html
- http://ency.info/materiya-i-dvigenie/molekulyarno-kineticheskaya-teoriya/355-svojstva-zhidkoste
- http://studopedia.info/5-101268.html
- http://lektsii.org/8-88658.html

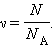
 , и упорядоченном движении со скоростью потока
, и упорядоченном движении со скоростью потока 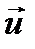 . Скорость
. Скорость 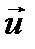 намного меньше, чем
намного меньше, чем 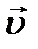 , т.е. (
, т.е. (  ). При рассмотрении внутреннего трения нас будет интересовать средний импульс молекулы в потоке жидкости
). При рассмотрении внутреннего трения нас будет интересовать средний импульс молекулы в потоке жидкости 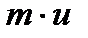 .
. и
и 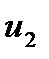
 . При перемещении одних слоев реальной жидкости относительно других, возникают силы внутреннего трения, направленные по касательной к поверхности слоев. Действие этих сил проявляется в том, что со стороны слоя, движущегося быстрее, на слой, движущийся медленнее, действует ускоряющая сила. Со стороны же слоя, движущегося медленнее, на слой, движущийся быстрее, действует тормозящая сила.
. При перемещении одних слоев реальной жидкости относительно других, возникают силы внутреннего трения, направленные по касательной к поверхности слоев. Действие этих сил проявляется в том, что со стороны слоя, движущегося быстрее, на слой, движущийся медленнее, действует ускоряющая сила. Со стороны же слоя, движущегося медленнее, на слой, движущийся быстрее, действует тормозящая сила.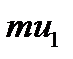 и
и  . Вследствии теплового движения происходит непрерывный переход молекул из одного слоя в другой. Попав в другой слой, молекула претерпевает столкновения с молекулами этого слоя, в результате чего она либо отдает избыток своего импульса другим молекулам (если она прилетела из слоя, движущегося быстрее), либо увеличивает свой импульс за счет других молекул ( если она “прилетела” из слоя, движущегося медленнее). В итоге импульс слоя, движущегося быстрее убывает, а слоя, движущегося медленнее, возрастает. Следовательно, слои ведут себя так, как если бы к слою, скорость которого больше, была приложена сила тормозящая его движение, а к слою скорость которого меньше – такая же по модулю сила, ускоряющая его движение. Таким образом, причиной возникновения вязкости ( внутреннего трения) является перенос импульса от одного слоя к другому. Экспериментально установлено, что модуль силы внутреннего трения, приложенный к площадке
. Вследствии теплового движения происходит непрерывный переход молекул из одного слоя в другой. Попав в другой слой, молекула претерпевает столкновения с молекулами этого слоя, в результате чего она либо отдает избыток своего импульса другим молекулам (если она прилетела из слоя, движущегося быстрее), либо увеличивает свой импульс за счет других молекул ( если она “прилетела” из слоя, движущегося медленнее). В итоге импульс слоя, движущегося быстрее убывает, а слоя, движущегося медленнее, возрастает. Следовательно, слои ведут себя так, как если бы к слою, скорость которого больше, была приложена сила тормозящая его движение, а к слою скорость которого меньше – такая же по модулю сила, ускоряющая его движение. Таким образом, причиной возникновения вязкости ( внутреннего трения) является перенос импульса от одного слоя к другому. Экспериментально установлено, что модуль силы внутреннего трения, приложенный к площадке 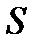 , лежащий на границе между слоями определяется формулой
, лежащий на границе между слоями определяется формулой (1)
(1) – площадь на границе между слоями поверхности, на которой действует сила
– площадь на границе между слоями поверхности, на которой действует сила  . Величина
. Величина  – показывает, как быстро меняется скорость при переходе от слоя к слою в направлении
– показывает, как быстро меняется скорость при переходе от слоя к слою в направлении  , перпендикулярном направлению движения слоев, и называется градиентом скорости. В этой формуле
, перпендикулярном направлению движения слоев, и называется градиентом скорости. В этой формуле  – коэффициент пропорцианальности, зависящий от природы и состояния жидкости, называется вязкостью.
– коэффициент пропорцианальности, зависящий от природы и состояния жидкости, называется вязкостью. (2)
(2)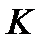 — импульс, передаваемый от слоя к слою, т.е. поток импульса через поверхность
— импульс, передаваемый от слоя к слою, т.е. поток импульса через поверхность 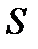 . Знак минус в этой формуле обусловлен, тем обстоятельством, что импуль “течет” в направлении убывания скорости
. Знак минус в этой формуле обусловлен, тем обстоятельством, что импуль “течет” в направлении убывания скорости . Поэтому знаки потока импульса и производной
. Поэтому знаки потока импульса и производной 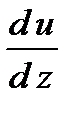 противоположны. Здесь вязкость показывает, какое количество импульса (поток импульса) переносится через единицу площади за единицу времени при градиенте скорости, равном единице.
противоположны. Здесь вязкость показывает, какое количество импульса (поток импульса) переносится через единицу площади за единицу времени при градиенте скорости, равном единице. или в паскаль–секундах
или в паскаль–секундах 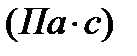 т.е.
т.е. 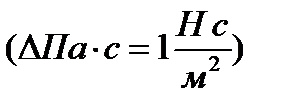 . Экспериментальную формулу Ньютона (2) можно вывести с помощью молекулярно – кинетической теории. При этом получается выражение для вязкости
. Экспериментальную формулу Ньютона (2) можно вывести с помощью молекулярно – кинетической теории. При этом получается выражение для вязкости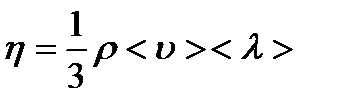 (3)
(3)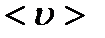 – средняя скорость теплового движения молкул,
– средняя скорость теплового движения молкул,  – средняя длина свободного пробега молекул,
– средняя длина свободного пробега молекул,  – плотность жидкости или газа. Вязкость является важной физико- технической характеристикой вещества и зависит от температуры и от природы вещества. С повышением температуры вязкость уменьшается.
– плотность жидкости или газа. Вязкость является важной физико- технической характеристикой вещества и зависит от температуры и от природы вещества. С повышением температуры вязкость уменьшается.