Живой организм и его функционирование находятся в постоянной зависимости от окружающей среды. Интенсивность обмена с внешней средой и скорость внутриклеточных процессов обмена веществ поддерживают постоянство внутренней среды и целостность организма.
Как было указано, обмен веществ в организме человека протекает не хаотично; он интегрирован и тонко настроен. Все превращения органических веществ, процессы анаболизма и катаболизма тесно связаны друг с другом. В частности, процессы синтеза и распада взаимосвязаны, координированы и регулируются нейрогормональными механизмами, придающими химическим процессам нужное направление. В организме человека, как и в живой природе вообще, не существует самостоятельного обмена белков, жиров, углеводов и нуклеиновых кислот. Все превращения объединены в целостный процесс метаболизма, подчиняющийся диалектическим закономерностям взаимозависимости и взаимообусловленности, допускающий также взаимопревращения между отдельными классами органических веществ. Подобные взаимопревращения диктуются физиологическими потребностями организма, а также целесообразностью замены одних классов органических веществ другими в условиях блокирования какого-либо процесса при патологии.
Еще Кребс и Корнберг отмечали, что, несмотря на огромное разнообразие пищевых веществ (белки, жиры, углеводы), число химических реакций, обеспечивающих их превращения (распад) и образование энергии, «удивительно мало». Эти закономерности свойственны как организму животных и человека, так и микроорганизмам и растениям.
В настоящее время экспериментально обосновано существование четырех главных этапов распада молекул углеводов, белков и жиров, которые интегрируют образование энергии из основных пищевых источников. На I этапе полисахариды расщепляются до моносахаридов (обычно гексоз); жиры распадаются на глицерин и высшие жирные кислоты, а белки – на составляющие их свободные аминокислоты. Следует подчеркнуть, что указанные процессы в основном являются гидролитическими, поэтому освобождающаяся в небольшом количестве энергия почти целиком используется организмами в качестве тепла.
На II этапе мономерные молекулы (гексозы, глицерин, жирные кислоты и аминокислоты) подвергаются дальнейшему распаду, в процессе которого образуются богатые энергией фосфатные соединения и ацетил-КоА. В частности, при гликолизе гексозы расщепляются до пировиноград-ной кислоты и далее до ацетил-КоА. Этот процесс сопровождается образованием ограниченного числа богатых энергией фосфатных связей путем субстратного фосфорилирования. На этом этапе высшие жирные кислоты аналогично распадаются до ацетил-КоА, в то время как глицерин окисляется по гликолитическому пути до пировиноградной кислоты и далее до ацетил-КоА. Для аминокислот ситуация на II этапе несколько отлична. При преимущественном использовании аминокислот в качестве источника энергии (при дефиците углеводов или при сахарном диабете) некоторые из них непосредственно превращаются в метаболиты лимоннокислого цикла (глутамат, аспартат), другие – опосредованно через глутамат (пролин, гистидин, аргинин), третьи – в пируват и далее в ацетил-КоА (аланин, серин, глицин, цистеин). Наконец, ряд аминокислот, в частности лейцин, изо-лейцин, расщепляется до ацетил-КоА, а из фенилаланина и тирозина, помимо ацетил-КоА, образуется оксалоацетат через фумаровую кислоту. Как видно, II этап можно назвать этапом образования ацетил-КоА, являющегося по существу единым (общим) промежуточным продуктом катаболизма основных пищевых веществ в клетках.
На III этапе ацетил-КоА (и некоторые другие метаболиты, например α-кетоглутарат, оксалоацетат) подвергаются окислению («сгоранию») в цикле ди- и трикарбоновых кислот Кребса. Окисление сопровождается образованием восстановленных форм НАДН + Н + и ФАДН2.
На IV этапе осуществляется перенос электронов от восстановленных нуклеотидов на кислород (через дыхательную цепь). Он сопровождается образованием конечного продукта – молекулы воды. Этот транспорт электронов сопряжен с синтезом АТФ в процессе окислительного фосфо-рилирования (см. главу 9).
Необходимо отметить, что, помимо взаимных переходов между разными классами веществ в организме, доказано существование более сложных форм связи. В частности, интенсивность и направление любой химической реакции определяются ферментами, т.е. белками, которые оказывают непосредственное влияние на обмен липидов, углеводов и нуклеиновых кислот. В свою очередь синтез любого белка-фермента требует участия ДНК и всех 3 типов рибонуклеиновых кислот: тРНК, мРНК и рРНК. Если к этому добавить влияние гормонов, а также продуктов распада какого-либо одного класса веществ (например, биогенных аминов) на обмен других классов органических веществ, то становятся понятными удивительная согласованность и координированность огромного разнообразия химических процессов, совершающихся в организме. Многие из этих процессов были подробно освещены при описании обмена отдельных классов веществ (см. главы 10-12). В данной главе кратко представлены примеры взаимных переходов отдельных структурных элементов белков, жиров, углеводов (рис. 15.1) и нуклеиновых кислот в процессе их превращений и обмена.
Помимо прямых переходов метаболитов этих классов веществ друг в друга, существует тесная энергетическая связь, когда энергетические потребности могут обеспечиваться окислением какого-либо одного класса органических веществ при недостаточном поступлении с пищей других. Важность белков (в частности, ферментов, гормонов и др.) в обмене всех типов химических соединений слишком очевидна и не требует доказательств. Ранее было отмечено большое значение белков и аминокислот для синтеза ряда специализированных соединений (пуриновые и пиримиди-новые нуклеотиды, порфирины, биогенные амины и др.). Кетогенные аминокислоты, образующие в процессе обмена ацетоуксусную кислоту (ацетоацетил-КоА), могут непосредственно участвовать в синтезе жирных кислот и стеринов. Аналогично могут использоваться гликогенные аминокислоты через ацетил-КоА, но после предварительного превращения в пируват. Некоторые структурные компоненты специализированных липидов, в частности фосфоглицеринов, имеют своим источником аминокислоты и их производные, например серин, этаноламин, сфингозин и холин. Необходимо подчеркнуть, что превращение углеродных скелетов кетогенных или гликогенных аминокислот в жирные кислоты является необратимым процессом, хотя нельзя исключить возможности частичного синтеза глутамата и опосредованно других аминокислот из продуктов распада жирных кислот – ацетил-КоА – через цикл трикарбоновых кислот, включающий α-кетоглутарат. В то же время из глицерина нейтральных жиров через пируват полностью осуществляется синтез углеродных скелетов некоторых гликогенных аминокислот.
Рис. 15.1. Взаимосвязь белков, жиров и углеводов.
Продукты гидролиза пищевых и тканевых триацилглицеролов, в частности высшие жирные кислоты, участвуют непосредственно в образовании сложных белков – липопротеинов плазмы крови. В составе липопротеинов, являющихся, таким образом, транспортной формой жирных кислот, они доставляются в органы-мишени, в которых жирные кислоты служат или источником энергии (сердечная и поперечно-полосатая мускулатура), или предшественниками синтеза тканевых триацилглицеролов с последующим их отложением в клетках ряда органов (депо липидов).
Получены доказательства синтеза глюкозы из большинства аминокислот. Для некоторых аминокислот (аланин, аспарагиновая и глутами-новая кислоты) связь с глюконеогенезом является непосредственной, для других она осуществляется через побочные метаболические пути. Следует особо подчеркнуть, что три α-кетокислоты (пируват, оксалоацетат и кето-глутарат), образующиеся соответственно из аланина, аспартата и глу-тамата, не только служат исходным материалом для синтеза глюкозы, но являются своеобразными кофакторами при распаде ацетильных остатков всех классов пищевых веществ в цикле Кребса для получения энергии.
Синтез незаменимых аминокислот из продуктов обмена углеводов и жиров в организме животных отсутствует. Клетки животных не содержат ферментных систем, катализирующих синтез углеродных скелетов этих аминокислот. В то же время организм может нормально развиваться исключительно при белковом питании, что также свидетельствует о возможности синтеза углеводов из белков. Процесс синтеза углеводов из аминокислот получил название глюконеогенеза. Он доказан прямым путем в опытах на животных с экспериментальным диабетом: более 50% введенного белка превращается в глюкозу. Как известно, при диабете организм теряет способность утилизировать глюкозу, и энергетические потребности покрываются за счет окисления аминокислот и жирных кислот. Доказано также, что исходными субстратами для глюконеогенеза являются те аминокислоты, распад которых сопровождается образованием прямо или опосредованно пировиноградной кислоты (например, аланин, серин, треонин и цистеин). Более того, имеются доказательства существования в организме своеобразного циклического процесса – глюкозоаланинового цикла, участвующего в тонкой регуляции концентрации глюкозы в крови в тех условиях, когда в период между приемами пищи организм испытывает дефицит глюкозы. Источниками пирувата при этом являются указанные аминокислоты, образующиеся в мышцах при распаде белков и поступающие в печень, в которой они подвергаются дезами-нированию. Образовавшийся аммиак в печени обезвреживается, участвуя в синтезе мочевины, которая выделяется из организма. Дефицит мышечных белков затем восполняется за счет поступления аминокислот пищи.
Энергетическая ценность пищи оказывает определенное влияние на белковый обмен, контролируемый азотистым балансом. Так, если потребляемая энергия пищи ниже минимального уровня, то наблюдается увеличение экскреции азота, и, наоборот, при увеличении энергетической ценности пищи экскреция азота с мочой снижается.
Между циклом лимонной кислоты и орнитиновым циклом мочевино-образования имеются сложные связи, определяющие в известной степени скорость реакций, зависимую от энергетических потребностей клетки и концентраций конечных продуктов метаболизма. Как было показано (см. главу 12), фумаровая кислота образуется в процессе распада аргинино-янтарной кислоты, синтез которой в свою очередь требует наличия аминокислоты аспартата. Образовавшаяся фумаровая кислота (из предшественника аминокислоты аспартата) далее вступает в цикл лимонной кислоты и под действием двух ферментов этого цикла: фумаратгидратазы и малат-дегидрогеназы – превращается в оксалоацетат, который при участии специфической трансаминазы вновь превращается в аспартат, т.е. получается своеобразный аспартат-аргининоянтарный шунт цикла лимонной кислоты, соединенного с циклом мочевинообразования (рис. 15.2). Таким образом, при помощи этого необычного сцепленного механизма происходит переплетение реакций обоих циклов (мочевинообразования и ди- и трикар-боновых кислот). Этот механизм получил название «велосипед Кребса» (The «Krebs bicycle»).
Из приведенной общей схемы (см. рис. 15.1) видно также, что имеются различные пути взаимопревращений жиров и углеводов. Практика откорма сельскохозяйственных животных давно подтвердила возможность синтеза жиров из углеводов пищи. С энергетической точки зрения, превращение углеводов в жиры следует рассматривать как накопление и депонирование энергии, хотя синтез жира сопровождается затратой энергии, которая вновь освобождается при окислении жиров в организме. Глицерин, входящий
Рис. 15.2. The «Krebs Bicycle». (Печатается с любезного разрешения д-ра David L. Nelson и д-ра М.М. Сох, 1993.)
в состав триацилглицеролов и фосфоглицеринов, может легко образоваться из промежуточных метаболитов гликолиза, в частности из глицераль-дегид-3-фосфата. Следует, однако, подчеркнуть, что основным путем превращения углеводов в жиры является путь образования высших жирных кислот из ацетил-КоА, который образуется при окислительном декар-боксилировании пирувата. Последняя реакция практически необратима, поэтому образования углеводов из высших жирных кислот почти не происходит. Таким образом, синтез углеводов из жиров в принципе может происходить только из глицерина, хотя в обычных условиях реакция протекает в обратную сторону, т.е. в сторону синтеза жиров из глицерина, образующегося при окислении углеводов. Ацетил-КоА, образующийся в процессе обмена углеводов, жиров и ряда аминокислот, служит пусковым субстратом как для синтеза жирных кислот (а следовательно, и липидов вообще), так и для цикла трикарбоновых кислот. Для окисления ацетил-КоА в этом цикле требуется оксалоацетат, который является вторым ключевым субстратом в цикле Кребса. Оксалоацетат может синтезироваться из пировиноградной кислоты и СО2 благодаря реакции карбокси-лирования или образоваться из аспарагиновой кислоты в процессе транс-аминирования с α-кетоглутаратом. Две молекулы ацетил-КоА, конденсируясь, образуют ацетоуксусную кислоту (ацетоацетат), которая является источником других кетоновых тел в организме, в частности β-оксимасляной кислоты (β-оксибутирата) и ацетона (см. главу 11). Следует подчеркнуть, что ацетоуксусная и β-оксимасляная кислоты часто рассматриваются как транспортные формы активной уксусной кислоты, доставляющие ее для окисления в цикле Кребса в периферических тканях. Эти же реакции конденсации двух молекул ацетил-КоА составляют начальные этапы синтеза холестерина, в свою очередь являющегося предшественником гормонов стероидной природы, витамина D3, а также желчных кислот. Последние в виде парных желчных кислот выполняют важную функцию эмульгаторов при переваривании липидов пищи в кишечнике, а также функцию транспортеров, способствуя всасыванию высших жирных кислот. Следует указать также на использование галактозы и частично глюкозы для биосинтеза цереброзидов и гликолипидов, выполняющих важные и специфические функции в деятельности ЦНС. В этом синтезе участвуют не свободные моносахариды, а гексозамины (галактозамин и глюкозамин), биосинтез которых в свою очередь требует доставки амидного азота глутамина, интегрируя тем самым обмен углеводов, липидов и белков.
В последние годы накоплено немало экспериментальных данных, свидетельствующих о существовании в живых организмах множества регулирующих механизмов, осуществляющих метаболический контроль и обеспечивающих как взаимопревращения белков, липидов и углеводов, так и интеграцию энергии. Не отрицая значение других типов регуляции метаболизма (см. главы 8, 9), следует подчеркнуть, что движущей силой во взаимопревращениях веществ и интенсивности метаболизма, вероятнее всего, является энергетическое состояние клетки, в частности уровень АТФ (точнее, отношение АМФ/АТФ). Так, при низких концентрациях АМФ и высоких концентрациях АТФ (состояние, которое принято обозначать «энергонасыщенностью») в клетках происходит резкое снижение глико-литического распада глюкозы, обусловленное действием этих нуклеотидов на ключевой фермент гликолиза – фосфофруктокиназу и на фосфатазу фруктозо-6-фосфата. В результате в клетках накапливается не только фруктозо-6-фосфат, но и его предшественник – глюкозо-6-фосфат. Последний, являясь положительным модулятором фермента гликогенсинтазы, стимулирует синтез полисахарида – гликогена. При низких концентрациях АТФ (соответственно при высоком уровне АМФ) в клетках отмечаются стимулирование гликолиза и окисление пирувата в лимоннокислом цикле, что способствует обеспечению клеток энергией. Однако при низких концентрациях АМФ имеет место снижение скорости цикла трикарбоновых кислот, обусловленное торможением активности изоцитратдегидрогеназы, соответственно наблюдается снижение скорости синтеза АТФ и накопление изолимонной кислоты. Последняя, как известно, повышает активность другого фермента – ацетил-КоА-карбоксилазы, которая в свою очередь катализирует I стадию превращения ацетил-КоА в жирную кислоту. Благодаря этим обстоятельствам клетка переводит образовавшуюся при гликолизе молекулу ацетил-КоА с энергетического пути на путь синтеза липидов и их отложения в депо. В то же время при восстановлении скорости утилизации АТФ, что обычно наблюдается при синтезе жирных кислот, соответствующее повышение уровня АМФ способствует снижению концентрации лимонной кислоты и соответственно торможению синтеза липидов.
Перечисленными примерами абсолютно не исчерпывается все многообразие взаимопревращений органических веществ, которые постоянно совершаются в живых организмах. Здесь приведены лишь главные, магистральные каналы и пути превращения общих классов веществ и указаны ключевые субстраты и ферментные системы, обеспечивающие постоянство химических компонентов и тканей и динамичность живых структур.
Таким образом, скорость распада одних питательных веществ и биосинтеза других прежде всего определяется физиологическим состоянием и потребностями организма в энергии и метаболитах. Благодаря динамичности и координации метаболической активности обеспечивается макро- и микроскопическое постоянство всех форм живого. Выяснение фундаментальных проблем структуры и функций отдельных биомолекул может служить основой для раскрытия как молекулярных механизмов химических процессов, лежащих в основе состава и функций отдельных клеток и целостного организма, так и процессов, обеспечивающих биологическую индивидуальность живых организмов. Любые нарушения этого динамического статуса организма сопровождаются развитием патологии, тяжесть и продолжительность которой будут определяться степенью повреждения структуры и функций отдельных молекулярных и надмолекулярных компонентов клеток.
В синтезе белков из аминокислот можно выделить три этапа.
Первый этап – транскрипция – был описан в предыдущей теме. Он состоит в образовании молекул РНК на матрицах ДНК. Для синтеза белка особое значение имеет синтез матричных или информационных РНК, так как здесь записана информация о будущем белке. Транскрипция протекает в ядре клеток. Затем с помощью специальных ферментов, образовавшаяся матричная РНК перемещается в цитоплазму.
Второй этап называется рекогниция. Аминокислоты избирательно связываются с своими переносчиками транспортными РНК.
Все т-РНК построены сходным образом. Молекула каждой т-РНК представляет собой полинуклеотидную цепь, изогнутую в виде «клеверного листа». Молекулы т-РНК устроены таким образом, что имеют разные концы, имеющие сродство и с м-РНК (антикодон) и с аминокислотами. Т-РНК имеет в клетке 60 разновидностей.
Для соединения аминокислот с транспортными РНК служит особый фермент т-РНК синтетаза или, точнее, амино-ацил – т-РНК синтетаза.
Третий этап биосинтеза белка называется трансляция. Он происходит на рибосомах. Каждая рибосома состоит из двух частей – большой и малой субъединиц. Они состоят из рибосомных РНК и белков.
Трансляция начинается с присоединения матричной РНК к рибосоме. Затем к образовавшемуся комплексу начинают присоединяться т-РНК с аминокислотами. Присоединение это происходит путем связывания антикодона т-РНК к кодону информационной РНК на основании принципа комплементарности. Одновременно к рибосоме могут присоединится не более двух т-РНК. Далее аминокислоты соединяются друг с другом пептидной связью, образуя постепенно полипептид. После этого рибосома передвигает информационную РНК ровно на один кодон. Дальше процесс повторяется снова до тех пор пока информационная РНК не закончится. На конце и-РНК находятся бессмысленные кодоны, которые являются точками в записи и одновременно командой для рибосомы, что она должна отделиться от и-РНК
Таким образом, можно выделить несколько особенности биосинтеза белков.
1. Первичная структура белков формируется строго на основе данных записанных в молекулах ДНК и информационных РНК,
2. Высшие структуры белка (вторичная, третичная, четвертичная) возникают самопроизвольно на основе первичной структуры.
3. В некоторых случаях полипептидная цепь после завершения синтеза подвергается незначительной химической модификации, в результате чего в ней появляются некодируемые аминокислоты, не относящиеся к 20 обычным. Примером такого превращения является белок коллаген, где аминокислоты лизин и пролин превращаются в оксипролин и оксилизин.
4. Синтез белков в организме ускоряется соматотропным гормоном и гормоном тестостероном.
5. Синтез белков очень энергоемкий процесс, требующий огромного количества АТФ.
6. Многие антибиотики подавляют трансляцию.
Метаболизм аминокислот.
Аминокислоты могут использоваться для синтеза различных небелковых соединений. Например, из аминокислот синтезируется глюкоза, азотистые основания, небелковая часть гемоглобина – гем, гормоны – адреналин, тироксин и такие важные соединения, как креатин, карнитин, принимающие участие в энергетическом обмене.
Часть аминокислот подвергается распаду до углекислого газа, воды и аммиака.
Распад начинается с реакций общих для большинства аминокислот.
К ним относятся.
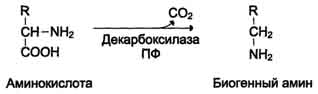
1. Декарбоксилирование — отщепление от аминокислот карбоксильной группы в виде углекислого газа.
ПФ (пиридоксальфосфат) – кофермент производное витамина В6.
Так, например, образуется гистамин из аминокислоты гистидина. Гистамин – важное сосудорасширяющее вещество.
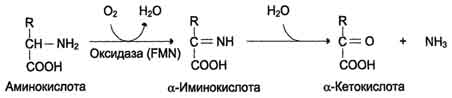
2. Дезаминирование — отцепление аминогруппы в виде NH3 . У человека дезаминирование аминокислот идет окислительным путем.
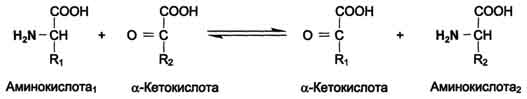
3. Трансаминирование – реакция между аминокислотами и α-кетокислотами. В ходе этой реакции её участники обмениваются функциональными группами.
Трансаминированию подвергаются все аминокислоты. Этот процесс – главное превращение аминокислот в организме, так как у него скорость значительно выше, чем у двух первых описанных реакций.
Трансаминирование выполняет две основные функции.
1. За счет этих реакций одни аминокислоты превращаются в другие. При этом общее количество аминокислот не меняется но меняется общее соотношение между ними в организме. С пищей в организм поступают чужеродные белки, у которых аминокислоты находятся в иных пропорциях. Путем трансаминирования происходит корректировка аминокислотного состава организма.
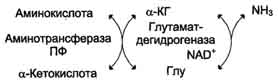
2. Трансаминирование является составной частью процесса косвенного дезаминирования аминокислот – процесса, с которого начинается распад большинства аминокислот.
Схема косвенного дезаминирования.
В результате трансаминирования образуются α-кетокислоты и аммиак. Первые разрушаются до углекислого газа и воды. Аммиак для организма высокотоксичен. Поэтому в организме существуют молекулярные механизмы его обезвреживания.
Синтез белка с энергетической точки зрения это
В первой половине 19 в. многие химики, и среди них в первую очередь Ю.фон Либих, постепенно пришли к выводу, что белки представляют собой особый класс азотистых соединений. Название «протеины» (от греч. protos первый) предложил в 1840 голландский химик Г.Мульдер.
Белки в твердом состоянии белого цвета, а в растворе бесцветны, если только они не несут какой-нибудь хромофорной (окрашенной) группы, как, например, гемоглобин. Растворимость в воде у разных белков сильно варьирует. Она изменяется также в зависимости от рН и от концентрации солей в растворе, так что можно подобрать условия, при которых один какой-нибудь белок будет избирательно осаждаться в присутствии других белков. Этот метод «высаливания» широко используется для выделения и очистки белков. Очищенный белок часто выпадает в осадок из раствора в виде кристаллов.
В сравнении с другими соединениями молекулярная масса белков очень велика от нескольких тысяч до многих миллионов дальтон. Поэтому при ультрацентрифугировании белки осаждаются, и притом с разной скоростью. Благодаря присутствию в молекулах белков положительно и отрицательно заряженных групп они движутся с разной скоростью и в электрическом поле. На этом основан электрофорез метод, применяемый для выделения индивидуальных белков из сложных смесей. Очистку белков проводят и методом хроматографии.
Строение. Белки это полимеры, т.е. молекулы, построенные, как цепи, из повторяющихся мономерных звеньев, или субъединиц, роль которых играют у них a -аминокислоты. Общая формула аминокислот
где R атом водорода или какая-нибудь органическая группа.
Белковая молекула (полипептидная цепь) может состоять всего лишь из относительно небольшого числа аминокислот или из нескольких тысяч мономерных звеньев. Соединение аминокислот в цепи возможно потому, что у каждой из них имеются две разные химические группы: обладающая основными свойствами аминогруппа, NH2 , и кислотная карбоксильная группа, СООН. Обе эти группы присоединены к a -атому углерода. Карбоксильная группа одной аминокислоты может образовать амидную (пептидную) связь с аминогруппой другой аминокислоты:
После того как две аминокислоты таким образом соединились, цепь может наращиваться путем добавления ко второй аминокислоте третьей и т.д. Как видно из приведенного выше уравнения, при образовании пептидной связи выделяется молекула воды. В присутствии кислот, щелочей или протеолитических ферментов реакция идет в обратном направлении: полипептидная цепь расщепляется на аминокислоты с присоединением воды. Такая реакция называется гидролизом. Гидролиз протекает спонтанно, а для соединения аминокислот в полипептидную цепь требуется энергия.
Карбоксильная группа и амидная группа (или сходная с ней имидная в случае аминокислоты пролина) имеются у всех аминокислот, различия же между аминокислотами определяются природой той группы, или «боковой цепи», которая обозначена выше буквой R . Роль боковой цепи может играть и один атом водорода, как у аминокислоты глицина, и какая-нибудь объемистая группировка, как у гистидина и триптофана. Некоторые боковые цепи в химическом смысле инертны, тогда как другие обладают заметной реакционной способностью.
Синтезировать можно многие тысячи различных аминокислот, и множество различных аминокислот встречается в природе, но для синтеза белков используется только 20 видов аминокислот: аланин, аргинин, аспарагин, аспарагиновая кислота, валин, гистидин, глицин, глутамин, глутаминовая кислота, изолейцин, лейцин, лизин, метионин, пролин, серин, тирозин, треонин, триптофан, фенилаланин и цистеин (в белках цистеин может присутствовать в виде димера цистина). Правда, в некоторых белках присутствуют и другие аминокислоты, помимо регулярно встречающихся двадцати, но они образуются в результате модификации какой-нибудь из двадцати перечисленных уже после того, как она включилась в белок.
Оптическая активность. У всех аминокислот, за исключением глицина, к a -атому углерода присоединены четыре разные группы. С точки зрения геометрии, четыре разные группы могут быть присоединены двумя способами, и соответственно есть две возможные конфигурации, или два изомера, относящиеся друг к другу, как предмет к своему зеркальному отражению, т.е. как левая рука к правой. Одну конфигурацию называют левой, или левовращающей ( L ), а другую правой, или правовращающей ( D ), поскольку два таких изомера различаются направлением вращения плоскости поляризованного света. В белках встречаются только L -аминокислоты (исключение составляет глицин; он может быть представлен лишь одной формой, поскольку у него две из четырех групп одинаковы), и все они обладают оптической активностью (поскольку имеется только один изомер). D -аминокислоты в природе редки; они встречаются в некоторых антибиотиках и клеточной оболочке бактерий.
Последовательность аминокислот. Аминокислоты в полипептидной цепи располагаются не случайным образом, а в определенном фиксированном порядке, и именно этот порядок определяет функции и свойства белка. Варьируя порядок расположения 20 видов аминокислот, можно получить огромное число разных белков, точно так же, как из букв алфавита можно составить множество разных текстов.
В прошлом на определение аминокислотной последовательности какого-нибудь белка уходило нередко несколько лет. Прямое определение и теперь достаточно трудоемкое дело, хотя созданы приборы, позволяющие вести его автоматически. Обычно проще бывает определить нуклеотидную последовательность соответствующего гена и вывести из нее аминокислотную последовательность белка. К настоящему времени уже определены аминокислотные последовательности многих сотен белков. Функции расшифрованных белков, как правило, известны, и это помогает представить себе возможные функции сходных белков, образующихся, например, при злокачественных новообразованиях.
Сложные белки. Белки, состоящие из одних только аминокислот, называют простыми. Часто, однако, к полипептидной цепи бывают присоединены атом металла или какое-нибудь химическое соединение, не являющееся аминокислотой. Такие белки называются сложными. Примером может служить гемоглобин: он содержит железопорфирин, который определяет его красный цвет и позволяет ему играть роль переносчика кислорода.
В названиях большинства сложных белков содержится указание на природу присоединенных групп: в гликопротеинах присутствуют сахара, в липопротеинах жиры. Если от присоединенной группы зависит каталитическая активность фермента, то ее называют простетической группой. Нередко какой-нибудь витамин играет роль простетической группы или входит в ее состав. Витамин А, например, присоединенный к одному из белков сетчатки, определяет ее чувствительность к свету.
Третичная структура. Важна не столько сама аминокислотная последовательность белка (первичная структура), сколько способ ее укладки в пространстве. По всей длине полипептидной цепи ионы водорода образуют регулярные водородные связи, которые придают ей форму спирали либо слоя (вторичная структура). Из комбинации таких спиралей и слоев возникает компактная форма следующего порядка третичная структура белка. Вокруг связей, удерживающих мономерные звенья цепи, возможны повороты на небольшие углы. Поэтому с чисто геометрической точки зрения число возможных конфигураций для любой полипептидной цепи бесконечно велико. В действительности же каждый белок существует в норме только в одной конфигурации, определяемой его аминокислотной последовательностью. Структура эта не жесткая, она как бы « дышит» колеблется вокруг некой средней конфигурации. Цепь складывается в такую конфигурацию, при которой свободная энергия (способность производить работу) минимальна, подобно тому как отпущенная пружина сжимается лишь до состояния, соответствующего минимуму свободной энергии. Нередко одна часть цепи бывает жестко сцеплена с другой дисульфидными ( SS) связями между двумя остатками цистеина. Отчасти именно поэтому цистеин среди аминокислот играет особо важную роль.
Сложность строения белков столь велика, что пока еще невозможно вычислить третичную структуру белка, если даже известна его аминокислотная последовательность. Но если удается получить кристаллы белка, то его третичную структуру можно определить по дифракции рентгеновских лучей.
У структурных, сократительных и некоторых других белков цепи вытянуты и несколько лежащих рядом слегка свернутых цепей образуют фибриллы; фибриллы, в свою очередь, складываются в более крупные образования волокна. Однако большинство белков в растворе имеет глобулярную форму: цепи свернуты в глобуле, как пряжа в клубке. Свободная энергия при такой конфигурации минимальна, поскольку гидрофобные («отталкивающие воду») аминокислоты скрыты внутри глобулы, а гидрофильные («притягивающие воду») находятся на ее поверхности.
Многие белки это комплексы из нескольких полипептидных цепей. Такое строение называется четвертичной структурой белка. Молекула гемоглобина, например, состоит из четырех субъединиц, каждая из которых представляет собой глобулярный белок.
Структурные белки благодаря своей линейной конфигурации образуют волокна, у которых предел прочности на разрыв очень высок, глобулярная же конфигурация позволяет белкам вступать в специфические взаимодействия с другими соединениями. На поверхности глобулы при правильной укладке цепей возникают определенной формы полости, в которых размещены реакционноспособные химические группы. Если данный белок фермент, то другая, обычно меньшая, молекула какого-то вещества входит в такую полость подобно тому, как ключ входит в замок; при этом меняется конфигурация электронного облака молекулы под влиянием находящихся в полости химических групп, и это вынуждает ее определенным образом реагировать. Таким способом фермент катализирует реакцию. В молекулах антител тоже имеются полости, в которых различные чужеродные вещества связываются и тем самым обезвреживаются. Модель «ключа и замка», объясняющая взаимодействие белков с другими соединениями, позволяет понять специфичность ферментов и антител, т.е. их способность реагировать только с определенными соединениями.
Белки у разных видов организмов. Белки, выполняющие одну и ту же функцию у разных видов растений и животных и потому носящие одно и то же название, имеют и сходную конфигурацию. Они, однако, несколько различаются по своей аминокислотной последовательности. По мере того как виды дивергируют от общего предка, некоторые аминокислоты в определенных положениях замещаются в результате мутаций другими. Вредные мутации, являющиеся причиной наследственных болезней, выбраковываются естественным отбором, но полезные или по крайней мере нейтральные могут сохраняться. Чем ближе друг к другу два каких-нибудь биологических вида, тем меньше различий обнаруживается в их белках.
Некоторые белки меняются относительно быстро, другие весьма консервативны. К последним принадлежит, например, цитохром с дыхательный фермент, имеющийся у большинства живых организмов. У человека и шимпанзе его аминокислотные последовательности идентичны, а в цитохроме с пшеницы иными оказались лишь 38% аминокислот. Даже сравнивая человека и бактерии, сходство цитохромов с (различия затрагивают здесь 65% аминокислот) все еще можно заметить, хотя общий предок бактерии и человека жил на Земле около двух миллиардов лет назад. В наше время сравнение аминокислотных последовательностей часто используют для построения филогенетического (генеалогического) древа, отражающего эволюционные связи между разными организмами.
Денатурация. Синтезированная молекула белка, складываясь, приобретает свойственную ей конфигурацию. Эта конфигурация, однако, может разрушиться при нагревании, при изменении рН, под действием органических растворителей и даже при простом взбалтывании раствора до появления на его поверхности пузырьков. Измененный таким образом белок называют денатурированным; он утрачивает свою биологическую активность и обычно становится нерастворимым. Хорошо знакомые всем примеры денатурированного белка вареные яйца или взбитые сливки. Небольшие белки, содержащие всего лишь около сотни аминокислот, способны ренатурировать, т.е. вновь приобретать исходную конфигурацию. Но большинство белков превращается при этом просто в массу спутанных полипептидных цепей и прежнюю конфигурацию не восстанавливает.
Одна из главных трудностей при выделении активных белков связана с их крайней чувствительностью к денатурации. Полезное применение это свойство белков находит при консервировании пищевых продуктов: высокая температура необратимо денатурирует ферменты микроорганизмов, и микроорганизмы погибают.
Для синтеза белка живой организм должен располагать системой ферментов, способных присоединять одну аминокислоту к другой. Необходим также источник информации, которая бы определяла, какие именно аминокислоты следует соединять. Поскольку в организме имеются тысячи видов белков и каждый из них состоит в среднем из нескольких сотен аминокислот, необходимая информация должна быть поистине огромной. Хранится она (подобно тому, как хранится запись на магнитной ленте) в молекулах нуклеиновых кислот, из которых состоят гены. См . также НАСЛЕДСТВЕННОСТЬ; НУКЛЕИНОВЫЕ КИСЛОТЫ.
Активация ферментов. Синтезированная из аминокислот полипептидная цепь это далеко не всегда белок в его окончательной форме. Многие ферменты синтезируются сначала в виде неактивных предшественников и переходят в активную форму лишь после того, как другой фермент удалит на одном из концов цепи несколько аминокислот. В такой неактивной форме синтезируются некоторые из пищеварительных ферментов, например трипсин; эти ферменты активируются в пищеварительном тракте в результате удаления концевого фрагмента цепи. Гормон инсулин, молекула которого в активной форме состоит из двух коротких цепей, синтезируется в виде одной цепи, т.н. проинсулина. Затем средняя часть этой цепи удаляется, а оставшиеся фрагменты связываются друг с другом, образуя активную молекулу гормона. Сложные белки образуются лишь после того, как к белку будет присоединена определенная химическая группа, а для этого присоединения часто тоже требуется фермент.
Метаболический кругооборот. После скармливания животному аминокислот, меченных радиоактивными изотопами углерода, азота или водорода, метка быстро включается в его белки. Если меченые аминокислоты перестают поступать в организм, то количество метки в белках начинает снижаться. Эти эксперименты показывают, что образовавшиеся белки не сохраняются в организме до конца жизни. Все они, за немногими исключениями, находятся в динамичном состоянии, постоянно распадаются до аминокислот, а затем вновь синтезируются.
Некоторые белки распадаются, когда гибнут и разрушаются клетки. Это постоянно происходит, например, с эритроцитами и клетками эпителия, выстилающего внутреннюю поверхность кишечника. Кроме того, распад и ресинтез белков протекают и в живых клетках. Как ни странно, о распаде белков известно меньше, чем об их синтезе. Ясно, однако, что в распаде участвуют протеолитические ферменты, сходные с теми, которые расщепляют белки до аминокислот в пищеварительном тракте.
Период полураспада у разных белков различен от нескольких часов до многих месяцев. Единственное исключение молекулы коллагена. Однажды образовавшись, они остаются стабильными, не обновляются и не замещаются. Со временем, однако, меняются некоторые их свойства, в частности эластичность, а поскольку они не обновляются, следствием этого оказываются определенные возрастные изменения, например появление морщин на коже.
Синтетические белки. Химики давно уже научились полимеризовать аминокислоты, но аминокислоты соединяются при этом неупорядоченно, так что продукты такой полимеризации мало похожи на природные. Правда, имеется возможность соединять аминокислоты в заданном порядке, что позволяет получать некоторые биологически активные белки, в частности инсулин. Процесс достаточно сложен, и таким способом удается получать лишь те белки, в молекулах которых содержится около сотни аминокислот. Предпочтительнее вместо этого синтезировать или выделить нуклеотидную последовательность гена, соответствующую желаемой аминокислотной последовательности, а затем ввести этот ген в бактерию, которая и будет вырабатывать путем репликации большое количество нужного продукта. У этого метода, впрочем, тоже есть свои недостатки. См . также ГЕННАЯ ИНЖЕНЕРИЯ.
Когда белки в организме распадаются до аминокислот, эти аминокислоты могут быть снова использованы для синтеза белков. В то же время и сами аминокислоты подвержены распаду, так что они реутилизируются не полностью. Ясно также, что в период роста, при беременности и заживлении ран синтез белков должен превышать распад. Некоторые же белки организм непрерывно теряет; это белки волос, ногтей и поверхностного слоя кожи. Поэтому для синтеза белков каждый организм должен получать аминокислоты с пищей.
Источники аминокислот. Зеленые растения синтезируют из СО 2 , воды и аммиака или нитратов все 20 аминокислот, встречающихся в белках. Многие бактерии тоже способны синтезировать аминокислоты при наличии сахара (или какого-нибудь его эквивалента) и фиксированного азота, но и сахар, в конечном счете, поставляется зелеными растениями. У животных способность к синтезу аминокислот ограниченна; они получают аминокислоты, поедая зеленые растения или других животных. В пищеварительном тракте поглощенные белки расщепляются до аминокислот, последние всасываются, и уже из них строятся белки, характерные для данного организма. Ни один поглощенный белок не включается в структуры тела как таковой. Единственное исключение заключается в том, что у многих млекопитающих часть материнских антител может в интактном виде попасть через плаценту в кровоток плода, а через материнское молоко (особенно у жвачных) быть передано новорожденному сразу же после его появления на свет.
Потребность в белках. Ясно, что для поддержания жизни организм должен получать с пищей некоторое количество белков. Однако размеры этой потребности зависят от ряда факторов. Организму необходима пища и как источник энергии (калорий), и как материал для построения его структур. На первом месте стоит потребность в энергии. Это значит, что, когда углеводов и жиров в рационе мало, пищевые белки используются не для синтеза собственных белков, а в качестве источника калорий. При длительном голодании даже собственные белки расходуются на удовлетворение энергетических нужд. Если же углеводов в рационе достаточно, то потребление белков может быть снижено.
Азотистый баланс. В среднем ок. 16% всей массы белка составляет азот. Когда входившие в состав белков аминокислоты расщепляются, содержавшийся в них азот выводится из организма с мочой и (в меньшей мере) с калом в виде различных азотистых соединений. Удобно поэтому для оценки качества белкового питания использовать такой показатель, как азотистый баланс, т.е. разность (в граммах) между количеством азота, поступившего в организм, и количеством выведенного азота за сутки. При нормальном питании у взрослого эти количества равны. У растущего организма количество выведенного азота меньше количества поступившего, т.е. баланс положителен. При нехватке белков в рационе баланс отрицателен. Если калорий в рационе достаточно, но белки в нем полностью отсутствуют, организм сберегает белки. Белковый обмен при этом замедляется, и повторная утилизация аминокислот в синтезе белка идет с максимально возможной эффективностью. Однако потери неизбежны, и азотистые соединения все же выводятся с мочой и частично с калом. Количество азота, выведенного из организма за сутки при белковом голодании, может служить мерой суточной нехватки белка. Естественно предположить, что, введя в рацион количество белка, эквивалентное этому дефициту, можно восстановить азотистый баланс. Однако это не так. Получив такое количество белка, организм начинает использовать аминокислоты менее эффективно, так что для восстановления азотистого баланса требуется некоторое дополнительное количество белка.
Если количество белка в рационе превышает необходимое для поддержания азотистого баланса, то вреда от этого, по-видимому, нет. Избыток аминокислот просто используется как источник энергии. В качестве особенно яркого примера можно сослаться на эскимосов, которые потребляют мало углеводов и примерно в десять раз больше белка, чем требуется для поддержания азотистого баланса. В большинстве случаев, однако, использование белка в качестве источника энергии невыгодно, поскольку из определенного количества углеводов можно получить намного больше калорий, чем из такого же количества белка. В бедных странах население получает необходимые калории за счет углеводов и потребляет минимальное количество белка.
Если необходимое число калорий организм получает в форме небелковых продуктов, то минимальное количество белка, обеспечивающее поддержание азотистого баланса, составляет для взрослого человека ок. 30 г в день. Примерно столько белка содержится в четырех ломтиках хлеба или 0,5 л молока. Оптимальным считают обычно несколько большее количество; рекомендуется от 50 до 70 г.
Незаменимые аминокислоты. До сих пор белок рассматривался как нечто целое. Между тем для того, чтобы мог идти синтез белка, в организме должны присутствовать все необходимые аминокислоты. Некоторые из аминокислот организм животного сам способен синтезировать. Их называют заменимыми, поскольку они не обязательно должны присутствовать в рационе, важно лишь, чтобы в целом поступление белка как источника азота было достаточным; тогда при нехватке заменимых аминокислот организм может синтезировать их за счет тех, что присутствуют в избытке. Остальные, «незаменимые», аминокислоты не могут быть синтезированы и должны поступать в организм с пищей. Для человека незаменимыми являются валин, лейцин, изолейцин, треонин, метионин, фенилаланин, триптофан, гистидин, лизин и аргинин. (Хотя аргинин и может синтезироваться в организме, его относят к незаменимым аминокислотам, поскольку у новорожденных и растущих детей он образуется в недостаточном количестве. С другой стороны, для человека зрелого возраста поступление некоторых из этих аминокислот с пищей может стать необязательным.)
Этот список незаменимых аминокислот приблизительно одинаков также и у других позвоночных и даже у насекомых. Питательную ценность белков обычно определяют, скармливая их растущим крысам и следя за прибавкой веса животных.
Питательная ценность белков. Питательную ценность белка определяют по той незаменимой аминокислоте, которой более всего не хватает. Проиллюстрируем это на примере. В белках нашего тела содержится в среднем ок. 2% триптофана (по весу). Допустим, что в рацион входит 10 г белка, содержащего 1% триптофана, и что других незаменимых аминокислот в нем достаточно. В нашем случае 10 г этого неполноценного белка по сути эквивалентны 5 г полноценного; остальные 5 г могут послужить только источником энергии. Отметим, что, поскольку аминокислоты в организме практически не запасаются, а для того чтобы мог идти синтез белка, должны одновременно присутствовать все аминокислоты, эффект от поступления незаменимых аминокислот можно обнаружить лишь в том случае, если все они поступят в организм одновременно .
Усредненный состав большей части животных белков близок к усредненному составу белков человеческого тела, так что аминокислотная недостаточность нам вряд ли грозит, если наш рацион богат такими продуктами, как мясо, яйца, молоко и сыр. Однако есть белки, например желатин (продукт денатурации коллагена), которые содержат очень мало незаменимых аминокислот. Растительные белки, хотя они в этом смысле и лучше желатина, тоже бедны незаменимыми аминокислотами; особенно мало в них лизина и триптофана. Тем не менее и чисто вегетарианскую диету вовсе нельзя считать вредной, если только при этом потребляется несколько большее количество растительных белков, достаточное для того, чтобы обеспечить организм незаменимыми аминокислотами. Больше всего белка содержится у растений в семенах, особенно в семенах пшеницы и различных бобовых культур. Богаты белком также и молодые побеги, например у спаржи.
Синтетические белки в рационе. Добавляя небольшие количества синтетических незаменимых аминокислот или богатых ими белков к неполноценным белкам, например к белкам кукурузы, можно значительно повысить питательную ценность последних, т.е. тем самым как бы увеличить количество потребляемого белка. Другая возможность состоит в выращивании бактерий или дрожжей на углеводородах нефти с добавлением нитратов или аммиака в качестве источника азота. Полученный таким путем микробный белок может служить кормом для домашней птицы или скота, а может и непосредственно потребляться человеком. Третий, широко применяющийся, метод использует особенности физиологии жвачных животных. У жвачных в начальном отделе желудка, т.н. рубце, обитают особые формы бактерий и простейших, которые превращают неполноценные растительные белки в более полноценные микробные белки, а эти, в свою очередь, после переваривания и всасывания превращаются в животные белки. К корму скота можно добавить мочевину дешевое синтетическое азотсодержащее соединение. Обитающие в рубце микроорганизмы используют азот мочевины для превращения углеводов (которых в корме значительно больше) в белок. Около трети всего азота в корме скота может поступать в виде мочевины, что по сути и означает в определенной мере химический синтез белка. В США этот метод играет важную роль как один из способов получения белка.
Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека , тт. 12. М., 1993
Албертс Б., Брей Д., Льюс Дж. и др. Молекулярная биология клетки , тт. 13. М., 1994
РЕГУЛЯЦИЯ СИНТЕЗА БЕЛКА
Читайте также:
- Белок.В норме в моче белок отсутствует или его концентрация менее 0,002 г/л. Появление белка в моче называется протеинурией.
- В иммунном ответе организма существенное место занимает синтез антител. Выберите взаимодействие клеток, необходимое для синтеза антител.
- В норме в суточном количестве мочи может определяться 50-100 мг белка.
- Взаимодействие токсикантов с белками
- Волевая регуляция деятельности т волевые свойства личности.
- Волевая регуляция поведения
- Волновой синтезатор (WSY)
- Гомеостаз и регуляция функций в организме.
- Гомеостаз и регуляция функций в организме.
- Гормональная регуляция Обмен веществ. Витамины
- Гуморальная регуляция тонуса сосудов
- Зависимость интенсивности фотосинтеза от температуры воздуха и уровня освещенности
Г I
Согласно теории Жакоба и Моно в биосинтезе белка у бактерий участвуют по крайней мере три типа генов: структурные гены, ген-регулятор и ген-оператор. Структурные гены определяют первичную структуру синтезируемого белка. Именно эти гены в цепи ДНК являются основой для биосинтеза мРНК, которая затем поступает в рибосому и, как было указано выше, служит матрицей для биосинтеза белка. Регуляция синтеза белка путем индукции представлена на рис. 13.10.
Видно, что синтез мРНК на структурных генах молекулы ДНК непосредственно контролируется определенным участком, называемым геном-оператором. Он служит как бы пусковым механизмом для функционирования структурных генов. Ген-оператор локализован на крайнем отрезке структурного гена или структурных генов, регулируемых им. «Считывание» генетического кода, т. е. формирование мРНК, начинается спромотора — участка ДНК, являющегося точкой инициации для синтеза мРНК, и далее распространяется последовательно вдоль оператора и структурных генов. Координированный одним оператором одиночный ген или группа структурных генов образует о п е р о н.
В свою очередь деятельность оперона находится под контролирующим влиянием другого участка цепи ДНК, получившего название гена-регулятора. Поскольку структурные гены и ген-регулятор находятся в разных участках цепи ДНК, связь между ними, как предполагают Ф. Жакоб и Ж. Моно, осуществляется при помощи вещества-посредника, оказавшегося белком и названного репрессором. Образование репрессора происходит в рибосомах ядра на матрице специфической мРНК, синтезированной на гене-регуляторе. Репрессор имеет сродство к гену-оператору и обратимо соединяется с ним в комплекс. Образование такого комплекса приводит к блокированию синтеза мРНК и, следовательно, синтеза белка, т. е. функция гена-регулятора состоит в том, чтобы через белок-репрессор прекращать деятельность структурных генов, синтезирующих мРНК. Репрессор, кроме того, обладает способностью строго специфически связываться с определенными низкомолекулярными веществами, называемыми индукторами, или эффекторами. Когда такой индуктор соединяется с репрессором, последний теряет способность связываться с геном-оператором, который таким образом выходит из-под контроля гена-регулятора, и начинается синтез мРНК.
Это типичный пример отрицательной формы контроля, когда индуктор, соединяясь с белком-репрессором, вызывает изменения его третичной структуры настолько, что репрессор теряет способность связываться с геном-оператором. Этот процесс аналогичен взаимоотношениям аллостерического центра фермента с эффектором, под влиянием которого изменяется третичная структура фермента и он теряет способность связываться со своим субстратом.
Механизм описанной регуляции синтеза белка и взаимоотношения репрессора со структурными генами были доказаны в опытах на Е. coli, на примере синтеза р-галактозидазы (лактазы) — фермента, гидролизующего молочый сахар на глюкозу и галактозу. Дикий штамм Е. coli, обычно растущий на глюкозе, не может расти, если вместо глюкозы в питательную среду добавить лактозу (новый источник энергии и углерода) до тех пор, пока не будут синтезированы соответствующие ферменты (адаптивный синтез). При поступлении в клетку лактозы (индуктора) молекулы ее связываются с белком-репрессором и блокируют связь между репрессором и геном-оператором. При этом ген-оператор и структурные гены начинают снова функционировать и синтезировать необходимую мРНК, которая «дает команду» рибосомам синтезировать Р-галактозидазу. Одновременно ген-регулятор продолжает вырабатывать репрессор, но он блокируется новыми молекулами лактозы, поэтому синтез фермента продолжается. Как только молекулы лактозы будут полностью расщеплены, репрессор освобождается и, поступив в ДНК, связывает ген-оператор и блокирует синтез мРНК, а следовательно, синтез р-галактозидазы в рибосомах.
Таким образом, биосинтез мРНК, контролирующий синтез белка в рибосомах, зависит от функционального состояния репрессора. Если репрессор, который представляет собой белок, построенный из 4 субъединиц с общей молекулярной массой около 150000 Да, находится в активном состоянии, не связан с индуктором, то он блокирует ген-оператор и синтез мРНК не происходит. При поступлении метаболита-индуктора в клетку его молекулы связывают репрессор, превращая его в неактивную форму (или, возможно, снижая его сродство к гену-оператору). Структурные гены выходят из-под запрещающего контроля и начинают синтезировать нужную мРНК.
Выше было указано, что концентрация ряда ферментов в клетках резко снижается при увеличении концентрации отдаленных конечных продуктов, образующихся в цепи последовательных ферментативных реакций. Такой эффект, получивший название репрессии ферментов, часто наблюдается при реакциях биосинтеза. В этих случаях оказалось, что молекулы репрессора, также образующиеся в рибосомах ядра по «команде» гена-регулятора, являются неактивными и сами по себе не обладают способностью подавлять деятельность гена-оператора и, следовательно, всего оперона, но приобретают такую способность после образования комплекса с конечным или одним из конечных продуктов биосинтетического процесса (рис. 13.11).
Конечный продукт выступает, таким образом, в качестве корепрессора. Имеются данные, показывающие, нто в качестве корепрессоров в синтезе ферментов обмена аминокислот выступает не свободная аминокислота как конечный продукт биосинтетической реакции, а комплекс ее с тРНК — аа-тРНК.
В регуляции экспрессии структурных генов специфическое участие принимает особый белок, получивший название катаболитный ген-активирующий белок (от англ. catabolite gene activation protein, сокращенно обозначаемый САР); этот белок взаимодействует с цАМФ, образуя комплекс, способствующий прикреплению РНК-полиме-разы к промоторному участку генома. В присутствии комплекса САР-цАМФ фермент может начать транскрипцию оперона, включая структурные гены, т. е. в клетках имеется еще один, дополнительный САР-цАМФ регулятор, действующий скорее всего в качестве положительного регулятора, поскольку его присутствие необходимо для начала экспрессии гена. Таким образом, концепции Жакоба и Моно о механизме проявления активности генов признана одним из блестящих достижений молекулярной биологии. Она явилась логическим развитием многочисленных исследований, проведенных генетиками и биохимиками в предшествующие десятилетия.
В заключение следует вкратце рассмотреть вопрос о регуляции процессов диф-ференцировки клеток высших организмов. ДНК, присутствующая во всех соматических клетках, вероятнее всего, имеет одинаковую первичную структуру у данного организма и соответственно располагает информацией для синтеза любых или всех
белков тела. Тем не менее клетки печени, например, синтезируют сывороточные белки, а клетки молочной железы — белки молока. Нет сомнения в том, что в дифференцированных клетках, очевидно, существует тонкий механизм контроля деятельности ДНК в разных тканях, обеспечивающий синтез многообразия белков.
Механизмы, лежащие в основе этой регуляции, пока неизвестны. Для объяснения их имеется ряд гипотез. Предполагается, что контроль осуществляется на уровне транскрипции по аналогии с индукцией ферментов у бактерий и что в этом случае в клетках животных должны функционировать аналогичные репрессоры. Поскольку с молекулой ДНК у эукариот связаны гистоны, считается, что именно они выполняют роль ренрессоров. Однако прямые доказательства их роли в качестве репрессоров отсутствуют, как и точные данные о существовании и природе каких-либо репрессоров в клетках эукариот. Высказано предположение, что в ядре синтезируется гигантская молекула мРНК, содержащая информацию для синтеза широкого разнообразия белков, но в цитоплазму, как было показано выше, попадает только небольшая часть зрелой мРНК, а основная часть распадается. Неясны, однако, биологический смысл и назначение этого механизма избирательного распада и, соответственно, трагы огромной части молекулы мРНК.
Существует еще одно предположение, что на ДНК клетки синтезируются все возможные мРНК, которые поступают в цитоплазму, и процесс трансляции регулируется путем специфического и избирательного взаимодействия с определенными молекулами мРНК.
ИНГИБИТОРЫ СИНТЕЗА БЕЛКА
Одним из путей выяснения механизмов синтеза нуклеиновых кислот и белков в клетках является использование таких лекарственных препаратов, которые могли бы избирательно тормозить эти процессы у бактерий, не оказывая влияния на организм человека. Некоторые препараты действительно обладают таким действием, однако многие из них оказываются токсичными и для человека. В настоящее время в медицинской практике применяются многие антибиотики, часть из которых будет рассмотрена ниже с целью выяснения механизма их действия на ключевые химические реакции синтеза белка и нуклеиновых кислот.
Одним из мощных ингибиторов белкового синтеза является пуромицин. В результате структурного сходства с концевым остатком АМФ в аминоацил-тРНК’ он легко взаимодействует с А-участком пептидил-тРНК с образованием пептидил-пуро-мицина.
Поскольку пептидил-пуромицин не несет на себе триплета антикодона, он тем самым тормозит элонгацию пептидной цепи, вызывая обрыв реакции. При помощи пуромицина было доказано, например, что гормональный эффект в ряде случаев зависит от синтеза белка de novo. Укажем также, что пуромицин тормозит синтез белка как у прокариот, так и у эукариот.
Белковый синтез тормозится актиномицином D, обладающим противоопухолевым эффектом, который вследствие высокой токсичности применяется редко. Он оказывает тормозящее влияние на синтез всех типов клеточной РНК, в особенности мРНК. Это свойство вызвано тормозящим влиянием актиномицина D на ДНК-зависимую РНК-полимеразу, поскольку он связывается с остатками дезоксигуанозина цепи ДНК, выключая матричную функцию последней. Можно считать, что актиномицин D ингибирует транскрипцию ДНК.
Другим антибиотиком, также тормозящим синтез клеточной РНК, является используемый при лечении туберкулеза рифамицин. Этот препарат тормозит ДНК-зависимую РНК-полимеразу путем связывания с ферментом. Наиболее чувствительна к нему бактериальная РНК-полимераза. На организм животных этот антибиотик оказывает незначительное влияние. По механизму действия он резко отличается от актиномицина D. Следует указать на недавно открытое противовирусное действие рифамицина, в частности, он успешно используется при лечении трахомы, которая вызывается ДНК-содержащим вирусом. По-видимому, этот антибиотик найдет применение в лечении опухолей, вызываемых вирусами.
Выяснены механизмы действия ряда других антибиотиков, применяемых при лечении тифозных инфекций. Так, хлорамфеникол оказывает ингибирующее влияние на пептидилтрансферазную реакцию (на стадии элонгации) синтеза белка в 70S рибосоме бактерий. На этот процесс в 80S рибосоме он не действует. Противоположное тормозящее действие на синтез белка в 80S (без поражения процесса в 70S рибосоме) оказывает циклогексимид, являющийся ингибитором транслоказы.
Весьма интересен молекулярный механизм действия дифтерийного токсина. Он оказался наделен способностью катализировать реакцию АДФ-рибозилирования фактора элонгации (трансляционный фактор-2, TF-2), выключая тем самым его из участия в синтезе белка. Резистентность многих животных к дифтерийному токсину обусловлена трудностью проникновения токсина через мембрану клеток.
Противотуберкулезные и антибактериальные антибиотики, в частности стрептомицин и неомицин, действуют на белоксинтезирующий аппарат чувствительных к ним штаммов бактерий. Высказано предположение, что эти антибиотики вызывают ошибки в трансляции мРНК, приводящие к нарушению соответствия между кодонами и включаемыми аминокислотами; например, кодон УУУ вместо фенилаланина начинает кодировать лейцин — в результате образуется аномальный белок, что приводит к гибели бактерий.
Широко применяемые в клинике тетрациклины также оказались ингибиторами синтеза белка в 70S рибосоме (меньше тормозится синтез в 80S рибосоме). Они легко проникают через клеточную мембрану. Считается, что тетрациклины тормозят связывание аминоацил-тРНК с аминоацильным центром в 50S субчастице рибосомы. Возможно, что тетрациклины химически связываются с этим центром, выключая тем самым одну из ведущих стадий процесса трансляции.
Пенициллины не являются истинными ингибиторами синтеза белка, однако их антибактериальный эффект связан с торможением синтеза гексапептидов, входящих в состав клеточной стенки. Механизм их синтеза отличается от рибосомального механизма синтеза белка. Эритромицин и олеандомицин тормозят активность транслоказы в процессе трансляции, подобно циклогексимиду, исключительно в 80S рибосомах, т. е. тормозят синтез белка в клетках животных.
Полученные к настоящему времени данные по механизму действия антибиотиков на синтез белка с учетом стадии и топографии процесса трансляции суммированы в табл. 13.2 (по Харперу).
Таблица 13.2. Антибиотики — ингибиторы трансляции
| Стадия трансляции | Эукариоты | Прокариоты | цитоплазма | митохондрия |
| /. Инициация | |||
| Ауринтрикарбоновая кислота | — | — | + |
| //. Элонгация | |||
| Амицетин Анизомицин Линкомицин Неомицин Пуромицин Спарсомицин Тетради клины Фузидовая кислота Хлорамфеникол Циклогексимид | \ | + | |
| ///. Терминация | |||
| Амицетин Анизомицин Линкомицин Спарсомицин Стрептомицин Хлорамфеникол Эритромицин | 7 7 7 |
Н—-торможение;——отсутствие торможения; * —стимулирование; ? — не известно.
Следует еще раз подчеркнуть, что нарушение или выпадение любого звена, участвующего в синтезе белка, почти всегда приводит к развитию патологии, причем клинические проявления болезни будут определяться природой и функцией белка, синтез которого оказывается нарушенным (структурный или функциональный белок). Иногда синтезируются так называемые аномальные белки как результат действия мутагенных факторов и, соответственно, изменения генетического кода (например, гемоглобин при серповидно-клеточной анемии). Последствия этих нарушений могут выражаться в развитии самых разнообразных синдромов или заканчиваться летально. Следует отметить, что организм располагает мощными механизмами защиты: подобные изменения генетического аппарата быстро распознаются специфическими ферментами — рестриктазами, измененные последовательности вырезаются и вновь замещаются соответствующими нуклеотидами при участии полиме-раз и лигаз.
ВЗАИМОСВЯЗЬ ОБМЕНА БЕЛКОВ, ЖИРОВ И УГЛЕВОДОВ
Живой организм и условия его существования находятся в постоянной зависимости от влияния окружающей среды. «Жизнь есть способ существования белковых тел, и этот способ существования состоит по своему существу в постоянном самообновлении химических составных частей этих тел» 1 .
Обмен веществ в организме человека протекает не хаотично, а строго интегрирован и «тонко настроен». Все превращения органических веществ, процессы анаболизма и катаболизма тесно связаны друг с другом. В частности, процессы синтеза и распада взаимосвязаны, координированы и регулируются нейрогормональны-ми механизмами, придающими химическим процессам нужное направление. В организме человека, как и в живой природе вообще, не существует самостоятельного обмена белков, жиров, углеводов и нуклеиновых кислот. Все превращения объединены в единый процесс метаболизма, подчиняющийся диалектическим закономерностям взаимозависимости и взаимообусловленности.
Однако, помимо взаимных переходов между разными классами веществ в организме, доказано существование более сложных форм связи. В частности, интенсивность, направление любой химической реакции определяются ферментами, т. е. белками, которые оказывают прямое влияние на обмен липидов, углеводов и нуклеиновых кислот. В свою очередь синтез любого белка-фермента требует участия ДНК и всех трех типов рибонуклеиновых кислот — тРНК, мРНК и рРНК. Если к этому добавить влияние гормонов, а также продуктов распада какого-либо одного класса веществ (например, биогенных аминов) на обмен других классов органических веществ, то становится понятным удивительная согласованность и координированность огромного разнообразия химических процессов, совершающихся в организме. Многие из этих процессов были освещены при описании обмена отдельных классов веществ; в данной главе кратко будут представлены примеры взаимных переходов отдельных структурных элементов белков, жиров, углеводов и нуклеиновых кислот в процессе их превращений и обмена.
В настоящее время экспериментально обосновано существование трех главных этапов распада молекул углеводов, белков и жиров, которые интегрируют образование энергии из основных пищевых источников. На первом этапе полисахариды расщепляются до моносахаридов (обычно гексоз); жиры распадаются на глицерин и высшие жирные кислоты, а белки — на составляющие их свободные аминокислоты. Следует подчеркнуть, что указанные процессы в основном являются гидролитическими, поэтому освобождающаяся в небольшом количестве энергия почти целиком используется организмами в качестве тепла. На втором этапе мономерные молекулы (гек-созы, глицерин, жирные кислоты и аминокислоты) подвергаются дальнейшему распаду, в процессе которого образуются богатые энергией фосфатные соединения и ацетил-КоА. На третьем этапе, как ацетил-КоА, так и промежуточные метаболиты (ос-кето-глутарат, сукцинат и оксалоацетат), образующиеся из сотен органических веществ
Рис. 14.1. Взаимодействие белков, жиров и углеводов.
пищи, подвергаются окислению («сгоранию») в цикле Кребса, давая энергию в виде АТФ; последний образуется в процессе окислительного фосфорилирования в митохондриях при переносе электронов от восстановленных пиридиновых и флавиновых нуклеотидов на молекулярный кислород.
Интенсивность обмена веществ регулируется как гормональными факторами, так и внутриклеточными регулирующими системами; более того, имеется немало доказательств, что живые организмы наделены удивительной способностью контролировать свой метаболизм. Однако необходимы дальнейшие усилия и знания, чтобы понять тонкости тех механизмов благодаря которым в целостном организме достигается постоянство сре;Лы.
Основные пути взаимопревращений белков, жиров и углеводов представлены на рис. 14.1. Помимо прямых переходов метаболитов этих классов веществ друг в друга, существует тесная энергетическая связь, когда энергетические потребности организма могут обеспечиваться окислением какого-либо одного класса органических веществ при недостаточном поступлении с пищей других. Важность белков (в частности, ферментов, гормонов и др.) в обмене всех типов химических соединений слишком очевидна и не требует доказательств. Выше также было указано на большую роль белков и аминокислот для синтеза ряда специализированных соединений (пуриновых и пиримидиновых нуклеотидов, порфиринов, биогенных аминов и др.). Кетогенные аминокислоты, образующие в процессе обмена ацетоуксусную кислоту (ацетоацетил-КоА), могут непосредственно участвовать в синтезе жирных кислот и стеринов. Аналогично могут использоваться гликогенные аминокислоты через аце-тил-КоА, но после предварительного превращения в пируват. Некоторые структурные компоненты специализированных липидов, в частности фосфоглицеридов, имеют своим источником аминокислоты и их производные, например серии, этаноламин, сфингозин и холин. Необходимо подчеркнуть, что путь превращения углеродных скелетов кетогенных или гликогенных аминокислот в жирные кислоты является необратимым процессом, хотя нельзя исключить возможности частичного синтеза глутамата и опосредованно других аминокислот из продуктов распада жирных кислот — ацетил-КоА — через цикл трикарбоновых кислот, включающий ос-кетоглутарат.
В то же время из глицерина нейтральных жиров через пируват полностью осуществляется синтез углеродных скелетов некоторых гликогенных аминокислот.
Продукты гидролиза пищевых и тканевых триглицеридов, в частности высшие ^ жирные кислоты, участвуют непосредственно в образовании сложных белков — липопротеинов плазмы крови. В составе липопротеинов, являющихся, таким образом, транспортной формой жирных кислот, они доставляются в органы-мишени, в которых жирные кислоты служат или источником энергии (сердечная и поперечнополосатая мускулатура), или предшественниками синтеза тканевых триглицеридов с последующим их отложением в органах (депо липидов).
Получены доказательства синтеза глюкозы из большинства аминокислот. В некоторых случаях (аланин, аспарагиновая и глутаминовая кислоты) эта связь является непосредственной, в других — осуществляется через побочные каналы. Следует особо подчеркнуть, что три а-кетокислоты (пируват, оксалоацетат и кетоглутарат), образующиеся соответственно из аланина, аспартата и глутамата, не только служат исходным материалом для синтеза глюкозы, но и являются своеобразными катализаторами в превращении ацетильных остатков всех классов пищевых веществ в цикле Кребса для получения энергии.
Синтез незаменимых аминокислот из продуктов обмена углеводов и жиров в организме не происходит. Клетки животных не содержат ферментных систем, катализирующих синтез углеродных скелетов этих аминокислот. Этим объясняется незаменимость белков в питании для человека и животных. В то же время организм может нормально развиваться исключительно при белковом питании, что также свидетельствует о возможности синтеза углеводов из белков. Процесс синтеза углеводов из аминокислот получил название глюконеогенеза, который доказан прямым путем в опытах на животных с экспериментальным диабетом, когда более 50% введенного белка превращается в глюкозу. Как известно, при диабете организм теряет способность утилизировать глюкозу и энергетические потребности покрываются за счет окисления аминокислот и жирных кислот. Доказано также, что исходными субстратами для глюконеогенеза являются те аминокислоты, распад которых сопровождается образованием прямо или опосредованно пировиноградной кислоты (например, аланин, серии, треонин и цистеин). Более того, имеются доказательства существования в организме своеобразного циклического процесса, названного глюкозо-аланиновым циклом, участвующего в тонкой регуляции концентрации глюкозы в крови в тех условиях, когда в период между приемами пищи организм испытывает дефицит глюкозы; источниками пирувата при этом являются указанные выше аминокислоты, образующиеся в мышцах при распаде белков и поступающие в печень, в которой они подвергаются дезаминированию; образовавшийся аммиак там же обезвреживается, участвуя в синтезе мочевины, которая выделяется из организма. Дефицит мышечных белков затем восполняется за счет поступления аминокислот пищи.
Энергетическая ценность пищи оказывает определенное влияние на белковый обмен, контролируемый азотистым балансом. Так, если потребляемая энергия пищи ниже минимального уровня, то наблюдается увеличение экскреции азота, и, наоборот, при увеличении энергетической ценности пищи экскреция азота с мочой снижается. Энергетическая ценность пищи, следовательно, является лимитирующим фактором в утилизации пищевых белков.
Из приведенной выше схемы видно также, что имеются различные пути взаимопревращений жиров и углеводов. Практика откорма сельскохозяйственных животных давно подтвердила возможность синтеза жиров из углеводов пищи. С энергетической точки зрения превращение углеводов в жиры следует рассматривать как накопление и депонирование энергии, хотя синтез жира сопровождается затратой энергии, которая вновь освобождается при окислении жиров в организме. Глицерин, входящий в состав триглицеридов и фосфоглицеридов, может легко образоваться из промежуточных метаболитов гликолиза, в частности из глицеральдегид-3-фосфата.
Следует, однако, подчеркнуть, что основным путем превращения углеводов в жиры является путь образования высших жирных кислот из ацетил-КоА, который образуется при окислительном декарбоксилировании пирувата. Последняя реакция практически необратима, поэтому образования углеводов из высших жирных кислот почти не происходит. Таким образом, синтез углеводов из жиров в принципе может происходить только из глицерина, хотя в обычных условиях реакция протекает в обратную сторону, т. е. в сторону синтеза жиров из глицерина, образующегося при окислении углеводов.
Ацетил-КоА, образующийся в процессе обмена углеводов, жиров и ряда аминокислот, служит пусковым субстратом как для синтеза жирных кислот (а следовательно, и липидов вообще), так и для цикла трикарбоновых кислот. Для окисления ацетил-КоА в этом цикле требуется оксалоацетат, который является вторым ключевым субстратом в цикле Кребса. Оксалоацетат может синтезироваться из пировино-градной кислоты и углекислого газа благодаря реакции карбоксилирования или образоваться из аспарагиновой кислоты в процессе трансаминирования. Две молекулы ацетил-КоА, конденсируясь, образуют ацетоуксусную кислоту (ацетоацетат), которая является источником других кетоновых тел в организме, в частности (3-оксимасляной кислоты (Р-оксибутирата) и ацетона (см. главу 10). Следует подчеркнуть, что ацетоуксусная и (З-оксимасляная кислоты часто рассматриваются как транспортные формы активной уксусной кислоты, доставляющие ее для окисления в цикле Кребса в периферические ткани. Эти же реакции конденсации двух молекул ацетил-КоА составляют начальные этапы синтеза холестерина, в свою очередь являющегося предшественником гормонов стероидной природы, витамина D3, а также желчных кислот; последние в виде парных желчных кислот выполняют важную функцию эмульгаторов при переваривании липидов пищи в кишечнике и способствуют всасыванию высших жирных кислот.
Следует указать также на использование галактозы и частично глюкозы для биосинтеза цереброзидов и гликолипидов, выполняющих специфические функции в деятельности ЦНС. В этих синтезах участвуют не свободные моносахариды, а галактозамин и глюкозамин, биосинтез которых в свою очередь требует доставки амидного азота глутамина, интегрируя, таким образом, обмен углеводов, липидов и белков.
Перечисленными примерами абсолютно не исчерпывается все многообразие взаимопревращений органических веществ, которое постоянно совершается в живых организмах. Здесь были приведены лишь главные, магистральные каналы и пути превращения общих классов веществ и указаны ключевые субстраты и ферментные системы, обеспечивающие постоянство химических компонентов и тканей и динамичность живых структур.
Таким образом, скорости распада одних питательных веществ и биосинтеза других прежде всего определяются физиологическим состоянием и потребностями организма в энергии и метаболитах. Этими факторами в значительной степени может быть объяснено существование постоянного динамического состояния химических составных компонентов организма как единого целого.
Благодаря этой динамичности и координации метаболической активности обеспечивается макро- и микроскопическое постоянство всех форм живого. Выяснение фундаментальных проблем структуры и функций отдельных биомолекул может служить основой для раскрытия как молекулярных механизмов химических процессов, лежащих в основе состава и функций отдельных клеток и целостного организма, так и процессов, обеспечивающих биологическую индивидуальность живых организмов. Любые нарушения этого динамического статуса организма сопровождаются развитием патологии, тяжесть и продолжительность которой будет определяться степенью повреждения структуры и функций клеток.
Глава 15 ПЕЧЕНЬ
Важнейшее значение печени в обмене веществ в первую очередь определяется тем, что она является как бы большой промежуточной станцией между портальным и общим кругом кровообращения. Более 70 % крови в печень человека поступает через воротную вену, остальная часть крови попадает в печень через печеночную артерию. Кровь воротной вены омывает всасывающую поверхность кишечника, и в результате большая часть веществ, всасывающихся в кишечнике, проходит через печень (кроме липидов, транспорт которых в основном осуществляется через лимфатическую систему).
Таким образом, печень функционирует как первичный регулятор содержания в крови веществ, поступающих в организм с пищей. Доказательством справедливости данного положения является следующий общеизвестный факт: несмотря на то что всасывание питательных веществ из кишечника в кровь происходит прерывисто, непостоянно, в связи с чем в портальном круге кровообращения могут наблюдаться изменения концентрации ряда веществ (глюкоза, аминокислоты и др.), в общем же круге кровообращения изменения в концентрации указанных соединений незначительны. Все это подтверждает важную роль печени в поддержании постоянства внутренней среды организма. Печень выполняет также крайне важную экскреторную функцию, теснейшим образом связанную с ее детоксикационной функцией. В целом же без преувеличения можно сказать, что в организме нет путей
> обмена веществ, которые прямо или косвенно не контролировались бы печенью, в связи с чем многие важнейшие функции печени уже обсуждены в соответствующих
— главах учебника. Поэтому в данной главе будет сделана попытка дать обобщающие представления о роли печени в обмене веществ целостного организма.
ХИМИЧЕСКИЙ СОСТАВ ПЕЧЕНИ
У взрослого здорового человека масса печени составляет в среднем 1,5 кг. Некоторые исследователи считают, что эту величину следует рассматривать как нижнюю границу нормальной при диапазоне колебаний в пределах 20 — 60 г на 1 кг массы тела.
В табл. 15.1 представлены некоторые данные о химическом составе печени в норме.
| Таблица 15.1. Химический состав печени | млекопитающих | ||
| Составные части | Содержание, % | Составные части | Содержание, % |
| Вода Сухой остаток Белок Липиды Триацилглицеролы | 70-75 25-30 12-24 2-6 1,5-2,0 | Фосфолипиды Холестерин Гликоген Железо | 1,5-3,0 0,3-0,5 2-8 0,02 |
Из таблицы видно, что более 70 % от массы печени составляет вода. Однако следует помнить, что масса печени и ее состав подвержены значительным колебаниям как в норме, так и особенно при патологических состояниях. Например, при отеках количество воды может составлять до 80% от массы печени, а при избыточном отложении жира количество воды в печени может снизиться до 55%. Более половины сухого остатка печени приходится на долю белков, причем примерно 90% из них — на долю глобулинов. Печень также богата различными ферментами. Около 5% от массы печени составляют липиды: нейтральные жиры (триглицериды), фосфолипиды, холестерин и др. При выраженном ожирении содержание липидов может достигать 20 % от массы органа, а при жировом перерождении печени количество липидов в этом органе может составлять 50% от сырой массы.
В печени может содержаться 150 — 200 г гликогена. Как правило, при тяжелых паренхиматозных поражениях печени количество гликогена в ней уменьшается. Напротив, при некоторых гликогенозах содержание гликогена может достигать 20% и более от массы печени.
Разнообразен и минеральный состав печени. Количество железа, меди, марганца, никеля и некоторых других элементов превышает их содержание в других органах и тканях. Ниже будет рассмотрена роль печени в разных видах обмена веществ.
РОЛЬ ПЕЧЕНИ В УГЛЕВОДНОМ ОБМЕНЕ
Основная роль печени в углеводном обмене заключается в обеспечении постоянства концентрации глюкозы в крови. Это достигается регуляцией соотношения между синтезом и распадом гликогена, депонируемого в печени.
Синтез гликогена в печени и его регуляция в основном аналогичны тем процессам, которые протекают в других органах и тканях, в частности в мышечной ткани. Синтез гликогена из глюкозы обеспечивает в норме временный резерв углеводов, необходимый для поддержания концентрации глюкозы в крови в тех случаях, когда ее содержание значительно уменьшается (например, у человека это происходит при недостаточном поступлении углеводов с пищей или в период ночного «голодания»).
Говоря об утилизации глюкозы печенью, необходимо подчеркнуть важную роль фермента глюкокиназы в этом процессе. Глюкокиназа, подобно гексокиназе, катализирует фосфорилирование глюкозы с образованием глюкозо-6-фосфата (см. главу 9). При этом активность глюкокиназы в печени почти в 10 раз превышает активность гексокиназы. Важное различие между этими двумя ферментами заключается в том, что глюкокиназа в противоположность гексокиназе имеет высокое значение Кмдля глюкозы и не ингибируется глюкозо-6-фосфатом.
После приема пищи содержание глюкозы в воротной вене резко возрастает; в тех же пределах увеличивается и ее внутрипеченочная концентрация ‘. Повышение концентрации глюкозы в печени вызывает существенное увеличение активности глюкокиназы и автоматически увеличивает поглощение глюкозы печенью (образовавшийся глюкозо-6-фосфат либо затрачивается на синтез гликогена, либо расщепляется).
Считают, что основная роль печени — расщепление глюкозы — сводится прежде всего к запасанию метаболитов-предшественников, необходимых для биосинтеза жирных кислот и глицерина, и в меньшей степени к окислению ее до СО2 и Н2О. Синтезированные в печени триглицериды в норме выделяются в кровь в составе липопротеинов и транспортируются в жировую ткань для более «постоянного» хранения.
В реакциях пентозофосфатного пути в печени образуется НАДФН2, используемый для восстановительных реакций в процессах синтеза жирных кислот, холестерина и других стероидов. Кроме того, при этом образуются пентозофосфаты, необходимые для синтеза нуклеиновых кислот.
Наряду с утилизацией глюкозы в печени, естественно, происходит и ее образование. Непосредственным источником глюкозы в печени служит гликоген. Распад гликогена в печени в основном происходит фосфоролитическим путем. В регуляции скорости гликогенолиза в печени большое значение имеет система циклических нуклеотидов. Кроме того, глюкоза в печени образуется также в процессе глюконеогенеза.
Основными субстратами глюконеогенеза служат лактат, глицерин и аминокислоты. Принято считать, что почти все аминокислоты, за исключением лейцина, могут пополнять пул предшественников глюконеогенеза.
При оценке углеводной функции печени необходимо иметь в виду, что соотношение между процессами утилизации и образования глюкозы регулируется прежде всего нейрогуморальным путем при участии желез внутренней секреции.
Центральную роль в превращениях углеводов и саморегуляции углеводного обмена в печени играет глюкозо-6-фосфат. Он резко тормозит фосфоролитическое расщепление гликогена, активирует ферментативный перенос глюкозы с уридинди-фосфоглюкозы на молекулу синтезирующегося гликогена, является субстратом для дальнейших гликолитических превращений, а также окисления глюкозы, в том числе по пентозофосфатному пути. Наконец, расщепление глюкозо-6-фосфата фосфатазой обеспечивает поступление в кровь свободной глюкозы, доставляемой током крови во все органы и ткани:
Рассматривая промежуточный обмен углеводов в печени, необходимо также остановиться на превращениях фруктозы и галактозы. Поступающая в печень фруктоза может фосфорилироваться в положении 6 до фруктозо-6-фосфата под действием гексокиназы, обладающей относительной специфичностью и катализирующей фосфо-рилирование, кроме глюкозы и фруктозы, еще и маннозы. Однако в печени существует и другой путь: фруктоза способна фосфорилироваться при участии и более специфического фермента — фруктокиназы. В результате образуется фруктозо-1-фосфат. Эта реакция не блокируется глюкозой. Далее фруктозо-1-фосфат под действием альдолазы расщепляется на две триозы: диоксиацетонфосфат и глицеральдегид. Под влиянием соответствующей киназы (триокиназы) и при участии АТФ глицеральдегид подвергается фосфорилированию до глицеральдегид-3-фосфата. Образовавшийся глицеральдегид-3-фосфат (в последний легко переходит и диоксиацетонфосфат) подвергается обычным превращениям, в том числе с образованием в качестве промежуточного продукта пировиноградной кислоты.
Галактоза в печени сначала фосфорилируется при участии АТФ и фермента галактокиназы с образованием галактозо-1-фосфата. Галактокиназа печени плода И ребенка характеризуется Кыи Vmax, примерно в 5 раз превосходящими таковьв у ферментов взрослого человека. Большая часть галактозо-1-фосфата в печени превращается в ходе реакции, катализируемой гексозо-1 -фосфат-уридилилтранс* феразой:
УДФ-глюкоза + галактозо-1-фосфат -> УДФ-галактоза + глюкозо-1-фосфат
Эта уникальная трансферазная реакция возвращения галактозы в основное русло углеводного метаболизма. Наследственная утрата гексозо-1-фосфат-уридилилтранс-‘ феразы приводит к галактоземии — заболеванию, для которого характерны умственная отсталость и катаракта хрусталика. В этом случае печень новорожденных теряет способность метаболизировать D-галактозу, входящую в состав лактозы молока.
РОЛЬ ПЕЧЕНИ В ЛИПИДНОМ ОБМЕНЕ
Ферментативные системы печени способны катализировать все или подавляющее большинство реакций метаболизма липидов. Совокупность этих реакций лежит в основе таких процессов, как синтез высших жирных кислот, триглицеридов, фосфо-липидов, холестерина и его эфиров, а также липолиз триглицеридов, окисление жирных кислот, образование ацетоновых (кетоновых) тел и т. д.
Напомним, что ферментативные реакции синтеза триглицеридов в печени и жировой ткани сходны. А именно, КоА-производные жирной кислоты с длинной цепью взаимодействуют с глицерол-3-фосфатом с образованием фосфатидной кислоты, которая затем гидролизуется до диглицерида. Путем присоединения к последнему еще одной молекулы КоА-производного жирной кислоты образуется триглицерид. Синтезированные в печени триглицериды либо остаются в печени, либо секретируются в кровь в форме липопротеинов. Секреция происходит с известной задержкой (у человека 1 — 3 ч). Задержка секреции, вероятно, соответствует времени, необходимому для образования липопротеинов.
Как уже отмечалось, основным местом образования плазменных пре-|3-липопро-теинов (липопротеинов очень низкой плотности — ЛПОНП) и а-липопротеинов (липопротеинов высокой плотности — ЛПВП) является печень. К сожалению, пока нет точных данных о последовательности сборки липопротеиновых частиц в гепатоцитах, не говоря уже о механизмах этого процесса.
У человека основная масса (3-липопротеинов (липопротеинов низкой плотности — ЛПНП) образуется в плазме крови из ЛПОНП при действии липопротеинлипазы. В ходе этого процесса образуются сначала промежуточные короткоживущие липо-протеины (Пр.ЛП). Через стадию образования промежуточных липопротеинов формируются частицы, обедненные триглицеридами и обогащенные холестерином, т. е. образуются ЛПНП (рис. 15.1).
При высоком содержании жирных кислот в плазме их поглощение печенью возрастает, усиливается синтез триглицеридов, а также окисление жирных кислот, что может привести к повышенному образованию кетоновых тел.
Следует подчеркнуть, что кетоновые тела образуются в печени в ходе так называемого Р-окси-Р-метилглутарил-КоА пути. Как уже отмечалось» прежние представления о том, что кетоновые тела являются промежуточными продуктами окисления жирных кислот в печени, оказались ошибочными. Из печени кетоновые тела током крови доставляются в ткани и органы (мышцы, почки, мозг и др.), где они быстро окисляются при участии соответствующих ферментов. В самой же ткани печени кетоновые тела не окисляются, т. е. в этом плане по сравнению с другими тканями печень является исключением.
В печени происходит как интенсивный распад фосфолипидов, так и их синтез. Помимо глицерина и жирных кислот, которые входят в состав нейтральных жиров, для синтеза фосфолипидов необходимы неорганические фосфаты и азотистые основания, в частности холин для синтеза фос-фатидилхолина. Неорганические фосфаты в печени имеются в достаточном количестве. Другое дело — холин. При недостаточном образовании или недостаточном поступлении его в печень синтез фосфолипидов из компонентов нейтрального жира становится либо невозможным, либо резко снижается, и нейтральный жир откладывается в печени. В этом случае говорят о жировой инфильтрации печени, которая может затем перейти в ее жировую дистрофию. Иными словами, синтез фосфолипидов лимитируется количеством/ азотистых
оснований, т. е. для синтеза фосфоглицеридов необходимы либо холин, либо соединения, которые могут являться донорами метальных групп и участвовать в образовании холина (например, метионин). Последние соединения получили название липотропных веществ. Отсюда становится ясным, почему при жировой инфильтрации печени весьма полезен творог, содержащий белок казеин, в составе которого имеется большое количество остатков аминокислоты метионина.
Рассмотрим роль печени в обмене стероидов, в частности холестерина. Часть холестерина поступает в организм с пищей, но значительно большее количество его синтезируется в печени из ацетил-КоА. Биосинтез холестерина в печени подавляется экзогенным холестерином, т. е. получаемым с пищей.
Таким образом, биосинтез холестерина в печени регулируется по принципу отрицательной обратной связи. Чем больше холестерина поступает с пищей, тем меньше его синтезируется в печени, и наоборот. Принято считать, что действие экзогенного холестерина на биосинтез его в печени связано с торможением (3-окси-Р-метилглутарил-КоА-редуктазной реакции:
Часть синтезированного в печени холестерина выделяется из организма совместно с желчью, другая часть превращается в желчные кислоты и используется в других органах для синтеза стероидных гормонов и других соединений.
В печени холестерин может взаимодействовать с жирными кислотами (в виде ацил-КоА) с образованием эфиров холестерина. Синтезированные в печени эфиры холестерина поступают в кровь, в которой содержится также определенное количество свободного холестерина.
Дата добавления: 2014-12-27 ; Просмотров: 858 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
- http://studfiles.net/preview/5920457/page:8/
- http://files.school-collection.edu.ru/dlrstore/53099f45-b86e-7b05-4591-a69c5bee0bb7/1000346A.htm
- http://studopedia.su/14_90611_regulyatsiya-sinteza-belka.html