О том, как появилось мыло, существует множество различных легенд. Пользовались им люди ещё около шести тысяч лет назад. Тогда оно изготавливалось из жиров растений и животных. За многие века его состав, конечно же, постоянно менялся. А часто задаваемый вопрос о том, почему мыло моет, не исчез.
Основная функция продукта заключается в очищении различных поверхностей от грязи. И он отлично с этим справляется. Так всё-таки, почему мыло моет? Попробуем разобраться.
Давайте разберемся. Итак, почему мыло моет? Секрет его, как и прочих моющих средств, которые относятся к поверхностно-активным веществам, заключается в уменьшении поверхностного натяжения воды. Это и усиливает её моющие свойства. Состоит мыльная пена из огромного количества мыльных пузырьков с водяной оболочкой. К этим самым пузырькам прилипают частички сажи, пыли и грязи. А пена под струёй воды очень легко смывается.
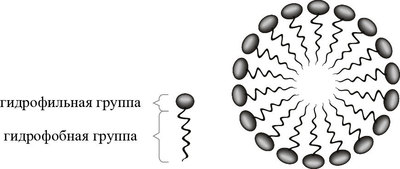
Поверхностно-активные вещества (точнее, их молекулы) расположены на пограничной поверхности так, что гидрофильные группы направляются прямо в воду, а гидрофобные – напротив, выталкиваются из неё. Таким образом, поверхность воды покрывается своеобразным забором, состоящим из вышеуказанных молекул.
Такая водная поверхность отличается меньшим поверхностным натяжением. Это, в свою очередь, помогает полному и быстрому смачиванию загрязнённых поверхностей. Покрытая поверхностно-активными веществами частица легко отделяется от ткани и уходит в раствор.
В общем, мыльные частицы имеют обволакивающие свойства, которые приводят к образованию эмульсий разнообразных загрязняющих веществ и препятствуют их осаждению на поверхности повторно. Они и удерживают нерастворимые частицы в суспензии. Потому они так легко удаляются при помощи воды.
Отличный эффект при невысокой стоимости
Впрочем, для большинства людей не так уж и важно, почему мыло моет. Главное, что человек привык к чистоплотности и аккуратности. В принципе, для того чтобы избавиться от грязи, ему достаточно самого обыкновенного мыла. Достигая прекрасного эффекта при невысокой стоимости, конечно же, таким продуктом можно оставаться довольным. Действие, как уже упоминалось выше, основано на понижении поверхностного натяжения воды и усилении моющего средства.
Дело в составе
Обратим внимание ещё на один момент. На вопрос о том, почему мыло моет руки, прямой ответ может дать его состав. Дело в том, что в него входит стеарат натрия – вещество, способное растворять кожное сало, которое образуется на поверхности кожи. Кроме того, смывается прилипшая грязь. Чем больше щелочной реакции происходит, тем лучше грязь удаляется. Хотя из-за щелочи кожа заметно высыхает. Потому производителями и добавляются в мыло всевозможные добавки, смягчающие его, придающие ему цвет и запах. Вспомните, к примеру, о глицерине. Он позволяет достичь смягчающего эффекта. Некоторые другие добавки, вообще, позволяют мылу стать лечебным. На сегодняшний день выбор достаточно велик – выбрать без особого труда можно именно то, что вам нужно.
Лучше других веществ
И напоследок. Почему мыло лучше прочих моющих веществ? Возьмите в руки простую сажу. Попробуйте её отмыть. Не получится. Добавьте мыла – руки сразу же станут чистыми. Секрет кроется в мыльной пене. Точнее, в её маленьких, юрких пузырьках. В состав мыла входит натуральный жир и каустическая сода. Соединяясь, они создают мыльную массу, содержащую большое количество пузырьков, к которым прилипают частички грязи и смываются водой.
В общем, мыло моет руки и различные поверхности намного лучше, чем это делают другие средства. Его состав и свойства позволяют справляться со всевозможными загрязнениями без особого труда. При этом насчёт больших затрат вы можете нисколько не беспокоиться.
Популярная химия
Главное меню
Существует множество легенд, рассказывающих о том, как появилось мыло. Известно, что ещё шесть тысяч лет назад люди пользовались мылом, сделанным из животных жиров и растений. Для получения мыла смешивали животные жиры с золой. Конечно, за многие века состав мыла изменился значительно. Но основная функция мыла – очищать поверхность от грязи, осталась неизменной.
Точная дата появления мыла учёными не установлена. Но с тем, что мыло появилось очень давно, согласятся все.
Химический состав мыла
Прообразом современного мыла стал пепел вместе с жиром. При смешивании этих двух компонентов происходит химическая реакция, которая составляет основу мыловарения. В результате такой реакции и получают мыло. В современном мыловаренном производстве жир заменяют натуральными маслами, а золу – каустической содой. Соединяясь, масла и сода образуют массу, которая содержит большое количество пузырьков. Оболочка каждого пузырька состоит из воды. Частички грязи прилипают к пузырькам и легко смываются водой.
Химическую реакцию между золой или содой и жиром называют реакцией омыления. В основе мыловарения эта реакция лежит и в наше время. А химический состав мыла впервые был установлен французским химиком Мишелем Эженом Шеврёлем. Оказывается, мыло — это натриевая соль высшей жирной (карбоновой) кислоты.
Каждый из нас в детстве знал, что мыть руки с мылом необходимо для того, чтобы убить бактерии. Но оказывается, мыло не убивает бактерии, а только отделяет их от кожи рук. И они легко смываются водой. Мыло растворяет все вещества, налипшие на кожу.
Какие же процессы происходят при этом?
В состав современного натурального мыла входят натриевые и калиевые соли высших жирных кислот — пальмитиновой С15Н31-СООNа и стеариновой С17Н35-СООNа. Основой твёрдого мыла являются натриевые соли высших карбоновых кислот, а основой жидкого – калиевые соли этих кислот. Но так как производство натурального мыла требует большого количества натурального сырья, то это сырьё впоследствии успешно заменили поверхностно-активными веществами, получаемыми при переработке нефтепродуктов и угля. Так получили синтетическое мыло и различные современные моющие средства.
Физика и химия моечного процесса
Как же всё-таки мыло моет?
Моечный процесс довольно сложен как с физической, так и с химической точек зрения.
Химическая формула молекулы мыла СН3—(CH2)n—COONa. Известно, что гидрофильность – это способность вещества взаимодействовать с водой на молекулярном уровне. А гидрофобные вещества – это вещества, которые не могут взаимодействовать с водой. Так вот, группа COONa и обеспечивает гидрофильность молекулы мыла. Благодаря этой группе, мыло способно растворяться в воде. А СН3—(CH2)n – длинный углеводородистый радикал, который гидрофобен. В состав этого радикала могут входить до 12 атомов углерода.
Мыло, как и другие моющие средства, уменьшает поверхностное напряжение воды, улучшая доступ молекул мыла к поверхности, которая моется. Во время процесса мытья при контакте с водой на поверхности образуются мыльные пузырьки. Молекулы мыла ориентируются так, что гидрофильные группы COONa + направлены к полярным молекулам воды, то есть внутрь. Они остаются в воде. А гидрофобные СН3—(CH2)n направлены наверх, к неполярным частицам грязи. Грязь содержит жир. А жир – это соединение глицерина с теми же жирными кислотами. СН3—(CH2)n образует с частицами жира суспензию, которая легко удаляется вместе с водой.
По такому же сценарию действуют практически все моющие средства, в основе которых лежат поверхностно-активные вещества.
Проект «Почему Мыло моет»
Приводится проект по химии 8 класс «Почему мыло моет?»
| Вложение | Размер |
|---|---|
| mylo_itog.docx | 847.41 КБ |
Предварительный просмотр:
1. Актуальность темы. Цели и задачи………………………………………. …….2
3. История создания мыла. Эволюция мыловарения…………………….……..…3
5. Состав мыла. Почему мыло моет…………………………………………..……7
6. Химия и физика моечного процесса……………………………………….…. 10
7. Изготовление мыла своими руками…………………………………….………12
9. Процесс производства мыла…………………………………………….………18
11. Интересные факты о мыле……………………………………………….…….21
13. Список используемой литературы……………………………………. …..23
Актуальность темы. Цели и задачи.
Актуальность моей работы определена тем, что мыло — первое гигиеническое средство, с которым встречается каждый человек после рождения. По нескольку раз в день мы пользуется мылом и даже не задумывается о том, как и когда оно появилось на свет. В настоящее время, разглядывая витрины магазинов, можно убедиться в богатом выборе мыла.
Не многие продукты столь же популярны и широко используются в быту, как мыло. Очень актуально стало делать мыло своими руками в подарок. Мыло пришло к нам из далекой древности и постепенно из роскоши превратилось в предмет первой необходимости.
Меня заинтересовало, чем же пользовались люди до изобретения мыла. Когда его изобрели? Из чего оно состоит? Какое мыло полезнее для кожи, а какое вреднее? Где еще можно применять мыло?
И я решила рассмотреть эти вопросы…
Цели и задачи работы:
- Познакомиться с мылом. Узнать историю появления мыла
- Изучить свойства и функции мыла, его состав
- Исследовать способы изготовления мыла в домашних условиях
- Изготовить мыло своими руками
- Провести опыт по определению водородных показателей нескольких образцов мыла. Разобраться, какое мыло лучше подходит для ребенка, а какое для взрослого человека
- Провести опыт и узнать, в какой воде мыло лучше пенится
- Узнать, где можно применять мыло в промышленности.
Задавая себе вопрос, без чего люди не сумеют обойтись, многие согласятся со мной: без средств гигиены. Никой кризис не заставит нас не принимать душ или ванну. Ну и, конечно же, лучший способ уберечься от бактерий и вирусов – регулярно мыть руки с мылом. На протяжении последних ста лет мыло неизменно считается лучшим средством в борьбе с заболеваниями.
В течение дня мы прикасаемся руками к различным предметам, некоторые из которых чистые, а другие не очень. После каждого прикосновения на руках остаются миллионы микробов, которые цепляются за жир, вырабатываемый нашими сальными железами. Если вовремя не удалить микробы, существует вероятность, что мы, например, вместе с приемом пищи, занесем их внутрь организма. Оказавшись в комфортных для себя условиях, микробы начнут размножаться и вызовут заболевание.
Каждый из нас с детства знает, что мыть руки с мылом необходимо для того, чтобы убить бактерии. Но оказывается, мыло не убивает бактерии, а только отделяет их от кожи рук. И они легко смываются водой. Мыло растворяет все вещества, налипшие на кожу. Какие же процессы происходят при этом? Из чего состоит мыло и почему оно моет? Эти вопросы я и решила изучить.
История создания мыла. Эволюция мыловарения.
История мыла насчитывает около 6 тысяч лет, но даже до его появления люди пытались очищать свое тело с помощью различных средств. Например, древние греки времен Гомера обтирали тело мелким песком, привезенным с берегов Нила, а древние египтяне умывались растворенным в воде пчелиным воском. Дикие галльские племена делали из золы букового дерева и сала специальную мазь, а скифы растирали в порошок древесину кипариса и кедра, добавляя к нему воду и ладан, натирая этой смесью тело и соскребая ее вместе с грязью.
О том же, где появилось первое мыло, и какой народ стал родоначальником мыловарения, ученые спорят до сих пор, склоняясь к совершенно разным и одинаково правдоподобным версиям.
По одной из версий, первое мыло было изобретено в Шумере – древнейшей цивилизации, существовавшей IV-III тысячелетиях до нашей эры. В частности, археологами были обнаружены древние шумерские таблички, датированные около 2500 г. до н. э., на которых был описан процесс, очень похожий на изготовление мыла: смешанную с водой древесную золу кипятили, а затем растапливали в ней жир. Однако в табличках не говорится, как назывался этот раствор и, самое главное, для чего он применялся.
Вторая версия гласит, что история мыловарения началась в Древнем Египте еще около 6000 лет назад. Это теория подтверждается древними папирусами, в которых описано, что мыло получалось из животных и растительных жиров, нагретых вместе с щелочными солями и содой.
Но какая бы из версий ни была правильной, первое мыло в более или менее современном значении этого слова появилось в Древнем Риме. По легенде, даже латинское слово «sapo» («мыло») происходит от названия горы Сапо в Древнем Риме, на которой совершались жертвоприношения. При сжигании жертвы выделялся жир, который смешивался с золой от костров. Во время дождя эта масса стекала в Тибр, и жители, стиравшие в реке белье, в итоге заметили, что благодаря ей все отстирывается намного лучше. Собственно, от слова «sapo» и произошли английское слово «soap», итальянское «sapone» и французское «savon».
Средневековье и мыло.
С наступлением в Европе Средневековья чистоте и личной гигиене совершенно перестали уделять должное внимание. Мыло было достаточно ценным товаром, который был доступен только двум высшим сословиям: дворянству и духовенству. Даже королева Испании Изабелла Кастильская созналась, что мылом она пользовалась всего дважды в жизни: при рождении и перед свадьбой.
Производство мыла развилось в Англии: здесь находилось несколько крупных мыловарен, и отношение к этому ремеслу было очень серьезным. Именно в Англии был выдан первый патент на производство мыла – это произошло в 1662 году.
Также одним из основных центров мыловарения стал французский Марсель благодаря доступу к такому сырью для мыловарения, как оливковое масло и сода. А душистые масла для мыла доставлялись из Прованса. Также мыловарение стало активно развиваться в Греции, Испании и Италии.
Действительно улучшилась техника мыловарения, и началось повсеместное строительство мыловаренных заводов только в XVII веке.
Лишь на рубеже XVIII и XIX вв. была выяснена химическая природа жиров и внесена ясность в реакцию их омыления. В 1779 г. шведский химик Шееле показал, что при взаимодействии оливкового масла с оксидом свинца и водой образуется сладкое и растворимое в воде вещество. Решающий шаг на пути изучения химической природы жиров был сделан французским химиком Шеврелем. Он открыл стеариновую, пальмитиновую и олеиновую кислоты, как продукты разложения жиров при их омылении водой и щелочами. Сладкое вещество, полученное Шееле, было Шеврелем названо глицерином. Сорок лет спустя Бертло установил природу глицерина и объяснил химическое строение жиров.
Естественно, эволюция мыловарения на этом не остановилась: развивались технологии производства, улучшалось оборудование, добавлялись новые ингредиенты.
Мыловарение в России.
Несмотря на то, что европейские страны в основном заимствовали друг у друга способы мыловарения, в России оно развивалось своим, отдельным путем. Изначально это ремесло даже называлось не «мыловарение», а «поташное дело» — по названию вещества, которое играло роль своеобразного мыла. Производство заключалось в том, что срубленные деревья сжигали в огромных котлах прямо в лесу, а получившуюся золу заваривали, делали из нее щелок, из которого при выпаривании получали этот самый поташ.
Поташное дело очень быстро стало невероятно популярным и прибыльным ремеслом: он стал одним из основных экспортных продуктов, им занимались целые деревни. Но такая популярность поташа повлекла за собой массовую вырубку лесов, которая приостановилась только после изобретения французом Николасом Лебланом заводского способа получения соды из соли – нового и более дешевого щелочного материала для производства мыла.
На промышленный уровень мыловарение в России вышло при Петре І, который даже приказал выращивать на полях растения, входящие в состав мыла. А вот первые настоящие мыловаренные фабрики появились в России только в XVIII веке. При этом в косметических и гигиенических целях мыло было доступно только дворянам — крестьяне же по-прежнему стирали и мылись с помощью щелока.
Французский парфюмер Анри Брокар одним из первых открыл в России филиал французского парфюмерного производства. Талантливый парфюмер превратил свое скромное производство в целую фабрику. Причем популярность Брокара была связана не только с выпускаемой им парфюмерией, но и с выпуском «народного» мыла для всех слоев населения стоимостью в 1 копейку. Еще одной находкой Брокара стал интересный внешний вид мыла — так, например, у него производилось мыло «Огурец», которое действительно выглядело, как настоящий одноименный овощ
В 1839 году император Николай I повелел учредить Общество для выделки стеариновых свечей, олеина и мыла. Производство началось в том же году Санкт-петербургским Невским заводом. А в 1840 году начинает выпускаться знаменитая и очень популярная в дореволюционной России косметическая линия «Невская косметика». Но основной упор в производстве все же делался на мыловарение. Оборудование постоянно менялось, использовалась только самая современная техника и технологии мыловарения, за качеством выпускаемого мыла очень строго следили.
Также одним из самых старых российских предприятий, которое пережило и революцию, и перестройку, является Нижегородский масложировой комбинат, на котором производят мыло с 1905 года. Особенно знаменит этот комбинат своим хозяйственным мылом. Еще одним таким предприятием является воронежский мыловаренный завод «Финист», который был основан в 1891 году и действует до сих пор, выпуская около 150 наименований туалетного и хозяйственного мыла. Кстати, «Финист» является единственной в России мыловарней в чистом виде — остальные отечественные производители мыла являются либо масложировыми, либо парфюмерно-косметическими предприятиями.
Состав мыла. Почему мыло моет.
Как мы уже говорили, ранее, обязательным ингредиентом древнего мыла была обычная зола. Химическая реакция, которая происходит между жиром и золой, составляет основу мыловарения. Называется она омылением. Соединяясь, эти вещества создают большое количество пузырьков, свойства которых позволяют удалять грязь.
Конечно, сегодня в мыловарении больше не используются пепел и животный жир. Их заменили натуральные масла и каустическая сода. Само мыло по своему химическому составу является натриевой или калиевой солью высших жирных (карбоновых) кислот, гидролизующихся в водном растворе с образованием кислоты и щелочи.
Современная индустрия использует соли высших жирных кислот – стеариновой и пальмитиновой. Для производства твердого мыла используются натриевые соли этих кислот, а для жидкого – калиевые. Сегодня натуральное сырье не может полностью удовлетворить запросы мыловаренной промышленности, поэтому используются поверхностно-активные вещества (ПАВ), которые получают при переработке угля и нефтепродуктов.
Настоящее же мыло сделано из натуральных масел (таких как, оливковое, кокосовое или пальмовое), оно больше подходит для использования на коже.
Масла в мыло добавляются с определенной целью. Кокосовое масло делает восхитительную пену. Оливковое масло используется для изготовления высококачественного мыла. Масло канола (растительное масло из особого сорта рапса, выведенного в Канаде; в отличие от традиционного рапсового масла имеет низкое содержание вредных для организма веществ и употребляется в пищу), а также пальмовое масло снабжают кожу питательными веществами, подсолнечное масло используется для создания крем-мыла.
Глицерин — это успокаивающее и смягчающее кожу средство, которое делает мыло более полезным. Глицерин очень важен при уходе за кожей, потому что это увлажнитель. Увлажнители впитывают влагу из воздуха, которая в свою очередь увлажняет вашу кожу. Кусок мыла на 1/5 состоит из глицерина.
Чаще всего мыло состоит из искусственных ингредиентов, которые дают определенный запах или цвет.
Некоторые виды мыла содержат ароматические масла. Это синтетические химикаты, которые смешивают для имитации определенного аромата. В некоторых случаях они могут оказывать воздействие на химическую чувствительность людей. Запахи в мыле должны происходить только от эфирных масел, которые по особой технологии выпариваются или выжимаются из растений. Эфирные масла — это компоненты растений, испускающие аромат, они являются основой ароматерапии. Они не только дают приятный запах, но и оказывают благотворное влияние на тело, разум и дух.
Цвет мыла также должен быть природным. Лепестки лаванды и розы могут быть использованы с этой целью. Может быть применен природный пигмент, который, в отличие от искусственных красителей, делает цвет насыщенным и натуральным.
Так почему же всё-таки мыло моет? Попробуйте взять жирную тарелку и вымыть ее под струей холодной воды. Можно с полной уверенностью заявить, что ничего у вас из этой затеи не выйдет. Удалить липкую маслянистую пленку получится только, если добавить к воде немного мыла. Само состоящее из разновидности жира оно удивительным образом растворяет любую грязь и делает предметы сверкающе-чистыми.
Мыло обладает одним очень важным качеством, а именно – оно способно значительно сокращать поверхностное натяжение воды, и тем самым существенно увеличивать ее моющие свойства. Мыльная пена состоит из огромного количества мелких пузырьков, каждый их которых обладает водной оболочкой. Именно эти пузырьки и являются основным секретом моющих способностей мыла.
Законы физики и химии, обеспечивающие существование пузырька, придают ему уникальные физические свойства. Потому что пузырек обманывает наш взгляд. Например, кажется, что он круглый, как шар (что действительно так, когда он один), но в большинстве случаев – а именно в пене – он предпочитает принимать форму кубика. За тонкой и хрупкой внешностью пузырек прячет целые сокровища. Он – один из волшебников так называемой мягкой материи, одновременно прочной и текучей: он образует пену, которая способна сохранять свою форму в пространстве, но может и течь, когда это от нее требуется.
Пузырьки уменьшают поверхностное натяжение воды, но при этом усиливаются ее собственные моющие свойства. К пузырькам прилипают мелкие частички сажи, пыли и жира, а сама пена без труда смывается струей воды.
При этом современные поверхностно-активные вещества, используемые для мыловарения, имеют такой молекулярный состав, который максимально эффективно взаимодействует с водой. Поверхностное натяжение воды уменьшается за счет того, что тончайшая мыльная «пленка» покрывает практически всю ее поверхность.
Химия и физика моечного процесса
Мыло относится к категории так называемых тензидов, и, как и многие другие вещества, состоит из множества мельчайших частичек – молекул. Молекулы тензидов обладают одной замечательной особенностью. Одна сторона молекулы способна притягивать воду, другая наоборот ее отталкивает. Ученые называют их соответственно гидрофилами и гидрофобами.
Гидрофобы в свою очередь способны притягивать к себе частички жира. В присутствии воды все эти молекулы окунаются в воду и, прижимаясь друг к другу, образуют тонкую гибкую пленку, способную закрываться и удерживать воздух либо другие тела.
Когда кусок мыла трут влажными руками, образуется эмульсия между водой, мыльными молекулами и частичками грязи. Для молекул это желанная добыча. Они тут же нападают на эти частички и окружают их. Таким образом, образуется пузырьки трех видов: «чистые» (содержащие только воздух), «менее чистые» (содержащие воздух и небольшое количество грязи) и «грязные» (в которых много грязи и мало воздуха). «Менее чистые» пузырьки не так стойки, как «чистые», и живут недолго, тогда как «грязные» пузырьки очень малы по размеру и незаметны. Поэтому при равном количестве мыла чистая вода дает более устойчивую и обильную пену, чем грязная вода.
Образовавшаяся щелочь эмульгирует, частично разлагает жиры и освобождает таким образом прилипшую к поверхности грязь. Карбоновые кислоты с водой образуют пену, которая захватывает частицы грязи. Калиевые соли по сравнению с натриевыми лучше растворимы в воде и поэтому обладают более сильным моющим свойством.
Гидрофобная часть мыла проникает в гидрофобное загрязняющее вещество, в результате поверхность каждой частицы загрязнения оказывается окруженной оболочкой гидрофильных групп. Они взаимодействуют с полярными молекулами воды. Благодаря этому ионы моющего средства вместе с загрязнением отрываются от поверхности и переходят в водную среду. Так происходит очистка загрязненной поверхности моющим веществом.
Изготовление мыла своими руками
Для изготовления мыла мне понадобилось:
— ароматизаторы и косметические отдушки,
— косметические и эфирные масла,
— силиконовые и пластмассовые формы,
— посуда и прочие вспомогательные инструменты.
Для изготовления этого мыла я взяла: краситель красного цвета, ароматизатор «Сирень», диоксид титана (для белого цвета), прямоугольная форма и форма «Бабочка».
1. Нарезаем и плавим прозрачную мыльную основу.
2. Разливаем жидкую мыльную основу пополам в два стакана. В один стакан добавляем диоксид титана, а в другой — красный краситель.
3. Добавляем ароматизатор «Сирень».
4. Сбрызгиваем форму спиртом и заливаем в нее мыльную основу двух цветов.
5. Деревянной палочкой делаем узор на мыле, смешивая красную и белую основу.
6. Из оставшейся красной основы делаем бабочку и приклеиваем ее к нашему мылу при помощи расплавленной основы.
7. Даем изделию полностью остыть и можем использовать по назначению.
См. фото — Приложение 1.
Для этого мыла я использовала краситель коричневого цвета, ароматизатор «Горячий шоколад», молотый кофе и форму в виде ракушки.
- Нарезаем и плавим непрозрачную мыльную основу.
- Разливаем жидкую мыльную основу пополам в два стакана.
3. В один стакан с мыльной основой добавляем коричневый краситель и молотый кофе.
3. Добавляем ароматизатор «Горячий шоколад».
4. Сбрызгиваем форму спиртом и заливаем туда мыльную основу, чередуя слои белого и коричневого цвета.
5. Даем изделию полностью остыть.
См. фото — Приложение 2.
Проведенные мною опыты
В ходе исследования своей темы я проделала три опыта:
1. Определение водородного показателя
2. Какое мыло лучше пенится
3. Отношение видов мыла к агрессивным средам
Для моего опыта я взяла шесть видов мыла: глицериновое, жидкое, мыло ручной работы, Dove, детское кусковое и детское жидкое. С каждым из видов я сделала мыльный раствор. Во все колбы я опустила индикатор, определяющий водородные показатели. После окрашивания индикаторов, я сверяла цвета с эталонной шкалой PH.
От 1 до 4 – кислая среда
5,6 – слабокислая среда
7 – нейтральная среда
От 8 до 12 – щелочная среда
При исследовании кислотности среды растворов мыл было установлено :
Почему моет мыло с точки зрения физики
Физика стирки и чистки: как моет мыло
Что такое «вымыть руки»? Если бы всё, что нас окружает, растворялось в воде (как, например, поваренная соль), то вымыть руки было бы очень легко – опустить их в воду и подождать чуть-чуть. К сожалению, большая часть веществ, к которым мы прикасаемся, нерастворимы в воде, и поэтому, если они прилипают к рукам или одежде, то одна вода не позволяет нам избавиться от этой грязи и пятен. Однако можно заставить любое вещество хотя бы через короткое время (несколько секунд) раствориться в воде, образовав эмульсию или суспензию – взвесь мельчайших частичек жидкого (или твёрдого) вещества в воде. Этого времени часто бывает достаточно для того, чтобы поток чистой воды смыл эмульгированную грязь, сделав руки чистыми. Мыло и служит прекрасным эмульгатором – химическим соединением, облегчающим получение водных эмульсий частичек самых различных веществ.
Почему мыло плохо стирает в морской воде? Морская вода характеризуется высоким содержанием двухвалентных катионов – Ca2+ и Mg2+. Эти катионы связываются с отрицательно заряженными головками мыльных молекул, мешая им образовать мицеллы вокруг частичек грязи и жира. Поэтому поверхностное натяжение мыльного раствора в морской воде увеличивается, что снижает качество стирки. То же происходит, когда в водопроводной воде высока концентрация двухвалентных ионов, например, железа. Такую воду называют «жёсткой», и мыло в ней стирает плохо.
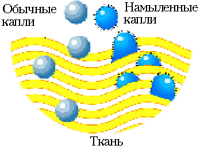
Почему полоскать надо в холодной воде? Цель полоскания – убрать остатки мыла из выстиранной ткани. При стирке мы нагреваем воду, чтобы понизить поверхностное натяжение воды, поэтому мыльный раствор залезает в самые тонкие промежутки между волокнами ткани. Чтобы он вылез оттуда, необходимо повысить поверхностное натяжение, и тогда каждой из сплющенных капелек опять станет выгодно стать шарообразной, и они выскочат из тонких промежутков между нитями. Поэтому полоскать ткань после стирки следует в холодной воде, когда её поверхностное натяжение велико.
Надо ли использовать антибактериальное мыло? Мыльные молекулы обволакивают бактерии, как и частички прилипшей к коже грязи. Поэтому в мыльном растворе скоро оказывается большинство бактерий. Учёные доказали, что обычное мыло ничуть не хуже борется с бактериями, чем разрекламированное повсюду антибактериальное. В отличие от обычного антибактериальное мыло содержит химические препараты (антибиотики), убивающие бактерий. Однако именно это и является недостатком антибактериального мыла. Дело в том, что антибиотик не в состоянии убить абсолютно все бактерии, а оставшиеся в живых «супербактерии» обладают необычайно высокой стойкостью по отношению к данному антибиотику. Они начинают размножаться, и скоро на нашей коже появляется столько же бактерий, сколько было до мытья, но все эти бактерии являются «детками» супербактерий, поэтому многие их них переняли от своих родителей нечувствительность к действию этого антибиотика. В результате антибактериальное мыло скоро становится бесполезным, а супербактерии с кожи распространяются по всему организму, и бороться с ними нужно уже с помощью другого, более мощного антибиотика. В общем, «хотели, как лучше, а получилось…».
Что такое отбеливатель? В моющих средствах для стирки белья, помимо собственно детергента (мыла), используют ещё и отбеливатель. Отбеливатели не удаляют грязь, а лишь обесцвечивают её. Одни из них окисляют и тем самым разрушают некоторые виды загрязнителей и красящих веществ. Классическим окислителем для этих целей служит хлор. В современных стиральных порошках используют более избирательные отбеливатели на основе брома. Другие отбеливатели, называемые усилителями белизны, делают выстиранное белье буквально «белее белого». Для этого в стиральные порошки добавляют флюоресцирующий «бесцветный краситель», который обеспечивает не только полное отражение видимого света, но и частичное превращение ультрафиолетового света в белый или голубоватый. В результате ткань становится «ослепительно белой».
Почему мыло моет?
Сложно представить себе современную жизнь без мыла. Чистота и гигиена, свежая опрятная одежда – всем этим мы обязаны именно мыльной пене и различным моющим средствам на его основе. Однако что вообще представляет собой это вещество, и почему оно может смывать с ткани и кожи грязь?
Мыло – важный и неотъемлемый инструмент современной гигиены
Жир и пепел
Появление первого мыла историки датируют приблизительно шестью тысячами лет назад. В те времена оно изготавливалось из растений и животных жиров. Обязательным ингредиентом древнего мыла также был обычный пепел. Химическая реакция, которая происходит между жиром и золой, составляет основу мыловарения. Называется она омылением. Соединяясь, эти вещества создают большое количество пузырьков, свойства которых позволяют удалять грязь.
Современный состав мыла
Конечно, сегодня в мыловарении больше не используются пепел и животный жир. Их заменили натуральные масла и каустическая сода. Соединяясь, они дают именно ту реакцию, которую заметили наши далекие предки, соединив пепел и жир животных. Само мыло по своему химическому составу является натриевой солью высшей жирной (карбоновой) кислоты.
Современная индустрия используют соли высших жирных кислот – стеариновой и пальмитиновой. Для производства твердого мыла используются натриевые соли этих кислот, а для жидкого – калиевые. Сегодня натуральное сырье не может полностью удовлетворить запросы мыловаренной промышленности, поэтому используются поверхностно-активные вещества, которые получают при переработке угля и нефтепродуктов.
Все дело в пузырьках!
Так почему же мыло моет? Дело в пузырьках. Пузырьки уменьшают поверхностное натяжение воды, но при этом усиливаются ее собственные моющие свойства. К пузырькам прилипают мелкие частички сажи, пыли и жира, а сама пена без труда смывается струей воды.
Очищающие свойства мыла основаны на поверхностном натяжении
При этом современные поверхностно-активные вещества, используемые для мыловарения, имеют такой молекулярный состав, который максимально эффективно взаимодействует с водой. Поверхностное натяжение воды уменьшается за счет того, что тончайшая мыльная «пленка» покрывает практически всю ее поверхность.
При стирке или мытье молекулы поверхностно-активных веществ покрывают частицы грязи, таким образом отделяя ее от ткани или другой поверхности. Покрытые такими молекулами частицы уходят в раствор в виде эмульсии или суспензии и больше не прилипают к ткани.
Химическая правда о мыле
Все мы пользуемся мылом. А знаете ли что это такое, и как оно работает. Вот мы и решили «пролить» немного химии на ваши головы. Не пугайтесь, ничего сложного. Зато много полезного и познавательного.
Что такое «вымыть руки»? Если бы всё, что нас окружает, растворялось в воде (как, например, поваренная соль), то вымыть руки было бы очень легко – опустить их в воду и подождать чуть-чуть. К сожалению, большая часть веществ, к которым мы прикасаемся, нерастворимы в воде, и поэтому, если они прилипают к рукам или одежде, то одна вода не позволяет нам избавиться от этой грязи и пятен. Однако можно заставить любое вещество хотя бы через короткое время (несколько секунд) раствориться в воде, образовав эмульсию или суспензию – взвесь мельчайших частичек жидкого (или твёрдого) вещества в воде. Этого времени часто бывает достаточно для того, чтобы поток чистой воды смыл эмульгированную грязь, сделав руки чистыми. Мыло и служит прекрасным эмульгатором – химическим соединением, облегчающим получение водных эмульсий частичек самых различных веществ.
Как родилось мыло и как его делают сейчас? При раскопках Древнего Вавилона были найдены глиняные ёмкости, наполненные веществом, похожим на мыло. Надписи на этих сосудах гласили, что содержимое сделано при кипячении жира с пеплом. Поэтому считают, что варить мыло умели ещё в 2800-х гг. до н.э. Записи на папирусах, оставленные древними египтянами за 1500 лет до н.э., тоже сохранили рецепты мыловарения из смеси животных и растительных масел и пепла. Древние греки не знали мыла, а когда мылись, то сначала тёрли себя глиной, песком, пемзой и пеплом, потом наносили на тело растительное масло и соскребали его вместе с грязью. Одежду свою они мыли безо всякого мыла в проточной воде.
Английское слово soap (мыло) произошло от названия горы Sapo в Италии, на вершине которой, согласно легенде, приносили животных в жертву, убивая и сжигая их. Дождь смывал вниз в реку Тибр, протекающую неподалёку, смесь расплавленного жира и древесного пепла. Поэтому глина вдоль Тибра хорошо мылилась, что быстро оценили женщины, стиравшие бельё на его берегах.
До Второй мировой войны мыло варили кипячением в воде жирных масел со щелочами. Жиры – это соединения глицерина и органических кислот, известных как жирные кислоты. Во время кипячения жиров со щелочами образуются глицерин и соли жирных кислот, т.е. мыл. Использование мыла после Второй мировой войны пошло на убыль, его постепенно вытесняли синтетические моющие средства. Главная причина спада потребления мыла состояла в том, что в жёсткой воде образовывались нерастворимые соли жирных кислот, выпадающие в осадок и отвечающие за появление кольцевого пятна в ванне и серый оттенок белья. Синтетические моющие средства (детергенты) имеют такой состав, что этой реакции не происходит.
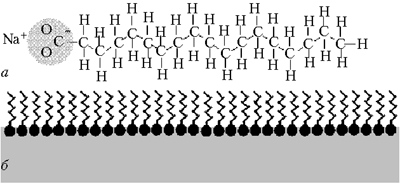
Что такое мыло? Мыло – это натриевая или калиевая соль одной из жирных кислот. Натриевые мыл более густые и, как правило, твёрдые; калиевые мыл более мягкие или жидкие. Молекула мыла представляет собой длинную цепочку (хвост), состоящую из десятка и более звеньев –CH2–, соединённых друг с другом, к одному концу которой (голове) прикреплена карбоксильная группа (–CO2). Простейшим мылом, например, является стеарат натрия, который можно представить формулой NaC17H35COO (жуть, правда?), где 17 атомов углерода с присоединёнными к ним атомами водорода вытянуты в извилистую цепочку. Асимметрия молекулы мыла – её важнейшее свойство. Голова молекулы в растворе заряжена отрицательно и поэтому притягивается к положительным полюсам диполей молекул воды или, как говорят, испытывает сродство к воде. Другой конец молекулы мыла электрически нейтрален и поэтому инертен по отношению к воде.
Вот так выглядит мыльная молекула стеарата натрия (а) и положение ионов этих молекул на поверхности плёнки воды (б):
Как мыло понижает поверхностное натяжение? Когда мыльная молекула стеарата натрия попадает в воду, то она диссоциирует на положительно заряженный ион Na+ и отрицательное основание жирной кислоты. Отрицательные ионы мыльных молекул выстраиваются так, чтобы с водой соприкасались лишь их головы, которые испытывают к ней сродство. Таким образом, на поверхности воды образуется двумерный «частокол» мыльных молекул, головы которых погружены в воду, а хвосты торчат наружу. Измерения показывают, что молекулы мыла на поверхности воды понижают её поверхностное натяжение почти в 2,5 раза. Происходит это из-за того, что, находясь на поверхности воды «головой вниз», они, во-первых, не стремятся внутрь и, во-вторых, отталкиваются друг от друга, а не притягиваются, как молекулы воды. Таким образом, увеличивать поверхность воды, если в ней растворено мыло, легче. А это значит, что жидкость может проникать в щели между нитями ткани. Другими словами, мыло делает воду «более мокрой», и «намыленные» капли воды легче пролезают в промежутки между нитями ткани.
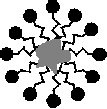
Как работает мыло? Мыльный раствор обволакивает частицы грязи, приводя к образованию эмульсий различных загрязняющих веществ, и удерживает нерастворимые частицы в состоянии суспензии в мыльной пене и воде, которые могут быть потом удалены c очищаемой поверхности проточной водой. Для моющего действия важно то, что углеводородная часть (хвост) отрицательного иона мыльной молекулы нерастворима в воде, но растворима в жирах и маслах. Поэтому водорастворимая отрицательно заряженная голова остаётся в воде, тогда как хвост погружается в жир. Анионы молекул со всех сторон окружают капельки жира и вытаскивают их в воду, в результате чего образуется взвесь капелек жира в воде. Так как каждая из мельчайших капелек несёт на себе отрицательный заряд, то они отталкиваются друг от друга, а не сливаются в более крупные капли. Этим объясняется диспергирующий и эмульгирующий эффект мыльных растворов.
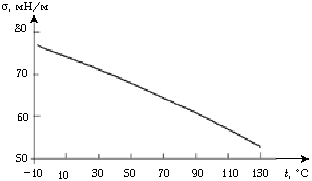
Почему горячая вода моет лучше? При нагревании средняя кинетическая энергия молекул воды растёт, а это значит, что каждой из них требуется меньше дополнительной энергии, чтобы выйти на поверхность. Поэтому коэффициент поверхностного натяжения воды уменьшается при нагревании, и она может проникать в самые мелкие поры и дырочки. Вот почему надо мыть руки горячей водой. Мыло и детергенты ещё больше понижают поверхностное натяжение горячей воды.
Почему мыло плохо стирает в морской воде? Морская вода характеризуется высоким содержанием двухвалентных катионов – Ca2+ и Mg2+. Эти катионы связываются с отрицательно заряженными головками мыльных молекул, мешая им образовать мицеллы вокруг частичек грязи и жира. Поэтому поверхностное натяжение мыльного раствора в морской воде увеличивается, что снижает качество стирки. То же происходит, когда в водопроводной воде высока концентрация двухвалентных ионов, например, железа. Такую воду называют «жёсткой», и мыло в ней стирает плохо.
Почему полоскать надо в холодной воде? Цель полоскания – убрать остатки мыла из выстиранной ткани. При стирке мы нагреваем воду, чтобы понизить поверхностное натяжение воды, поэтому мыльный раствор залезает в самые тонкие промежутки между волокнами ткани. Чтобы он вылез оттуда, необходимо повысить поверхностное натяжение, и тогда каждой из сплющенных капелек опять станет выгодно стать шарообразной, и они выскочат из тонких промежутков между нитями. Поэтому полоскать ткань после стирки следует в холодной воде, когда её поверхностное натяжение велико.
Надо ли использовать антибактериальное мыло? Мыльные молекулы обволакивают бактерии, как и частички прилипшей к коже грязи. Поэтому в мыльном растворе скоро оказывается большинство бактерий. Учёные доказали, что обычное мыло ничуть не хуже борется с бактериями, чем разрекламированное повсюду антибактериальное. В отличие от обычного антибактериальное мыло содержит химические препараты (антибиотики), убивающие бактерий. Однако именно это и является недостатком антибактериального мыла. Дело в том, что антибиотик не в состоянии убить абсолютно все бактерии, а оставшиеся в живых «супербактерии» обладают необычайно высокой стойкостью по отношению к данному антибиотику. Они начинают размножаться, и скоро на нашей коже появляется столько же бактерий, сколько было до мытья, но все эти бактерии являются «детками» супербактерий, поэтому многие их них переняли от своих родителей нечувствительность к действию этого антибиотика. В результате антибактериальное мыло скоро становится бесполезным, а супербактерии с кожи распространяются по всему организму, и бороться с ними нужно уже с помощью другого, более мощного антибиотика. В общем, «хотели, как лучше, а получилось…».
Что такое отбеливатель? В моющих средствах для стирки белья, помимо собственно детергента (мыла), используют ещё и отбеливатель. Отбеливатели не удаляют грязь, а лишь обесцвечивают её. Одни из них окисляют и тем самым разрушают некоторые виды загрязнителей и красящих веществ. Классическим окислителем для этих целей служит хлор. В современных стиральных порошках используют более избирательные отбеливатели на основе брома. Другие отбеливатели, называемые усилителями белизны, делают выстиранное белье буквально «белее белого». Для этого в стиральные порошки добавляют флюоресцирующий «бесцветный краситель», который обеспечивает не только полное отражение видимого света, но и частичное превращение ультрафиолетового света в белый или голубоватый. В результате ткань становится «ослепительно белой».
почему мыло стирает грязь? с физической точки зрения
Углеводородный «хвост» (C17H35-) имеет гидрофобные свойства, но «любит» родственные, углеводородные вещества — например, жиры. А -COONa прямо противоположное свойство — гидрофильность.
Гидрофобная часть молекулы мыла проникает в гидрофобное загрязняющее вещество (жир) , в результате чего поверхность каждой частицы жира оказывается как бы окруженной оболочкой из множества молекул мыла. В свою очередь гидрофильные части молекул, оказываются на поверхности загрязнения, они взаимодействуют с полярными молекулами воды. Благодаря этому молекулы мыла вместе с загрязнением отрываются от поверхности и уходят в водную среду.
Почему мыло отмывает грязь?
Никто из Вас не задумывался, почему обычная вода плохо смывает грязь (пятна), а мыльный раствор хорошо? Есть идеи? Если да, то поделитесь со мной, а если нет, то я предложу свою версию. Моя версия окончательно сформировалась на лекциях по физической химии, которые я уже смутно помню.
Давайте рассмотрим этот процесс на примере масляного пятна.
Мыльный раствор представляет собой жидкость, в которой присутствуют Поверхностно-Активные Вещества (сокращенно ПАВ).
Они выглядят так:
Но для простоты нарисуем их так:
Эти ПАВчики подлетают к грязи, которая прилипла к поверхности и начинают откусывать ее понемножку.
Так как таких ПАВчиков в мыльном растворе много, они откусывают большие куски (много по чуть-чуть = немного по большому куску).
Когда они откусили грязь (масляное пятно) от ладони, ПАВчики начинают окружать кусочки грязи. Получаются вот такие хороводы.
Затем все это смывается струей воды, и пятна как и не бывало! Чистота!
В зависимости от химического состава мыла, меняется тип загрязнения (его химический состав), которое данное мыло может отмыть. Поэтому не каждое мыло отмывает все типы грязи.
Конечно этот процесс я описал в шуточной форме, но оно так и происходит на самом деле. Данный процесс даже имеет серьезное название – солюбилизация! Правда, в реальности, молекулы ПАВ входят в масляную грязь не головами, а хвостами. Но целью статьи было донести суть процесса.
Вот так мы разобрались с этим обычным процессом, с которым сталкиваемся ежедневно (не забыли сегодня руки помыть?).
Почему мыло моет?
А если подробнее:
При смешивании мыла и воды, у последней уменьшается поверхностное натяжение, что способствует увеличению смачивающей способности. Затем те самые микро пузырьки «прилепляют» к себе мокрую грязь, и мы можем без труда смыть образовавшуюся эмульсию.
Найдены возможные дубликаты
тема не раскрыта, не всякая грязь может быть мокрой, есть и гидрофобная ненамокаемая грязь, но её можно смыть мылом
помогу, мыло это соли жирных кислот растворимые в воде, попадая в воду они распадаются на ионы, как и другие соли, один из которых СH3-(CH2)N — Na+ (где N дохуя, потому что жирные кислоты длинные),которые ориентируются по поверхности положительными хвостами внутрь и делают поверхность способной смешиваться с другими жирными кислотами (зачастую грязь это какой-то жир).
Единственное, что я понял.
кароче блять, молекула мыла большая, одной стороной может связаться с грязью (жирорастворимая часть молекулы, ведь грязь на коже удерживается в основном за счет кожного сала), другой — с водой (гидрофильная часть), так они смешиваются, со школы инфа, 10 лет назад заканчивал
Я ещё в детстве читал какую-то книжку для детей по химии, там было написано, типа «представьте что у мыла есть руки и хвост, так вот руками оно очень любит цепляться за воду, а к хвосту прилипает грязь и так с водой мыло утаскивает грязь с рук». Так понятнее?
Во-во, этот фактор гораздо значимее каких-то микропузырьков. Грязь это как правило не столько всякая хуета вроде пыли и т. п., а смесь этой хуеты с кожным салом и другими жирами. Мыло в результате химической реакции превращает эти жиры не в вязкую субстанцию, которая легко смывается водой.
Невероятно. Держи нас в курсе.
Книжки в детстве надо было читать. Много в каких это объясняется, попроще конечно.
Получение мыла основано на реакции омыления — гидролиза сложных эфиров жирных кислот (в частности, жиров) со щелочами, в результате которого образуются соли щелочных металлов и спирты. В специальных ёмкостях (варочных котлах) нагретые жиры омыляют едкой щёлочью (обычно гидроксидом натрия).
*режим ботан включен*
если рассматримать вопрос с чисто химической точки зрения, без учитывания поверхностного натяжения и т.п., то под пузырьками, скорее всего, имеются в виду мицеллы (элементарные частицы коллоидной системы), т.к. мыла при контакте с водой — полярным протонным растворителем — дают высокодисперсную коллоидную систему (у соли жирной кислоты углеводородный конец гидрофобный, ориентируется во внутрь «шарика», а другой конец — кислотный — гидрофильный и располагается на поверхности «шарика»). с другой стороны, эти соли диссоциируют и гидролизуют, что дает довольно неплохую щелочную среду. получается, что у мыла двоякое действие: с одной стороны мицеллы могут захватывать во внутрь себя другие молекулы жира с наших рук (у нас на руках всегда собственный жир и на него липнет вся грязь), с другой стороны, щелочная среда частично омыляет жир с наших рук, растворяя его уже именно в воде. таким образом мыльный раствор является универсальным моющим средством, т.к. позволяет одновременно избавляться и от полярных неорганических загрязнителей, типа грязи и пыли (благодаря полярной воде), при этом отлично справляется со всякими жирами и прочим (благодаря наличию мицелл). ну а вообще основное «моющее» и антибактериальное действие достигается именно смыванием нашего собственного жира с рук, на который налипло много всякого.
*режим ботан выключен*
Раньше жир с золой смешивали, она действовала как мыло. Щас золу заменили чем то. И жир похоже заменили. Хотя в «хозяйственном» еще применяют
- http://ximik.biz/prakticheskaya-himiya/79-pochemu-mylo-moet
- http://nsportal.ru/ap/library/drugoe/2017/07/26/proekt-pochemu-mylo-moet
- http://vitazone.ru/forum/showthread.php?t=2365
- http://slygod.com/usage/pochemu-mylo-moet/
- http://www.livemaster.ru/topic/1011295-himicheskaya-pravda-o-myle
- http://otvet.mail.ru/question/92230248
- http://boeffblog.ru/fizika/fizika-eto-interesno/pochemu-mylo-otmyvaet-gryaz
- http://pikabu.ru/story/pochemu_myilo_moet_5345087