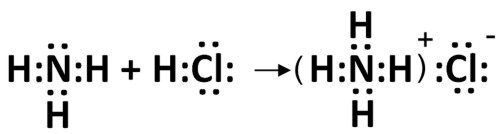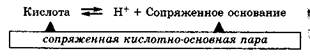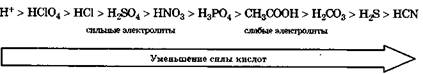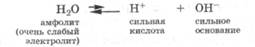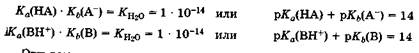Согласно теории электролитической диссоциации Аррениуса, кислотаминазываются вещества, при диссоциации которыхобразуется ион гидроксония ианион кислотного остатка, а основаниями называются соединения. при диссоциации которых образуются гидроксид-ионы и катионы металла. Теория Аррениуса объясняет поведение и свойства электролитов в водных растворах, а также дает возможность сравнивать силу электролитов по степени электролитической диссоциации.
Однако с помощью теории Аррениуса нельзя объяснить изменение свойств многих веществ в неводных растворителях. В зависимости от растворителя одно и то же вещество может быть сильным и слабым электролитом, кислотой или основанием или вообще не проявлять кислотно-основных свойств.
В настоящее время существует несколько обобщенных теорий кислот и оснований. Наиболее широкое применение имеютпротонная теория кислот и оснований,предложенная в 1923 г. датским ученым Бренстедом и английским ученым Лоури, и электронная теория Льюиса.
Согласно теории Бренстеда—Лоури, кислотами называют вещества, отдающие протоны, а основаниями — вещества, принимающие протоны. Протон не может существовать в растворе самостоятельно, он должен быть принят основанием, поэтому, чтобы кислота могла отдать протон, необходимо присутствие основания, к которому протон переходит. Таким образом, возникают кислотно – основные пары, которые называют сопряженными. Следовательно, каждая кислота имеет сопряженное с ней основание и каждое основание – сопряженную с ним кислоту.
Реакция отдачи Протона выражается схемой:
Реакция принятия протона выражается схемой:
Например, в уравнениях:
кислота1 основание2 основание1 кислота2
В приведенном равновесии участвуют 2 пары кислот и оснований: сопряженными кислотой и основанием являются НС1 и С1 — , NH4 — и NНз.
К кислотам и основаниям по теории Бренстеда – Лоури относятся не только молекулы, но и ионы. Например, ионы аммония и гидросульфат ион являются кислотами, так как они способны отщеплять протоны:
HSO4 — ↔ SO4 2- + H + . Ацетат-ион является основанием так как он принимает протон.
СНзСОО — + Н + ↔ СНзСООН.
Одно и то же вещество при растворении в разных растворителях может проявлять амфотерные свойства, т. е. Быть кислотой и основанием. Например, в жидком аммиаке гидросульфид-ион HS — проявляет свойства кислоты:
кислота основание кислота основание
находясь же в бромоводороде НS — , будет основанием
НS — + НВг ↔ Н2S + Вг — .
Основание Кислота Кислота Основание
Во всех этих реакциях протон играет особую роль при взаимодействии кислот и оснований, поэтому, согласно теории Бренстеда—Лоури, кислоты и основания носят общее название протолиты, а реакции между ними называют протолитическими. К протолитическим реакциям относят реакции нейтрализации, гидролиза, диссоциации кислот и оснований. Например:
1) диссоциация кислот:
основание2 кислота1 кислота2 основание1
2) диссоциация оснований:
кислота1 основание2 основание1 кислота2
CH3COONa + HOH ↔ CH3COOH + NaOH
4) реакция нейтрализации:
HCl + NaOH ↔ NaCl + H2O
кислота1 основание2 кислота2 основание1
Механизм этих реакций один и тот„же в реакциях происходит перемещение протона от одних молекул или ионов к другим молекулам или ионам.
Применив протонную теорию, растворители можно разделить на три группы: кислые, основные и амфотерные неводные растворители.
К кислым неводным растворителям относятся уксусная и муравьиная кислоты (а также их смеси с уксусным ангидридом, бензолом, хлороформом), серная, циановодородная. фтороводородная кислоты. Молекулы этих растворителей легко отдают протоны, поэтому в кислых растворителях сила оснований возрастает, ионизация основания резко увеличивается.
К основным неводным растворителям относятся диметилформамид. пиридин, бутиламин и их смеси с бензолом, хлороформом, а также жидкий аммиак, этилендиамин, формамид, 1,4-диоксан, этаноламин.Основные растворители обладают ярковыраженным сродством к протону. Их акцепторные свойства поотношению к протону преобладают над донорными. Молекулы этих растворителей могут отдавать протоны лишь очень сильным основаниям.
Основные растворители увеличивают силу кислот. По уменьшению сродства к протону растворители располагают в следующем порядке: NНз, N2Н4, H2O, C2H5OH, НСN, Н2S, СНзСООН, НСООН, НF, Н2SO4, HNO3, HClO4.
Амфотерные растворители способны проявлять двойственный характер, т. е. они обладают основными и кислотными свойствами. К таким растворителям относятся вода, пероксид водорода, метанол, этанол и др.
Таким образом, применяя различные растворители кислотного, основного или амфотерного характера, можно изменять силу кислот и оснований. Эти приемы широко используют, в методе кислотно-основного титрования в неводных растворителях. Этот метод позволяет количественно определять кислоты, основания, соли, титрование которых в воде невозможно или затруднительно из-за их слабых кислотно-основных свойств или плохой растворимости.
Протолитическая теория является более общей по сравнению с классической теорией Аррениуса, так как она объясняет поведение кислот и оснований не только в воде, но и в неводных растворителях.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Да какие ж вы математики, если запаролиться нормально не можете. 7702 — 

Дальнейшим развитием теории кислот и оснований явилась предложенная И. Бренстедом и Т. Лоурипротолитическая (протонная) теория. В соответствии с этой теорией:
Кислотой называют любое вещество, молекулы (или ионы) которого способны отдавать протон, т.е. быть донором протона;
Основанием называют любое вещество, молекулы (или ионы) которого способны присоединять протон, т.е. быть акцептором протона;
Таким образом, понятие основания значительно расширяется, что подтверждается следующими реакциями:
По теории И. Бренстеда и Т. Лоури кислота и основание составляют сопряженную пару и связаны равновесием:
КИСЛОТА ⇄ ПРОТОН + ОСНОВАНИЕ
Поскольку реакция переноса протона (протолитическая реакция) обратима, причем в обратном процессе тоже передается протон, то продукты реакции являются друг по отношению к другу кислотой и основанием. Это можно записать в виде равновесного процесса:
где НА – кислота, В – основание, ВН + – кислота, сопряженная с основанием В, А — – основание, сопряженное с кислотой НА.
Примеры.
HCl и H2O – кислоты, Cl — и OH — – соответствующие сопряженные с ними основания;
HSO4 — и H3O + – кислоты, SO4 2 — и H2O – основания;
NH4 + – кислота, NH2 — – основание, а NH3 выступает в роли как кислоты (одна молекула), так и основания (другая молекула), т.е. демонстрирует признаки амфотерности – способности проявлять свойства кислоты и основания.
Такой способностью обладает и вода:
Здесь одна молекула Н2О присоединяет протон (основание), образуя сопряженную кислоту – ион гидроксония Н3О + , другая отдает протон (кислота), образуя сопряженное основание ОН — . Этот процесс называется автопротолизом.
Из приведенных примеров видно, что в отличие от представлений Аррениуса, в теории Бренстеда и Лоури реакции кислот с основаниями не приводят к взаимной нейтрализации, а сопровождаются образованием новых кислот и оснований.
Необходимо также отметить, что протолитическая теория рассматривает понятия «кислота» и «основание» не как свойство, но как функцию, которую выполняет рассматриваемое соединение в протолитической реакции. Одно и то же соединение может в одних условиях реагировать как кислота, в других – как основание. Так, в водном растворе СН3СООН проявляет свойства кислоты, а в 100%-й H2SO4 – основания.
Однако, несмотря на свои достоинства, протолитическая теория, как и теория Аррениуса, не применима к веществам, не содержащим атомов водорода, но, в тоже время, проявляющим функцию кислоты: галогенидам бора, алюминия, кремния, олова.
Дата добавления: 2015-10-30 ; просмотров: 1674 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Теория Бренстеда-Лоури
В 1923 г. Бренстед и Лоури выдвинули новую теорию кислот и оснований, основанную на представлении о переносе протона. Согласно этой теории, кислота представляет собой вещество, состоящее из молекул или ионов-доноров протонов (т. к. они отдают протоны), а основание-вещество, состоящее из молекул или ионов-акцепторов протонов (т.к. они принимают протоны).
Чтобы подробнее разобраться в этой теории, начнем наше рассмотрение со случая сильной кислоты, как, например, соляная кислота. При растворении хлороводорода в воде его молекулы полностью диссоциируют, образуя ионы водорода H+ и хлорид-ионы Cl». Ионы водорода называют также протонами, поскольку каждый такой ион представляет собой просто протон. В растворе эти протоны связываются с молекулами воды, образуя ионы гидроксония H3O+. Растворение хлороводорода в воде может быть представлено с помощью уравнения
В случае слабой кислоты, как, например, уксусная кислота, молекулы кислоты лишь частично диссоциированы в водном растворе, так что в нем устанавливается равновесие
(1)
Но и в этом случае молекулы кислоты тоже донируют (передают) протоны молекулам воды.
Каждая молекула соляной кислоты и уксусной кислоты может донировать только по одному протону. Поэтому они называются однопротонными или одноосновными кислотами (последнее название объясняется тем, что каждая такая кислота имеет только одно сопряженное основание; см. ниже).
Кислота, способная донировать более одного протона, называется многопротонной или многоосновной. Например, серная кислота является двухпротонной, потому что она может донировать два протона. Ее называют также двухосновной, потому что она имеет два сопряженных основания, HSO4- и SO4-; процесс растворения серной кислоты в воде можно представить двумя уравнениями:
H2SO4(ж.) + H2O (ж.) = H3O+ (водн.) + HSO4 (водн.) или
H2SO4(ж.) + 2H2O(ж.) = 2H3O+ (водн.) + SO2.» (водн.)
Сильные основания, такие, как гидроксиды щелочных металлов, полностью ионизируются в воде:
NaOH(TB.) + H2O = Na+(водн.) + ОН- (водн.)
Эти вещества являются основаниями, потому что гидроксидные ионы могут акцептировать (присоединять) ионы водорода:
ОН- (водн.) + H3O+ (водн.) = 2H2O (ж.)
Эта реакция является общей для всех реакций нейтрализации между кислотами и основаниями в водных растворах. Отметим также, что в водных растворах ионы водорода существуют в гидратированной форме, т.е. в виде ионов гидроксония.
Рассмотрим теперь реакцию между слабым основанием аммиаком NH3 и хлоро-водородом в газовой фазе. В этой реакции происходит образование твердого хлорида аммония:
Реакция, обратная этой, называется реакцией термической диссоциации хлорида аммония. Аммиак представляет собой основание, потому что он акцептирует протон от хлороводорода. Однако следует обратить внимание на то обстоятельство, что в обсуждаемом равновесии не принимают участия ни вода, ни гидроксидные ионы. Таким образом, теория Бренстеда-Лоури охватывает и такие кислотно-основные реакции, которые осуществляются в отсутствие растворителя либо в присутствии неводного растворителя.
Если внимательнее присмотреться к каждому из обсуждавшихся выше равновесий, то обнаружится, что в равновесной смеси всегда присутствуют частицы четырех типов. Пользуясь представлениями теории Бренстеда-Лоури, нетрудно убедиться, что две из этих частиц являются кислотами, а две другие-основаниями. Например,
Эта равновесная смесь состоит из двух следующих сопряженных пар кислот и оснований:
Обратим внимание на то, что в каждой сопряженной паре кислота и основание отличаются друг от друга на один протон. Каждая кислота имеет свое сопряженное основание. Сильной кислоте всегда соответствует слабое сопряженное основание, а слабой кислоте — сильное сопряженное основание.
Протолитическая теория Брёнстеда и Лоури
Читайте также:
- A. Организм. Индивид. Личность. Ииндивидуальность. Теория развития индивидуальности Б.Г. Ананьева.
- I.4. Общая теория относительности (ОТО) и теория гравитации
- L Ситуативная теория (Т.Хилтон)
- XY» — Теория Д.макгрегора.
- Адсорбционная теория Штерна
- БИХЕВИОРИЗМ И ТЕОРИЯ СОЦИАЛЬНОГО НАУЧЕНИЯ
- Боровская теория атома.
- Бюрократическая теория организации
- В современной российской философии (как и в прежней советской философии) широко распространено материалистическое объяснение природы сознания,известное как теория отражения.
- Введение в менеджмент: теория и практика
- Взаимодействия. Концепция поля, гравитационное и электромагнитное поля. Волновая теория света
- Возникновение Вселенной. Теория Большого Взрыва
Теории кислот и оснований
До сих пор мы рассматривали равновесия в растворах электролитов с точки зрения традиционной теории кислот и оснований, сформулированной в конце ХIX века Аррениусом и Оствальдом. Согласно этой теории кислоты — электролиты, образующие при диссоциации в растворе ионы Н + (точнее — катионы гидроксония Н3О + ), а основания — электролиты, образующие в результате диссоциации ионы гидроксила ОН — . Однако данная теория охватывает слишком узкий круг явлений и не всегда объясняет кислотно-основные свойства соединений. Например, аммиак и его органические производные — амины — проявляют свойства оснований, хотя и не содержат в своем составе гидроксильных групп. Кислые растворы часто нейтрализуют содой, но карбонат натрия с точки зрения теории Аррениуса — Оствальда является солью, а не основанием. Металлический цинк растворяется с выделением водорода в растворе соли алюминия так же, как в кислоте. Кроме того, часто необходимо объяснить кислотно-основные свойства веществ в неводных средах. Поэтому уже в начале ХХ столетия появилась потребность в более общей теории кислот и оснований.
Первой обобщенной теорией кислот и оснований явилась протолитическая теория, созданная в 1923 г. одновременно и независимо друг от друга Бренстедом, Лоури и Бьеррумом, хотя в дальнейшем наибольший вклад в её развитие внес Бренстед. Протолитическими называют реакции, протекающие с участием катионов водорода Н + , то есть протонов. Согласно Бренстеду, любая протолитическая реакция является кислотно-основным равновесием. Кислота есть донор протонов, а основание — акцептор протонов. Кислота и основание, связанные между собой протолитическим равновесием, называются сопряженными. Кислоту и её характеристики в протолитической теории принято обозначать или индексировать буквой А (acidum), а основание — B (base). Протолитическое равновесие в общем виде может быть записано следующим образом:
А Û В — + Н + ; (9.1)
где А — кислота, В — сопряженное с ней основание. Количественной характеристикой протолитического равновесия является константа кислотности, вычисляемая согласно закону действующих масс:
Чем больше константа кислотности, тем сильнее кислота. Силу основания характеризуют также константой кислотности данного протолитического равновесия. Чем ниже константа кислотности, тем сильнее сопряженное основание. Иногда для характеристики оснований используют константу основности, описывающую следующее равновесие:
B — + H2O Û A + OH — ; Kb = [A]×[OH — ]×Pg / [B — ] ; (9.3)
Если константы кислотности и основности одного и того же равновесия перемножить, то получим:
Чем больше константа основности, тем сильнее основание и тем слабее сопряженная кислота.
Типы кислот по Бренстеду:
1. Все кислоты Аррениуса — Оствальда. Константа кислотности для них равна константе диссоциации кислоты.
2. Гидролизующиеся катионы слабых оснований, например, катион Fe 3+ . Его гидролиз является протолитической реакцией, сокращенная запись которой: Fe 3+ + H2O Û Fe(OH) 2+ + H + , несколько отличается от уравнения (9.1). Однако, если вспомнить, что реально в водном растворе катион железа (3+) находится в форме аквокомплекса, то реакцию гидролиза можно записать точно в соответствии с (9.1):
Константа кислотности катионов в водных растворах равна константе их гидролиза. Для железа (3+) Ka = 6,3×10 — 3 . Таким образом, катион Fe 3+ является кислотой средней силы, совпадающей с силой фосфорной кислоты, и значительно превышающей силу уксусной кислоты, константа кислотности которой 1,8×10 — 5 .
4. Катионы не только слабых, но и сильных оснований в неводных растворах. В неводных растворах константа кислотности отличается по величине от константы гидролиза и количественно характеризует процессы протолитического сольволиза. При этом в различных протолитических растворителях сольволизу могут подвергаться практически все катионы.
Типы оснований по Брёнстеду:
1. Все основания Аррениуса — Оствальда, то есть соединения, образующие в результате диссоциации ионы гидроксила. Их константа основности равна константе диссоциации, а константа кислотности согласно (9.4) в водном растворе равна константе гидролиза образующегося при диссоциации катиона.
2. Гидролизующиеся анионы слабых кислот. Их константа основности в водном растворе равна константе их гидролиза, а константа кислотности — константе диссоциации продукта гидролиза. Например, для сульфид-иона константа кислотности равна константе диссоциации гидросульфид-иона. По значению константы основности 2,75×10 — 3 сульфид-ион является более сильным основанием по сравнению с гидроксидом аммония, константа диссоциации которого 1,8×10 — 5 .
3. Молекулы, способные акцептировать протоны: аммиак, амины, гидразин, гидроксиламин, фосфин и др.
4. Все анионы в различных неводных протолитических растворителях могут подвергаться сольволизу. Например, нитрат-ион, не гидролизующийся в водном растворе, претерпевает сольволиз в безводной уксусной кислоте с образованием недиссоциированных молекул HNO3.
Кроме кислот и оснований в теории Бренстеда различают амфипротонные соединения. Это аналоги амфотерных электролитов Аррениуса — Оствальда, которые в зависимости от среды могут проявлять свойства как кислот, так и оснований. Типы амфипротонных соединений:
1. Гидроксокатионы. Например, Fe(OH) 2+ в реакции (9.5) является основанием, но в процессе гидролиза по 2-ой ступени выступает как кислота:
2. Гидроанионы, например, гидросульфид-ион:
HS — Û S 2 — + H + (кислота)
HS — + H2O Û H2S + OH — (основание)
3. В неводных средах любая кислота является основанием по отношению к более сильной кислоте. Так же любое основание проявляет кислотные свойства в отношении более слабого основания. То есть в неводных средах амфипротонность является общим свойством соединений. Например, одна из сильных кислот — серная — ведет себя как основание (акцептор протонов) в жидкой безводной хлорной кислоте:
4. Амфипротонные растворители, например, вода:
Н2О Û Н + + ОН — (кислота)
Кислотно-основные свойства соединений существенно зависят от природы растворителя. Чем выше протон-донорные кислотные свойства растворителя, тем сильнее выражены в его среде основные свойства растворенных веществ и их сольволиз. Кислотные свойства растворителя количественно характеризуют константами равновесий автопротолиза (отщепления протона) в среде чистого растворителя. Для воды константа автопротолиза равна её ионному произведению 10 — 14 (при 298 К). Другие примеры:
2HCOOH Û HCOOH2 + + HCOO — ; KS = 6,3×10 — 7 ;
Чем выше константа автопротолиза, тем сильнее кислотные свойства растворителя, тем сильнее будет протекать в нем сольволиз анионов. Сольволиз катионов, напротив, сильнее в растворителях с низкими константами автопротолиза. Любое вещество ведет себя как кислота по отношению к другому соединению с более низкой константой автопротолиза и как основание в отношении к соединению, константа автопротолиза которого выше. Так уксусная кислота, расположенная в середине приведенного выше ряда примеров, является кислотой по отношению к воде, этанолу и аммиаку и основанием по отношению к муравьиной и серной кислотам. Сила кислоты определяется соотношением констант автопротолиза кислоты и растворителя. В водном растворе уксусная кислота слабая, а в этаноле и в жидком аммиаке — сильная.
Буферный раствор по Бренстеду есть смесь сопряженных кислоты и основания в растворителе с близкой по величине константой автопротолиза. Следовательно, буферность является таким же общим свойством, как и амфотерность, и определяется средой, в которой находится соединение. Например, смесь азотной кислоты с нитратом калия в водной среде не обладает буферными свойствами, а в безводной серной кислоте это буферная система.
Заслуга протолитической теории в том, что она объяснила кислотно-основные свойства широкого круга соединений, в том числе в неводных средах. Однако все-таки эта теория не охватывает вещества, не вступающие в протолитические равновесия. Более общей, но менее разработанной в плане количественных характеристик, является теория кислот и оснований Льюиса, появившаяся одновременно в 1923 г.
Дата добавления: 2014-01-07 ; Просмотров: 1583 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
12.Протонная теория кислот и оснований и. Бренстеда и т. Лоури.
Протонная теория кислот и оснований.В 1923г И. Бренстед и Т. Лоури разработали протонную теорию кислот и оснований. Согласно этой теории
кислотой называют любое вещество, молекулярные частицы которого (в том числе ионы) способны отдавать протон, т.е. быть донором протонов;
основанием называют вещество, молекулярные частицы которого (в том числе и ионы) способны присоединять протоны, т.е. быть акцептором протонов.
Такие определения кислот и оснований позволяют включать в их число не только молекулы, но и ионы. Например, карбонат-ион согласно протонной теории является основанием, т.к. в водном растворе он присоединяет протон:
Согласно протонной теории кислоты подразделяют на три типа:
1. Нейтральные кислоты, например HCl, H2SO4, H3PO4 и др.
2. Катионные кислоты, представляющие собой положительные ионы, например NH4 + , Н3О + :
3. Анионные кислоты, представляющие собой отрицательные ионы, например, HSO4 — , H2PO4 — , HPO4 2- и др.:
Подобного типа классификация имеется и для оснований:
1. Нейтральные основания, например, NH3,Н2О, С2Н5ОН и др.:
2. Анионные основания, представляющие собой отрицательные ионы, например, Cl — , СН3СОО — , ОН — :
3. Катионные основания, представляющие собой положительные ионы, например, Н2N−NH3 + .
Растворители типа воды, жидкого аммиака, а так же анионы многоосновных кислот, которые могут быть и донорам и акцепторами протонов, являются амфолитами.
Например, в реакции
молекула воды отдает протон и является кислотой. Однако в реакции
молекула воды присоединят протон и является основанием. Таким образом, вода — типичный амфолит.
Процесс диссоциации (ионизации) вещества происходит в контакте с растворителем. При этом растворитель выполняет или функцию кислоты или основания. Например, при растворении аммиака вода – кислота
При растворении фторида водорода – основание
Если сродство к протону у растворителя больше, чем у растворенного вещества, то растворитель выступает как основание (сродство к протону Н2О больше сродства к протону HF), а если оно меньше – как кислота (сродство к протону Н2О меньше сродства к протону NH3).
Согласно протонной теории, отдавая протон, кислота превращается в основание, которое называют сопряженным этой кислоте:
т.е. каждой кислоте соответствует сопряженное основание. Наоборот, основание, присоединяя протон, превращается в сопряженную кислоту:
II. (основание)2+Н + =(сопряженная кислота)2
Например, кислоте H2SO4 соответствует сопряженное основание HSO4 — , а основанию Cl — — сопряженная кислота НСl.
Для краткости обратимый процесс кислотно-основного взаимодействия называют кислотно-основным равновесием.
Несмотря на свои достоинства теория Бренстеда, как и теория Аррениуса, не применима к веществам, проявляющим функцию кислоты веществ, не содержащих водорода, например галогенидам бора, алюминия, кремния и олова. Поэтому более общей является теория кислот и оснований Льюиса.
Теория Льюиса (электронная теория).В теории Льюиса за основу взято наиболее общее свойство кислот и оснований – их электронное строение. Согласно этой теории:
кислотойназывают вещество, принимающее неподеленную электронную пару, — акцептор электронов;
основанием называют вещество, поставляющее электроны для образования химической связи, — донор электронов.
По Льюису отличительной способностью кислот и оснований является их взаимная нейтрализация путем образования ковалентной связи:
В приведенных примерах в качестве кислоты выступают молекулы трихлорида брома и оксида серы (VI), а в качестве оснований – молекулы аммиака и воды.
Таким образом, теория Льюиса рассматривает разные химические процессы как однотипные: реакцию аминов с галогенидом бора, комплексообразование.
К основаниям Льюиса относят галогенид — ионы, аммиак, алифатические и ароматические амины, кислородсодержащие соединения общей формулы R2CO (где R- органический радикал).
К кислотам Льюиса относят галогениды бора, алюминия, кремния, олова и других элементов.
Рассмотренные теории кислот и оснований не противоречат, а дополняют друг друга и имеют глубокую внутреннюю связь. Так, кислоты, по Бренстеду, можно рассматривать как частный случай льюисовских кислот, поскольку протон характеризуется большим сродством к электронной паре и может рассматриваться, по Люйсу, как кислота.
Свойства кислот и оснований
Распространенные кислоты:
- HCl — хлороводород (соляная кислота);
- H2SO4 — уксус;
- H2CO3 — серная кислота;
- CH3COOH — угольная кислота (газированная вода);
- H3BO3 — борная кислота (глазные капли);
- C16H12O6 — аспирин.
Распространенные основания:
- NH3 — нашатырный спирт (водный раствор аммиака);
- NaOH — гидроксид натрия (щелок);
- NaHCO3 — бикарбонат натрия (пищевая сода);
- CaCO3 — карбонат кальция.
Основные свойства кислот и оснований сведены в таблице:
| Кислоты | Основания | |
|---|---|---|
| На вкус | кислые | горькие |
| При попадании на кожу | вызывают ожог | вызывают ощущение намыленности |
| Вступают в реакцию | с металлами с образованием газообразного водорода | с маслами и жирами |
| Цвет индикатора | окрашивают лакмус в красный цвет | окрашивают лакмус в синий цвет |
| Образуют | диоксид углерода при соединении с пищевой содой | соль и воду при соединении с кислотами |
Приведенные выше свойства растворов кислот и оснований объясняют две основные теории: Аррениуса и Бренстеда-Лоури.
Теория Аррениуса
Сванте Аррениус разработал первую современную кислотно-основную теорию, которая, хоть и не лишена недостатков, но актуальна и по сей день.
Согласно теории Аррениуса:
- кислоты являются электролитами, которые диссоциируют с образованием ионов водорода, например: HCl→H + +Cl —
- основания — это электролиты, которые диссоциируют в растворах с отщеплением гидроксид-ионов (ОН — ), например: NaOH→Na + +OH —
Поскольку, при смешивании водного раствора кислоты и основания получается нейтральный раствор, кислотно-основную реакцию Аррениус назвал реакцией нейтрализации.
Ион водорода, взаимодействуя с гидроксид-ионом, образует молекулу воды (основной процесс, лежащий в основе кислотно-основных реакций Аррениуса):
Теория Аррениуса не лишена недостатков. Например, в результате взаимодействия газообразных аммиака с хлористым водородом образуется твердое вещество хлорид аммония:
В результате реакции соляная кислота передает аммиаку ион водорода, однако, данная реакция протекает в газовой фазе, а не в водном растворе (в ней не участвует гидроксид-ион), поэтому, ее нельзя отнести к кислотно-основным реакциям по Аррениусу.
Данную проблему решает протонная теория Бренстеда-Лоури, предложенная в 1923 году.
Теория Бренстеда-Лоури
Согласно теории Бренстеда-Лоури, кислота является донором, поставляя свои протоны водорода для образования химической связи, а основание выступает в роли акцептора, принимая эти протоны. Для образования донорно-акцепторной связи основание предоставляет одну пару своих электронов. Таким образом, ковалентная связь между кислотой и основанием образуется за счет двух электронов, которые изначально принадлежали одному атому, выступающего в качестве донора электронной пары, и свободной орбитали другого атома, выступающего в роли акцептора той же пары. Обычно ковалентная связь образуется из двух атомов, каждый из которых предоставляет по одному своему электрону, однако, при донорно-акцепторном способе формирования ковалентной связи оба электрона предоставляет один и тот же атом.
В ходе реакции взаимодействия NH3 и HCl, соляная кислота является донором протона, при этом аммиак и основание играют роль акцепторов, поскольку у аммиака имеется одна пара несвязанных электронов, которая используется для создания донорно-акцепторной связи.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки:
ПРОТОЛИТИЧЕСКАЯ ТЕОРИЯ КИСЛОТ И ОСНОВАНИЙ
Понятия «кислота» и «основание» применяют по отношению к двум группам соединений, обладающих совокупностью диаметрально противоположных свойств. В 1923 г. И. Бренстед и Т. Лоури предложили общую протолитическую теорию кислот и оснований. Согласно этой теории понятиям кислота и основание отвечают следующие определения.
 |
Кислота — молекула или ион, способные отдавать катион водорода (протон). Кислота — донор протонов.
Основание — молекула или ион, способные присоединять катион водорода (протон). Основание — акцептор протонов.
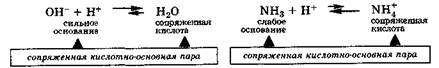
Кислота, отдавая протон, превращается в частицу, стремящуюся его принять, которая называется сопряженным основанием:
Основание, присоединяя протон, превращается в частицу, стремящуюся его отдать, которая называется сопряженной кислотой:
Совокупность кислоты и ее сопряженного основания или основания и его сопряженной кислоты называются сопряженными кислотно-основными парами.
Сила кислоты определяется ее способностью отдавать протон, т. е. сильная кислота — активный донор протона. Сила кислот в водных растворах уменьшается в ряду:
 |
Сила основания определяется его способностью присоединять протон, т. е. сильное основание — активный акцептор протона. Сила оснований в водных растворах, т. е. их сродство к протону, уменьшается в ряду:
Сильные кислоты, легко отдавая протон, превращаются в сопряженные основания, которые плохо присоединяют протон. Поэтому диссоциация этих кислот протекает практически необратимо:
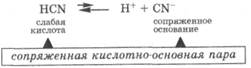
Слабые кислоты, трудно отдавая протон, превращаются в сопряженные основания, которые активно принимают протон, что делает диссоциацию слабых кислот обратимым процессом, причем равновесие смещено в сторону недиссоциированной формы:
Аналогичным образом ведут себя сильные и слабые основания, превращаясь в результате реакции в соответствующие сопряженные кислоты, т. е. и в этих случаях также имеются сопряженные кислотно-основные пары:
Некоторые вещества способны выступать в одних реакциях в роли донора протона, отдавая его соединениям, у которых сродство к протону выше, а в других — в роли акцептора протона, отнимая его у соединений с меньшим сродством к протону. Такие вещества называются амфолитами.
Амфолиты — молекулы или ионы, способные как отдавать, так и присоединять протон, а следовательно, вступать в реакции, характерные как для кислот, так и для оснований. Амфолит проявляет свойства кислоты или основания в зависимости от того, с какими веществами он взаимодействует. Типичным амфолитом является вода, так как в результате ее электролитической диссоциации образуются одновременно сильная кислота и сильное основание:
Кроме того, вода взаимодействует и с кислотами, выступая основанием, и с основаниями, проявляя свойства кислоты:
 |
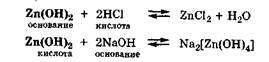 |
Амфолитами являются гидроксиды некоторых металлов (Zn, Al, Pb, Sn, Cr):
Амфолитами являются гидроанионы многоосновных кислот, например НС03-, НР042-и Н2РО4-.
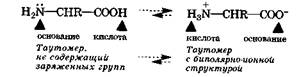
Амфолитами являются также соединения, молекулы которых содержат две различные кислотно-основные группы, например важные в биологическом отношении а-аминокислоты. Молекула а-аминокислоты в результате переноса протона от карбоксильной группы на аминогруппу превращается из таутомера*, не содержащего заряженные группы, в таутомер, имеющий биполярно-ионную (цвиттерионную) структуру. Таким образом, для а-аминокислот характерна прототропная таутомерия (разд. 21.2.1).
В кристаллическом состоянии и в водных растворах это равновесие для а-аминокислот практически полностью смещено в сторону таутомера с биполярной структурой. Так, для глицина в водном растворе содержание таутомера с биполярно-ионной структурой в 223 000 раз больше, чем другого таутомера.
Вследствие этой особенности строения молекулы а-аминокислот проявляют кислотные свойства за счет аммонийной группы ( NH3+), а основные — за счет ионизованной карбоксильной группы (—СОО- ), выступая амфолитами:
Как и все амфолиты, а-аминокислоты являются слабыми электролитами.
Согласно протолитической теории кислоты, основания и амфолиты являются протолитами, а процесс перехода протона от кислоты к основанию называется протолизом и объясняется тем, что эти два вещества имеют разное сродство к протону. В кислотно-основном взаимодействии всегда участвуют две сопряженные кислотно-основные пары, и переход протона всегда происходит в сторону образования более слабых кислот, включая сопряженные. Если склонность к взаимодействию с протоном у реагентов соизмерима, то наблюдается протолитическое равновесие.
Протолитическое, или кислотно-основное, равновесие устанавливается в результате конкуренции за протон (Н + ) между основаниями взаимодействующих сопряженных кислотно-основных пар (НА, А- и ВН + , В). Протолитическое равновесие всегда смещается в сторону образования более слабой кислоты:
Схематично протолитическое равновесие можно представить следующей схемой:
Переход протона всегда происходит от сильной кислоты каниону слабой кислоты, что сопровождается вытеснением слабой кислоты из ее соли под действием более сильной кислоты.
Протолитическое равновесие наблюдается при ионизации слабых электролитов в воде (разд. 7.2). Так, ионизация слабой кислоты в водных растворах является следствием конкуренции за протон между анионом слабой кислоты и водой, выступающей основанием, т. е. акцептором протона. Этот процесс является обратимым и характеризуется константой равновесия Ка:
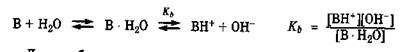 |
При взаимодействии слабого основания с водой последняя, выступая донором протона, способствует ионизации этого основания, носящей равновесный характер:
для слаоых электролитовсила кислот и оснований характеризуется величинами констант кислотности Каи основности Кbссоответственно (разд. 7.2). Если эти константы характеризуют протолитическое взаимодействие воды с кислотой или основанием одной сопряженной пары НА, А или ВН + , В, то произведение констант кислотности Ка и основности Kb, компонентов данной пары всегда равно ионному произведению воды Кн2о = 1 * 10 -14 (при 22 °С):
Эти выражения позволяют заменить в случае водных растворов константу основности Кь или показатель основности рКь слабого основания на константу кислотности Каили на показатель кислотности рКасопряженной кислоты этого основания. На практике для характеристики протолитических свойств соединения обычно используют величину рКа. Так, силу аммиака в воде как основания (pKb, = 4,76) можно охарактеризовать показателем кислотности иона аммония NH4+, т. е. сопряженной кислоты: рKа(NH4+) = 14 — 4,76 — 9,24. Поэтому в случае водных растворов нет необходимости в специальной таблице констант или показателя! основности, достаточно единой шкалы кислотности, представленной в табл. 8.1, где свойства оснований характеризуются констгантой Каили показателем кислотности рКаих сопряженных кислот. Самой сильной кислотой в водных растворах является ка-тион водорода Н + (точнее НзО + ), а самым сильным основанием -анион ОН-. Величина рКаколичественно характеризует силу слабьпх электролитов в водных растворах.
Слабая кислота тем слабее, чем больше значение ее рКа. Слабое основание тем слабее, чем меньше значение рКа его сопряженной кислоты.
Значение рКаравно значению рН водного раствора, в котоpoм данный слабый электролит ионизован на 50 %: поскольку в атом случае [А — ] = [НА], то Ка= [Н + ] и рКа= рН. Так, для уксусной кислоты в ее водном растворе с рН = рKа(СН3СООН) = = 4,76 имеет место равенство [СН3СОО-] = [СН3СООН], а для вод-Hoгo раствора аммиака равенство [NH4] = [NH3 ■ Н2О] будет наблюдаться в растворе с рН = рKа(NH4+) = 9,24.
Кроме того, значение рКапозволяет определить значение рН’ водных растворов, где данная слабая кислота НА находится преимущественно (99 % и более) в виде аниона (А») — это будет в растворах с рН > рКа + 2; или в виде молекул (НА) — в растворах с рН
studopedia.org — Студопедия.Орг — 2014-2019 год. Студопедия не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования (0.003 с) .
Теория Бренстеда-Лоури
В 1923 г. Бренстед и Лоури выдвинули новую теорию кислот и оснований, основанную на представлении о переносе протона. Согласно этой теории, кислота представляет собой вещество, состоящее из молекул или ионов-доноров протонов (т. к. они отдают протоны), а основание-вещество, состоящее из молекул или ионов-акцепторов протонов (т.к. они принимают протоны).
Чтобы подробнее разобраться в этой теории, начнем наше рассмотрение со случая сильной кислоты, как, например, соляная кислота. При растворении хлороводорода в воде его молекулы полностью диссоциируют, образуя ионы водорода H+ и хлорид-ионы Cl». Ионы водорода называют также протонами, поскольку каждый такой ион представляет собой просто протон. В растворе эти протоны связываются с молекулами воды, образуя ионы гидроксония H3O+. Растворение хлороводорода в воде может быть представлено с помощью уравнения
В случае слабой кислоты, как, например, уксусная кислота, молекулы кислоты лишь частично диссоциированы в водном растворе, так что в нем устанавливается равновесие
(1)
Но и в этом случае молекулы кислоты тоже донируют (передают) протоны молекулам воды.
Каждая молекула соляной кислоты и уксусной кислоты может донировать только по одному протону. Поэтому они называются однопротонными или одноосновными кислотами (последнее название объясняется тем, что каждая такая кислота имеет только одно сопряженное основание; см. ниже).
Кислота, способная донировать более одного протона, называется многопротонной или многоосновной. Например, серная кислота является двухпротонной, потому что она может донировать два протона. Ее называют также двухосновной, потому что она имеет два сопряженных основания, HSO4- и SO4-; процесс растворения серной кислоты в воде можно представить двумя уравнениями:
H2SO4(ж.) + H2O (ж.) = H3O+ (водн.) + HSO4 (водн.) или
H2SO4(ж.) + 2H2O(ж.) = 2H3O+ (водн.) + SO2.» (водн.)
Сильные основания, такие, как гидроксиды щелочных металлов, полностью ионизируются в воде:
NaOH(TB.) + H2O = Na+(водн.) + ОН- (водн.)
Эти вещества являются основаниями, потому что гидроксидные ионы могут акцептировать (присоединять) ионы водорода:
ОН- (водн.) + H3O+ (водн.) = 2H2O (ж.)
Эта реакция является общей для всех реакций нейтрализации между кислотами и основаниями в водных растворах. Отметим также, что в водных растворах ионы водорода существуют в гидратированной форме, т.е. в виде ионов гидроксония.
Рассмотрим теперь реакцию между слабым основанием аммиаком NH3 и хлоро-водородом в газовой фазе. В этой реакции происходит образование твердого хлорида аммония:
Реакция, обратная этой, называется реакцией термической диссоциации хлорида аммония. Аммиак представляет собой основание, потому что он акцептирует протон от хлороводорода. Однако следует обратить внимание на то обстоятельство, что в обсуждаемом равновесии не принимают участия ни вода, ни гидроксидные ионы. Таким образом, теория Бренстеда-Лоури охватывает и такие кислотно-основные реакции, которые осуществляются в отсутствие растворителя либо в присутствии неводного растворителя.
Если внимательнее присмотреться к каждому из обсуждавшихся выше равновесий, то обнаружится, что в равновесной смеси всегда присутствуют частицы четырех типов. Пользуясь представлениями теории Бренстеда-Лоури, нетрудно убедиться, что две из этих частиц являются кислотами, а две другие-основаниями. Например,
Эта равновесная смесь состоит из двух следующих сопряженных пар кислот и оснований:
Обратим внимание на то, что в каждой сопряженной паре кислота и основание отличаются друг от друга на один протон. Каждая кислота имеет свое сопряженное основание. Сильной кислоте всегда соответствует слабое сопряженное основание, а слабой кислоте — сильное сопряженное основание.
Основные положения протолитической теории кислот и оснований Бренстеда-Лоури
Кислоты – молекулы или ионы, способные в данной реакции отдавать катион водорода
Кислота – донор протонов
Основания – молекулы или ионы, способные в данной реакции присоединять протоны (акцепторы протонов)
Основания – акцепторы протонов.
С каждой кислотой сопряжено основание, в которое она переходит, теряя протоны.
Каждой кислоте соответствует свое основание и каждому основанию — своя кислота. Эту пару сопряженных веществ называют кислотно-основной или протолитической парой. Каждый отдельный компонент этой пары называется протолитом. Кислота и основание одной протолитической пары называются сопряженными протолитами (сопряженными кислотой и основанием).
Чем сильнее кислота, тем слабее сопряжённое с ней основание.
Согласно протонной теории кислоты подразделяют на 3 типа:
нейтр. к-та основание сопряжённая к-та сопряжённое основание
2) Катионные кислоты, представляющие собой положительные ионы, например NH4 + , H3O + :
3) Анионные кислоты, представляющие собой отрицательные ионы, например HSO4 — , H2PO4 — , HPO4 2- и др.
анионная к-та основание сопряжённая к-та сопряжённое основание
Подобного рода классификация имеется и для оснований:
2) Анионные основания, представляющие собой отрицательные ионы, например Cl — , CH3COO — , OH — :
3) Катионные основания, представляющие собой положительные ионы, например H2N-NH3 +
Связь между константой кислотности и константой основности в сопряженной протолитической паре.
К равновесию, которое устанавливается в растворе слабого электролита между молекулами и ионами, можно применить законы химического равновесия и записать выражение константы равновесия. Например, для электролитической диссоциации (протолиза) уксусной кислоты, протекающей под действием молекул воды,
константа равновесия имеет вид
| Кa = | [H3O + ][CH3COO – ]/ [CH3COOH] |
Здесь в числителе дроби стоят равновесные концентрации ионов — продуктов диссоциации, а в знаменателе — равновесная концентрация недиссоциированных молекул.
Константа протолитического равновесия, определяющая полноту протекания протолиза слабой кислоты при данной температуре, называется константой кислотности.
Аналогично для протолиза слабого основания
существует константа основности, определяющая полноту протекания протолиза слабого основания при данной температуре
| Кb = | [NH4 + ][OH – ]/ [NH3 · HOH] |
Величины Ка и Кb для сопряженной кислотно-основной пары связаны также простым соотношением.
Амфолиты.
Амфолиты — амфотерные электролиты, т. е. вещества, молекулы которых содержат одновременно и кислотные, и основные группы, и поэтому в водных растворах диссоциируют и как кислоты с отщеплением водородных ионов Н + , и как основания с отщеплением гидроксильных ионов ОН — .
К амфолитам относятся биологически важные вещества: аминокислоты , пептиды , белки и др. Кислотные свойства этих веществ обусловлены наличием в них карбоксильных групп СООН, а основные свойства — содержанием аминогрупп NH2. К амфолитам также относится вода.
Теория Льюиса.
Кислоты Льюиса – это молекулы или ионы, имеющие вакантные электронные орбитали, вследствие чего они могут акцептировать электронную пару. (пример – протон водорода, катионы металлов, оксиды некоторых неметаллов (SO3, SiO2), ряд солей (AlCl3 и др.))
Основания Льюиса – это молекулы и ионы, имеющие пару электронов, являющиеся донорами электронных пар. Примеры: все анионы, аммиак, вода, спирты, галогены и др.
Взаимодействие между кислотой и основанием заключается в образовании донорно-акцепторной связи между реагирующими частицами.
Принцип жестких и мягких кислот (ЖМКО).
Основан на теории Льюиса.
Жёсткие кислоты – это акцепторы электронной пары, обладающие малым размером, значительным положительным зарядом, большой электроотрицательностью и низкой поляризуемостью.
Примеры: протоны водорода, катиона лития, магния, калия, натрия, алюминия, хрома. Молекулы BF3, AlCl3 и др.
Жёсткие основания – донорные частицы с высокой электроотрицательностью, низкой поляризуемостью. Соединения прочно удерживают электроны.
Примеры: гидроксид-ион, фторид-ион, хлорид-ион, нитрат-ион, NH3, R-NH2, H2O, спирты, эфиры.
Мягкие кислоты – кислоты Льюиса, содержащие акцепторные атомы с малым положительным зарядом, большим размером, низкой электроотрицательностью, высокой поляризуемостью.
Примеры: Катионы серебра, меди (I), ртути, I + , Br +
Мягкие основания – основания Льюиса, содержащие донорные частицы с низкой электроотрицательностью, высокой поляризуемостью.
Слабо удерживают валентные электроны.
Примеры: I — , H — , C6H6, алкены
Суть принципа ЖМКО: жёсткие кислоты реагируют с жёсткими основаниями, мягкие кислоты – с мягкими основаниями.
Билет 18. Автопротолиз воды. Константа автопротолиза воды. Водородный показатель (pH) как количественная мера активной кислотности и основности. Определение активной концентрации ионов водорода.
Автопротолиз воды.
Автопротолиз – обратимый процесс образования равного числа катионов и анионов из незаряженных молекул жидкого индивидуального вещества за счет передачи протона от одной молекулы к другой.
Наличие водородных связей в жидкой воде объясняет её автопротолиз
Для воды характерна протолитическая амфотерность. Реакция самоионизации (автопротолиза) воды, в ходе которой протон от одной молекулы воды (кислоты) переходит к другой молекуле воды (основанию) описывается уравнением:
Константа равновесия для уравнения автопротолиза воды равна 1,82*10 -16
- http://helpiks.org/5-94184.html
- http://www.himikatus.ru/art/ch-act/0373.php
- http://studopedia.su/9_75064_protoliticheskaya-teoriya-brensteda-i-louri.html
- http://studfiles.net/preview/5807240/page:2/
- http://prosto-o-slognom.ru/chimia/25_kisloty_i_osnovaniya.html
- http://studopedia.org/1-7349.html
- http://www.himikatus.ru/art/ch-act/0373.php
- http://megalektsii.ru/s4359t7.html