Здесь читатель найдет ответ на вопрос о том, что такое горение. В этой статье мы рассмотрим этот процесс, ознакомимся с характеристиками и классификацией, изучим исторические сведения и определим место в природе и жизни человека. Также уделим внимание конкретным параметрам для определенных видов горения.
Когда человек слышит слово «горение», скорее всего, в его воображении возникает образ пламени, который охватывает что-либо. Этот процесс имеет исторически, даже эволюционно, огромное значение для человека.
Горение – химические процесс, в ходе которого исходный ряд веществ преобразуется в продукт сгорания. Это экзотермический тип реакции, при которой интенсивно выделяется тепло. Энергетические ресурсы, запасенные в веществах, участвующих в процессе горения, могут выделяться, принимать вид излучения света.
Ответив на вопрос о том, что такое горение, человек смог сделать его главным ресурсом, из которого мы до сих пор черпаем энергию. Около 90 % всех энергетических ресурсов, производимых на Земле людьми, выпадают на процессы сжигания ископаемых видов топлива. Однако в обозримом будущем (приблизительно до 2040 года) этот показатель снизится на 10 %. Это связано с истощением ресурсов Земли, которые не подлежат восстановлению, а также загрязнением мира, явлением глобального потепления.
Горение – химический процесс, обычно идущий по пути разветвленно-цепного механизма. Здесь прогрессирует самостоятельное ускорение благодаря теплу, которое выделяется в ходе реакций. Особенностями, которые выделяют горение, можно считать наличие больших показателей выделения тепла и потребность в относительно огромных ресурсах, необходимых для активации реакции. Эти два фактора напрямую влияют на скорость, при которой она будет проходить.
Исторические факты
Кислород был открыт в первых годах 1770-х. Совершили открытие К. Шееле и Дж. Пристли. До этого события существовала теория флогистона, которая утверждала, что тела, подвергающиеся процессу горения, обладают особым началом «флогистоном». Спустя пять лет — в 1775 г., Лавуазье доказал, что горючее вещество не обладает такими элементами, а только присоединяет к себе кислородные молекулы, черпаемые из воздуха.
Буркеном и Шуманном в 1928 году была рассмотрена задача о явлении диффузионного пламени. Они показали, что при наличии скорости сгорания веществ, участвующих в реакции, выше скорости подвода реагентов, поставляемых диффузией, зона горения становится тонкой до бесконечности. Это значит, что в такой области процессов происходит автоматическое установление стехиометрического соотношения между веществами, отвечающими за окисление, и горючими материалами. Максимальные температурные показатели приближаются к адиабатическим.
Теория горения в своем современном виде началась с трудов Н.Н. Семенова, который изучал явление теплового взрыва. Это произошло в 1920 году. Через восемнадцать лет, в 1938 году, Д.А. Франком-Каменецким была развита теория тепловых взрывов.
Уже в 1940 году была развита общая теория детонации – ZND. Ее основателем считается Я.Б. Зельдович. Название происходит от имен З. Неймана, Деринга и, собственно, Зельдовича. Это связано с тем, что независимо друг от друга исследователи пришли к схожим итогам и выводам на основе своих экспериментов и вычислений.
Классификационные данные
Сущность процесса горения позволяет классифицировать его в соответствии с определенными параметрами. Например, в зависимости от скорости сгорания веществ, его делят на детонацию и дефлаграцию. Последнее бывает ламинарным и турбулентным. Детонация – только турбулентная.
Если газ – это исходный и основной компонент смеси, которая горит, то реакцию можно назвать гомогенной. Этот процесс характеризуется взаимодействием окислителя и горючего вещества в газофазном горении. Разделение горючих веществ и их постепенное слияние, вызывающее рассматриваемый процесс, называют диффузией. Гетерогенной можно назвать реакцию, в которой окислители и горючее имеют разное положение фазы. Кроме перечисленного выше, выделяют: процесс тления, беспламенное, холоднопламенное и (термо)ядерное горение.
Отвечая на вопрос о том, что такое горение, человек смог выделить в нем явление пламени, которое представляет собой зону, излучающую свет и образующуюся в ходе реакций горения. Ее температурные показатели определяются составом смесей и условиями, при которых протекает процесс. Сгорание природных газов позволяет разгонять температуру до двух тысяч кельвинов и выше.
Пламя многих видов топлива, основанных на углеводородах, обладает способностью к взаимодействию с электромагнитными полями. Это обуславливается наличием собственных частиц в заряженном состоянии. Посредством проведения экспериментов было доказано, что количество ионов в пламени может превышать в шесть порядков концентрацию анионов и катионов в процессах чистой термической ионизации. Главный механизм, отвечающий за образование ионов, — хемоионизация. Это сложный физико-химический процесс, который превращает исходные в продукты сгорания. В ходе экзотермической реакции выделяется большое количество тепла.
Теория горения
Суть процесса горения, несмотря на большой практический опыт и применение, исследовалась в течение многих лет и остается одной из самых сложных загадок человечества. Наука, изучающая явление горения, является междисциплинарной и располагается на стыке газодинамики, химической термодинамики, химкинетики, молекулярной и химической физики, а также материаловедения и моделирования с использованием компьютерных технологий.
Рассмотрим следующие положения теории горения: полноту сгорания и его термодинамический механизм. Положение полноты сгорания включает в себя информацию о том, что исходные компоненты горючих смесей характеризуются молярной и массовой долей элемента, а также начальными показателями давления и температуры. Подобрав вещество, способное в ходе сгорания и окисления полностью превратиться в продукт рассматриваемого явления, можно получить стехиометрическую реакцию. Смесь, обладающая избытком горючего вещества, что не может полностью разложиться из-за нехватки окислителей, именуется богатой. Вещество с нехваткой топливного ресурса называют бедным.
Термодинамические данные позволяют нам утверждать, что горение, протекающее адиабатическим путем при наличии постоянного показателя объема, сохранит полную энергию внутренней системы. Если имеется постоянное давление, то наблюдается энтальпия структурных компонентов. Условия, при которых протекает адиабатическое давление, практически применяются и реализуются в пламени, что распространяется свободными путями. При этом расчетом теплопотери пренебрегают.
Гетерогенность
Гетерогенные процессы наблюдаются в случае, когда взаимодействуют несколько фаз (от двух). Это могут быть газы и жидкости. Такое же явление можно отслеживать в «территории» границы разделения между фазами. В терминологии это слово используют для описания процессов горения, в которых окислительное и горючее вещество пребывают в разных состояниях фазы. Сюда относится даже испарение топлива, происходящее в газовой форме. Ярким примером может послужить взаимодействие угля и кислорода, содержащегося в воздухе. В ходе этого образуется угарный газ, который может подвергаться дальнейшему сгоранию в состоянии газа и превращаться в CO2.
Твердое топливо
Что такое горение твердого топлива? Чаще всего это процесс окисления веществ, используемых в различных снарядах и патронах. Например, это может быть артиллерийский или реактивный снаряд. Другое применение находит себя в конструировании и эксплуатации межконтинентальных ракет баллистического типа. Многоразовые шаттлы выводятся на орбиту Земли посредством применения ускорителей, основанных на твердом топливе.
Те вещества, что используются в качестве топлива для ракет, делятся на две формы: смесевую и баллиститную. В первом случае разделение горючего вещества и окислителя не наблюдается, а сгорание происходит послойным способом. Их именуют гомогенным порохом. Главный компонент – это нитроцеллюлоза, которую добывают путем желатинизации в толще нитроглицерина.
Общие данные о сгорании твердого топлива
Процесс разложения пороха включает в себя несколько этапов, которые отличаются типом экзотермической реакции, а именно проходят в двух фазах газа и конденсации. Проведение опытов с горением баллиститных порохов в пространстве вакуума и при показателе давления ниже двух мм.рт.ст. показало, что экзотермические реакции происходят лишь в приповерхностном уровне фазы конденсации. При диапазоне давления от пяти до двадцати мм.рт.ст. можно увидеть пламя, но заметное только в темноте, а реакции протекают в газовом этапе.
Медленный тип горения
Процессам горения свойственно наличие тления, которое является его медленной формой. Поддержание такого явления осуществляется благодаря теплу, выделяемому в ходе взаимодействия O2 и горячего соединения в конденсированной форме, а реакции протекают на ее поверхности и подвергаются аккумулированию. Типичная ситуация, при которой наблюдается данное явление, — это тление сигареты. Здесь можно наблюдать медленное распространение вдоль материала. Нехватка высоты температуры обуславливает отсутствие газофазного пламени, а в ходе большой потери тепла сигарета начинает гаснуть. Чаще всего тление можно наблюдать в пористом или волокнистом ряде веществ.
Твердофазный тип горения
Существует явление, которое можно наблюдать в порошках неорганической и органической природы. Оно характеризуется автоволновой экзотермической реакцией, в ходе которой заметное выделение газа не наблюдается, но образуются продукты в конденсированной форме. Однако это конечный результат реакции, а в промежутках между фазами отслеживается создание газов или жидкостей.
Самостоятельно распространяющийся высокотемпературный синтез на практике основывается именно на безгазовом или твердопламенном горении. Ниже расскажем о том, как охарактеризовать слово «горение».
Сведения о слове
Разбор слова «горение» по составу показывает нам, что оно образуется с помощью:
- корня — гор;
- суффикса — ени;
- окончания — е.
Это три составных элемента, которые включены в общую структуру термина.
Чтобы ответить на вопрос о том, как пишется слово «горение», достаточно вслух сказать его. Произношение слова совпадает с правописанием. Гласными буквами, образующими эту языковую единицу, являются: «о», «и», «е». Ударение ставим на первую «е». Проверочное слово у «горения» отсутствует, однако можно определить правильность написания путем чередования гласных «а» и «о». Их варьирование подчиняется правилам правописания корней «гор» и «гар».
Подводя итоги
Анализируя полученную информацию, скажем, что слово «горение» означает химический процесс, взаимосвязанный с физическими явлениями. Он является главным источником энергии для всего населения планеты и основывается на сжигании различного вида топлив. Включает в себя множество разновидностей и имеет огромное значение для людей. Горение играло немаловажную роль в истории развития человечества, а детальное изучение его позволило стремительно расти технологическому процессу.
Изучением данного процесса занималось огромное множество ученых, а на достижение, систематизацию и обобщение всей информации ушло огромнейшее количество времени. Величайшие умы различных эпох и поколений совершили ценные вклады в общее развитие теории горения. Однокоренные с «горением» слова — это: горько, горы, горе, пригореть и прочее. Чаще всего гласная «о» пишется в корне тогда, когда на нее не падает ударение.
Глава 2 горение и средства тушения пожаров
2.1. Понятие о процессе горения
Горением называют физико-химический процесс, характеризующийся следующими признаками: химическими превращениями, выделением тепла и света. Для того чтобы возникло устойчивое горение, необходимо наличие трех факторов: горючего вещества (материала, смеси), окислителя и источника зажигания.
Химическая реакция горения, идущая с выделением значительного количества тепла, почти всегда сопровождается различного рода физическими явлениями. Так, в процессе горения происходит перенос тепла реагирующих веществ и продуктов горения из одного места в другое. Все процессы, происходящие в зоне реакции горения, взаимосвязаны — скорость химических реакций определяется уровнем теплопередачи и скоростью диффузии вещества и, наоборот, физические параметры (температура, давление, скорость переноса вещества) зависят от скорости химической реакции.
Горючее вещество. Все вещества и материалы, обращающиеся в производстве, используемые в качестве сырья, полуфабрикатов, строительных конструктивных элементов, подразделяются на три группы: негорючие, трудногорючие и горючие.
Негорючими называются вещества и материалы, не способные к горению в воздухе нормального состава. Негорючие вещества и материалы составляют значительную группу. К ним относятся все естественные и искусственные неорганические вещества и материалы, применяемые в строительстве металлы, а также гипсовые или гипсо-волокнистые плиты при содержании органической массы до 8%, минерало-ватные плиты на синтетической, крахмальной или битумной связке при содержании ее по массе до 6%.
Трудногорючими называются вещества (материалы), способные загораться под действием источника зажигания, но не способные самостоятельно гореть после его удаления. К ним относятся вещества и материалы, состоящие из негорючих и горючих составляющих, например: асфальтобетон, гипсовые и бетонные материалы, содержащие более 8% по массе органического заполнителя; минерало-ватные плиты на битумной связке при содержании ее от 7 до 15%; глиносоломенные материалы объемной массой не менее 900 кг/м 3 ; войлок, пропитанный глиняным раствором; древесина, подвергнутая глубокой пропитке антипиренами; цементный фибролит; отдельные виды конструкционных пластмасс и т. п.
Горючими называются вещества (материалы, смеси), способные к самостоятельному горению в воздухе нормального состава. К ним относятся все вещества и материалы, не отвечающие требованиям, предъявляемым к негорючим и трудногорючим веществам и материалам, например: авиационные топлива, спирты, органические и неорганические масла, декоративно-отделочные материалы на основе пластмасс, текстильные материалы, магний, натрий, сера и другие материалы и химические вещества.
В свою очередь, все горючие вещества и материалы подразделяются на три подгруппы: легковоспламеняющиеся, средней воспламеняемости, трудновоспламеняющиеся.
Легковоспламеняющимися называются вещества (материалы, смеси), способные воспламеняться от кратковременного воздействия пламени спички, искры, накаленного электрического провода и тому подобных источников зажигания с низкой энергией.
Среднюю воспламенимость имеют вещества (материалы, смеси), способные воспламеняться от длительного воздействия источника зажигания с низкой энергией.
Трудновоспламеняющимися называются вещества (материалы, смеси), способные воспламеняться только под воздействием мощного источника зажигания, который нагревает значительную часть вещества до температуры воспламенения.
К подгруппе легковоспламеняющихся веществ и материалов в первую очередь относятся газы и легковоспламеняющиеся жидкости.
К легковоспламеняющимся жидкостям (ЛВЖ) из всех жидкостей, обращающихся в производстве, относятся горючие жидкости с температурой вспышки, не превышающей + 61° С в закрытом тигле. Они делятся на три разряда:
I — особо опасные ЛВЖ с температурой вспышки до — 18° С;
II — постоянно опасные ЛВЖ с температурой вспышки от — 18 до 23° С;
III — ЛЖВ, опасные при повышенной температуре воздуха или жидкости с температурой вспышки от 23° до 61° С.
Температурой вспышки называется самая низкая (в условиях специальных испытаний) температура горючего вещества, при которой над его поверхностью образуются пары или газы, способные вспыхивать в воздухе от источника зажигания, но скорость их образования еще недостаточна для устойчивого горения. Для ЛВЖ температура вспышки на 1 —5° С ниже температуры воспламенения.
Температурой воспламенения называется температура горючего вещества, при которой оно выделяет горючие пары и газы с такой скоростью, что после воспламенения их от источника зажигания возникает устойчивое горение.
Практически все горючие и трудногорючие вещества и материалы горят в паровой или газовой фазе, исключение составляют титан, алюминий, антрацит и ряд других. Горючие вещества и материалы могут различаться по химическому составу, агрегатному состоянию другим свойствам, исходя из чего процессы подготовки их к горению протекают по-разному. Газы вступают в реакцию горения If Практически без каких-либо изменений, так как их перемешивание с окислителем (кислородом воздуха) происходит при любых температурах среды и не требует значительных дополнительных затрат f энергии. Жидкости должны сначала испариться и перейти в парообразное состояние, на что затрачивается определенное количество тепловой энергии, и только в паровой фазе перемешиваются с окислителем и горят. Твердые вещества и материалы при своей подготовке к горению требуют значительно большее количество энергии, так как сначала они должны либо расплавиться, либо разложиться. Расплавленные или разложившиеся вещества и материалы должны испариться и перемешаться с окислителем, после чего под воздействием источника зажигания возникает процесс горения. Каучук, резина и другие пластические материалы, а также магний и его, сплавы перед воспламенением плавятся и испаряются (при этом пластмассы разлагаются). Такие материалы, как бумага, древесина, хлопчатобумажные ткани и отдельные виды конструкционных пластмасс при нагревании разлагаются с образованием газообразных продуктов и твердого остатка (как правило, угля).
Окислитель. Окислителем обычно служит кислород воздуха. Воздух по своему составу представляет собой смесь многих газов, основными из которых являются: азот (N2)— 78,2% по объему и 75,5% по массе; кислород (О2) — 20,9% по объему и 23,2% по массе; инертные газы (Не, Ne, Аг, Кг) — 0,9% по объему и 1,3% по массе. Помимо данных газов в воздушном объеме всегда присутствует незначительное количество углекислого газа, водяных паров и пыли. Все эти составляющие воздуха, кроме кислорода, при горении органических веществ и материалов в реакцию горения практически не вступают. Кислород, азот и инертные газы считаются постоянными составными частями воздуха. Содержание же углекислого газа, водяных паров и пыли непостоянно и может изменяться в зависимости от условий, в которых протекает тот или иной процесс горения.
Источник зажигания. Им может быть горящее или накаленное тело, а также электрический разряд, обладающие запасом энергии и температурой, достаточными для возникновения горения других веществ.
На практике существуют или возникают различные явления, повышающие температуру веществ и материалов, находящихся в производстве или на хранении, что в большинстве случаев приводит к возникновению процесса горения как локально, так и во всем объеме горючего вещества или материала. К источникам зажигания относятся: искры, образующиеся при ударах металла о металл или другие твердые материалы; искры и капли расплавленного металла при коротких замыканиях в электрооборудовании и при производстве сварочных и других огневых работ; нагрев электрических проводов при перегрузках электрических сетей; механический нагрев трущихся деталей машин, биологический нагрев при окислении растительных масел и ветоши, смоченной этими маслами; горящие спич, окурки и т. п. Характер воздействия этих источников зажигания неодинаков. Так, искры, образующиеся при ударах металлических предметов, как источник зажигания имеют весьма малую мощность и способны воспламенить только газопаровоздушные смеси: метано-воздушную, ацетиленовоздушную, сероуглеродно-воздушную и др. Искры, возникающие при коротких замыканиях в электрооборудовании или при электросварке, обладают мощной воспламеняющей способностью и могут вызвать горение практически всех горючих веществ и материалов независимо от их агрегатного состояния.
Горючая среда. При возникновении и протекании процесса горения горючее вещество и окислитель являются реагирующими веществами и представляют собой горючую среду, а источник зажигания является стартером процесса горения. При установившемся горении источником зажигания еще не горящих веществ и материалов служит теплота, выделяющаяся из зоны реакции горения.
Горючие среды могут быть физически однородными (гомогенными) и неоднородными (гетерогенными). К первым относятся среды, в которых горючее вещество и окислитель (воздух) равномерно перемешаны: смеси горючих газов, паров и пылей с воздухом. Примерами горения однородной среды могут служить: горение паров, поднимающихся со свободной поверхности жидкости (разлитого авиатоплива ТС-1 при авиационном происшествии); горение газа, вытекающего из поврежденного баллона или трубопровода; взрывы газо-, паро- и пылевоздушных смесей. К гетерогенным относятся среды, в которых горючее вещество (материал) и окислитель не перемешаны и имеют поверхность раздела: твердые горючие вещества и материалы, струи горючих газов и жидкостей, поступающие в воздух под высоким давлением, и т. п. Примером горения неоднородной среды является горение титана, алюминия, антрацита или нефтяных и газовых фонтанов, когда нефть и газ поступают, в зону горения под большим давлением и имеют весьма значительные скорости истечения.
Пламя. Пространство, в котором сгорают пары, газы и взвеси, называется пламенем. Пламя может быть кинетическим или диффузионным в зависимости от того, горит ли заранее подготовленная смесь паров, газов или пыли с воздухом или такая смесь образуется непосредственно в зоне пламени в процессе горения. Процессы, протекающие в кинетическом пламени, характеризуются высокими скоростями протекания реакции горения (линейная скорость распространения пламени может превышать 1000 м/с) и, как правило, представляют собой взрыв горючей среды, сопровождающийся высоким уровнем тепловыделения и резким повышением давления в зоне горения.
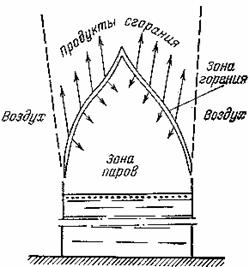
В условиях пожара практически все газы, пары, жидкости и твердые вещества и материалы горят диффузионным пламенем. Структура данного пламени существенно зависит от сечения потока горючих паров или газов и его скорости. По характеру этого потока различают ламинарное и турбулентное диффузионное пламя. Первое возникает при малых сечениях потока горючих паров или газов, движущихся с небольшой скоростью (пламя свечи, спички, газа в горелке домашней плиты и т. п.). На пожарах при горении различных веществ и материалов образуется турбулентное диффузионное пламя, минарное и турбулентное пламя представляет собой зону реакции горения, которая окружает зону паров или газов, последняя практически занимает весь объем зоны горения. Зона реакции горения иффузионном пламени представляет очень тонкий (всего несколько микрометров) слой, в котором происходит выделение тепла и светурбулентное пламя в отличие от ламинарного характеризуется I, что не имеет четких очертаний, постоянных сечений и положений фронта пламени.
Температура в зоне паров значительно ниже, чем в зоне реакции.
В пламени авиационных топлив температура потока паров около поверхности жидкости приближается к температуре ее кипения (для авиатоплива ТС-1 эта температура лежит в пределах 150 — 280° С). По мере движения потока паров к зоне реакции их температура повышается сначала за счет теплового излучения пламени, а затем — диффузии из зоны реакции нагретых продуктов сгорания. В результате нагрева происходит термическое разложение (диссоциация) парообразных веществ, и образующиеся свободные атомы и радикалы совместно с продуктами сгорания поступают непосредственно в зону реакции, т. е. в пламя. Атомы углерода, поступая в зону реакции горения, нагреваются и начинают светиться, образуя так называемое светящееся пламя. Температура зоны реакции горения меняется по высоте пламени. В нижней части пламени температура снижается за счет расхода значительного количества тепла на нагрев массы холодного воздуха, поступающего в зону горения, и является минимальной для каждого вида горения. Наибольшая температура развивается в средней части пламени, поскольку в верхней скорость реакции уменьшается за счет падения концентрации реагирующих компонентов (выгорания), в связи с чем падает уровень тепловыделения и снижается температура.
Парциальное давление кислорода воздуха в нормальных условиях равно 228,72 кПа, а в зоне реакции горения — 0, поэтому в результате разности парциальных давлений кислород из окружающего воздуха диффундирует (фильтруется, просачивается) через слой продуктов сгорания к зоне реакции. Поступление же в зону реакции горения горючих компонентов практически ничем не ограничивается. Таким образом, скорость реакции горения при развившемся процессе зависит в основном только от количества кислорода, поступающего в зону реакции, т. е. от скорости его диффузии. В случае горения неоднородной среды проникновению кислорода в зону реакции также препятствуют продукты сгорания, выделяющиеся в пространство, примыкающее к зоне реакции.
Отсутствие достаточного количества кислорода в зоне реакции горения тормозит скорость ее протекания. Если бы этого торможения не происходило, то все реакции горения, происходящие в атмосфере, протекали бы с постоянно возрастающей скоростью и заканчивались взрывом реагирующих веществ. Процессы горения, как и все химические процессы, протекают с различными скоростями, зависящими от условий, в которых они протекают, от природы реагирующих веществ, от их агрегатного состояния. Например, взрывчатые вещества разлагаются в тысячные доли секунды, а химические процессы в земной коре длятся сотни и тысячи лет. Взаимодействие веществ в газовой и паровой фазах протекают значительно быстрее, чем в жидком, а тем более твердом состоянии. Так, разлитое авиационное топливо ТС-1 сгорает относительно медленно, образуя коптящее пламя (неполное сгорание), а подготовленная паровоздушная смесь этого топлива с воздухом сгорает со взрывом. Скорость взаимодействия твердых веществ и материалов с окислителем резко изменяется в зависимости от степени их измельченное. Например, алюминий и титан, медленно горящие в слитках, при наличии особых условий могут образовывать в пылевидном состоянии взрывоопасные пылевоздушные смеси, развивающие при горении давления взрыва соответственно в 0,62 и 0,49 МПа.
Горение как химический процесс во всех случаях происходит одинаково. Однако как физический процесс оно отличается по характеру протекания реакции горения, поэтому процессы горения в начальной стадии делятся на следующие виды: самовозгорание, воспламенение и самовоспламенение.
Самовозгорание. Отдельные вещества (материалы, смеси) при хранении и в процессе эксплуатации технологического оборудования способны самовозгораться. Самовозгорание — это явление резкого увеличения скорости экзотермических реакций, приводящее к возникновению горения вещества в отсутствии источника загорания. К веществам, способным самовозгораться, относятся растительные и жирные масла, тряпки и ветошь, смоченные растительными маслами, сульфиды железа и другие индивидуальные химические вещества. Растительные и жирные масла (подсолнечное, льняное, конопляное, кукурузное, животные жиры и т. п.) относятся к классу жиров и представляют собой смесь глицеридов высокомолекулярных жирных кислот. Молекулы этих кислот имеют ненасыщенные (двойные) связи, способствующие при определенных условиях самовозгоранию данных веществ. Согласно перекисной теории А. Н. Баха окисление может происходить за счет присоединения кислорода к метиленовой группе, находящейся в положении по отношению к двойной связи, с образованием гидроперекиси. Как известно, все перекиси и гидроперекиси — нестойкие химические соединения. При их распаде образуются свободные радикалы, полимеризующиеся в более крупные органические молекулы. При полимеризации всегда выделяется определенное количество тепла, что в конечном результате может привести к самовозгоранию окисляющегося органического вещества. Самовозгорание органических веществ возникает при определенных условиях. К ним относятся: содержание в масле или жире глицеридов высокомолекулярных кар боковых кислот не ниже определенного минимального количества; наличие большой поверхности контакта с окислителем и малой теплоотдачи; определенное соотношение жиров и масел я пропитанного ими пористого или волокнистого материала.
Сульфиды железа FeS, Fe2S3 могут образовываться в технологическом оборудовании складов службы ГСМ авиапредприятий. Они способны самовозгораться на воздухе, особенно в присутствии горючиx паров и газов. Рассмотрим механизм соединения сульфидов железа с кислородом воздуха на примере реакции окисления природного соединения пирита FeS2:
Помимо сульфидов железа могут самовозгораться такие материалы, как бурый уголь, торф, продукты растительного происхождения: сено, солома, силосная масса и др.
Наиболее опасным является самовозгорание индивидуальных, химических веществ при их неправильном хранении, поскольку этот процесс может привести к пожару на объекте, где хранятся данные вещества. Эти вещества по своим химическим свойствам делятся на три группы: самовозгорающиеся при контакте с воздухом, с водой и друг с. другом.
Вещества, относящиеся к первой группе, мы не рассматриваем, поскольку они практически не встречаются в технологии авиапредприятий.
Ко второй группе относится ряд веществ, из которых наибольший интерес представляют карбид кальция СаС2 и окись кальция СаО. При взаимодействии с водой карбида кальция происходит выделение ацетилена, являющегося горючим газом, и значительного количества тепла. При относительно малом количестве воды система карбид кальция — вода может разгореться до 920 К, что может вызвать взрыв ацетиленовоздушной смеси:
Помимо карбида кальция, способностью разогреваться до температуры свечения при попадании на нее небольших количеств воды обладает окись кальция СаО, что также может привести к загоранию тары и сгораемых конструктивных элементов помещения склада:
К третьей группе относятся сильные окислители, индивидуальные Химические вещества, а также органические вещества и материалы. Например, нельзя совместно хранить такие вещества, как перманганат калия и глицерин; концентрированную азотную кислоту со скипидаром, этиловым спиртом и сероводородом; галогены с горючими ,газами и легковоспламеняющимися жидкостями; серную кислоту с селитрами, хлоратами, перхлоратами, так как в этом случае между ними возможна химическая реакция, идущая с выделением большого количества тепла.
Воспламенение. Помимо самовозгорания возможно просто возгорание, т. е. возникновение горения под воздействием источника зажигания. Возгорание, сопровождающееся появлением пламени, называется воспламенением. При этом происходит нагрев объема, прилегающего к точке теплового воздействия. В результате повышения температуры в указанном объеме происходит распространение тепла на граничащие с ним участки (объемы) горючей среды. Чем большее количество горючего вещества (материала, смеси) вовлекается в процесс горения, тем больше тепла выделяется в окружающее пространство. Таким образом, процесс горения развивается самопроизвольно. Источник зажигания в данном случае первоначально нагревает только малый объем горючей смеси, в то время как температура всего объема горючей среды может оставаться неизменной.
Процесс воспламенения различается по своему характеру в зависимости от вида горючей смеси. Наиболее опасными являются газовоздушные смеси. Однако и для них минимальная энергия источника воспламенения зависит от многих параметров, основными из которых являются процентный состав смеси, вид горючего вещества, давление смеси, поскольку от этих величин зависят температура воспламенения, нормальная скорость распространения пламени и температура горения. Помимо этого на минимальную температуру источника воспламенения оказывает влияние продолжительность его контакта с горючей средой.
Воспламенение жидкостей возможно лишь в том случае, если температура окружающей среды или самой жидкости достаточна для испарения такого количества паров, которое необходимо для возникновения устойчивого горения. Для различных горючих жидкостей эта температура неодинакова. При температурах ниже температуры воспламенения горение невозможно, так как скорость испарения той или иной жидкости в данном случае слишком мала. С ростом температуры наружного воздуха или самой горючей жидкости при прочих равных условиях испаряемость жидкостей растет и количество паров становится достаточным для возникновения устойчивого горения.
Самовоспламенение. Им называется самовозгорание, сопровождающееся появлением пламени. Помимо процессов самовозгорания и воспламенения в практике встречается также процесс самовоспламенения различных горючих сред. По своей химической природе все эти три процесса не отличаются друг от друга. Разница между ними лежит в физической сущности процесса горения, так как в отличие от процессов самовозгорания и воспламенения процесс самовоспламенения идет сразу во всем объеме реагирующей горючей среды. С точки зрения физики, это кинетический процесс горения уже перемешанной и подготовленной смеси, идущий с высокими скоростями распространения пламени. При горении паро-, пыле- и газовоздушных смесей это, как правило, скорости взрыва. Для возникновения процесса самовоспламенения необходимо, чтобы весь объем горючей смеси имел температуру самовоспламенения данной смеси. Под температурой самовоспламенения понимают самую низкую температуру вещества (материала, смеси), при которой происходит резкое увеличение скорости экзотермических реакций, заканчивающееся возникновением пламенного горения. Температура самовоспламенения горючего вещества не является постоянной величиной. Она зависит от скоростей тепловыделения и теплоотвода, которыё в свою очередь зависят от объема смеси, концентрации, давления и других факторов. Температура самовоспламенения смесей горючих паров и газов с воздухом изменяется в зависимости от их процентного состава. Самая низкая температура самовоспламенения у стехиометрической смеси или смесей, близких к ней по концентрациям реагирующих веществ. Температура самовоспламенения твердых веществ или материалов находится в обратной зависимости от степени их измельчения: чем выше степень измельченности вещества, тем ниже его температура самовоспламенения. Это связано с тем, что с измельчением веществ и материалов резко возрастает площадь контактной поверхности этих горючих компонентов и окислителя.
∀ x, y, z
| Главная ≫ Инфотека ≫ Химия ≫ Что такое огонь и горение |
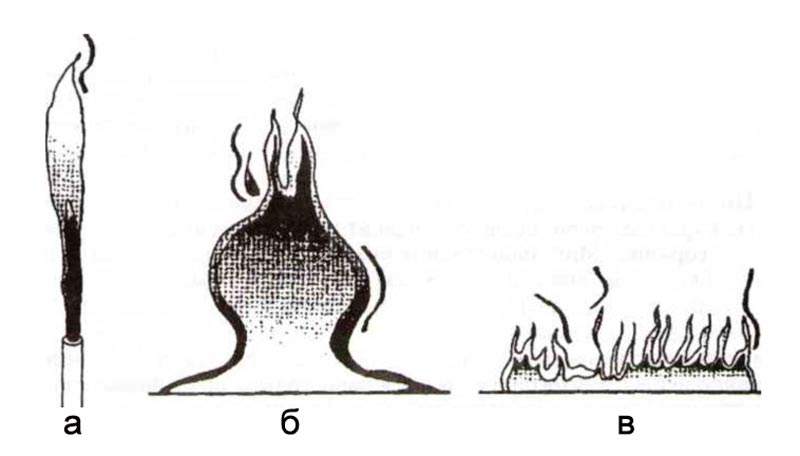
Что такое огонь и горениеЧто именно мы называем огнем? То, что мы привыкли видеть в очаге, на самом деле представляет собой очень сложную совокупность различных физико-химических процессов. Их объединяет то, что все они в той или иной форме участвуют в реакции окисления, сопровождающейся бурным выделением тепла и излучения. Соответственно, чтобы понять, что такое огонь, все эти процессы стоит обсудить по отдельности, к чему мы и приступим. Вспомним, что химическими реакциями называются процессы, в которых образуются новые вещества. Это может происходить несколькими путями: с существенным изменением электронной структуры атомов, участвующих в реакции, и без изменения их структуры. Второй случай более простой — к нему относятся в основном обменные реакции, когда молекулы передают друг другу целые блоки, при этом не изменяя их состав и строение. К таким реакциям относится, например, гашение соды уксусом. Реакции с более существенным изменением электронной структуры протекают сложнее и зачастую гораздо более бурно. В них обязательно должны участвовать два вещества: окислитель и восстановитель, которые условно обмениваются между собой электронами. В результате этого сильно меняется строение связей: из менее выгодной конфигурации они перестраиваются в более выгодную (это и движет реакцию вперед), а «лишняя» энергия высвобождается в виде тепла и излучения. Не все окислительно-восстановительные реакции протекают именно так, но реакция горения, которая нас больше всего интересует, идет по такому пути. Итак, что же требуется для нормального течения реакции горения? Прежде всего, сами окислитель и восстановитель. Первым в обычных условиях чаще всего является кислород — O2. Два атома в этой молекуле прочно связаны между собой, но энергетически они «предпочитают» связываться с атомами других элементов. Если им предоставить такую возможность (ввести в контакт с топливом), произойдет бурная реакция. То, что мы обычно называем топливом, или горючим (дрова, бензин, торф и т.п.), с точки зрения химии называется восстановителем, с которым прочно связываются атомы кислорода. Некоторые вещества могут воспламениться при контакте с кислородом даже при комнатной температуре — металл калий, например. Однако для большинства видов горючего необходимо также нагреть его. На молекулярном уровне высокая температура означает, что все атомы двигаются очень быстро, что позволяет им легче приблизиться друг к другу на достаточное расстояние (и столкнуться с достаточной силой), чтобы вступить в реакцию. Если бы процесс горения ограничивался вышеперечисленным, он бы не играл настолько важной роли в жизни природы и человека. Что делает его исключительным, так это цепной механизм, по которому протекает эта реакция. Представим другой известный пример окисления — ржавление железа. Оно протекает достаточно медленно, и существует лишь малый риск, что крошечной пятно ржавчины быстро расползется по всему образцу. Однако реакция горения железа (есть и такая!) протекает совсем не так: тонкая железная «вата», или опилки, помещенные в атмосферу чистого кислорода, вспыхивают и за несколько мгновений полностью сгорают. Так происходит потому, что тепло, выделяющееся в ходе реакции, подогревает материал, позволяя ему легче вступать в реакцию с кислородом. Кроме того, многие нестабильные промежуточные соединения, образующиеся в ходе горения, приводят к очень быстрому распространению пламени. Кстати, для некоторых смесей (кислорода и водорода, например) этот процесс приводит к практически мгновенной реакции, которую мы называем взрывом. Остался лишь один необходимый элемент реакции горения: продукты, которые получаются в ходе этого процесса. Во многих случаях при сгорании топлива образуются газообразные вещества (углекислый газ, угарный газ, оксиды азота), некоторые из них уже не могут окисляться дальше. Оставаясь в зоне реакции, они только мешают процессу, так как не дают новым молекулам кислорода вступить в контакт с топливом. В большинстве случаев на Земле эта проблема решается благодаря наличию гравитации и конвективным процессам в атмосфере: все это способствуют постоянному перемешиванию в зоне реакции и обогащению ее кислородом. Совсем не так обстоят дела в космосе, где горение затухает мгновенно, даже если гипотетически рядом еще остался кислород: продукты реакции настолько плотно окружают зону реакции, что цепной процесс прерывается. Подведем промежуточные итоги: горение основывается на совокупности сложных процессов, каждый из которых критичен для быстрого и стабильного протекания реакции. Все факторы вместе часто объединяют в «пожарный тетраэдр», гранями которого являются кислород (или другой окислитель), горючее вещество, температура и существование цепной реакции. Все методы тушения пожаров и защиты от огня так или иначе работают за счет удаления одной из граней пожарного тетраэдра. Именно этим фактом мы воспользуемся, чтобы понять, как работают несгораемые материалы. Простая логика подсказывает нам: чтобы материал был огнеупорным, он просто не должен вступать в реакцию горения. Эта идея широко применяется на практике, но не все оказывается так просто. Например, большинство строительных огнеупорных материалов по химическому составу представляет собой оксиды и их смеси, то есть уже максимально окисленные вещества. Кислород попросту не может прореагировать с таким соединением, поэтому горения не происходит. В реальности, однако, в условиях пожара присутствует много поражающих факторов, и сам факт сгорания — лишь один из них. К другим относится, конечно, очень высокая температура. Из-за этого даже негорючий материал может существенно ухудшить свою структуру и даже разрушиться, хотя технически он не вступал в реакцию горения. По этой причине обязательным свойством современных огнезащитных материалов является защита от высоких температур. Собственно, эта характеристика в сочетании с устойчивостью к открытому пламени и является основным параметром при оценке того или иного материала. Как обеспечить защиту от высокой температуры? На этом поприще, к сожалению, велосипед не изобретешь: теплоизоляция (что от высоких, что от низких температур) в абсолютном большинстве случаев основывается на воздушной прослойке или «чистой» толщине покрытия. Часто эти факторы сочетаются, поэтому важной характеристикой огнеупорных материалов является их пористость. Для носимой одежды в этом случае используется та же идея, что в зимних пуховиках: лучшим теплоизолятором является материал очень малой плотности, например вата. Важно упомянуть, что химическая стойкость материалов срабатывает не только в случае пожара, но и в контакте с другими едкими веществами, хотя и не всегда огнезащиты оказывается достаточно, чтобы «удержать» сильные кислоты, например. В этом случае материал должен быть дополнен другими химически стойкими включениями. По этой и другой причинам современная огнезащита подразумевает использование сложных композитов, в которых разные материалы отвечают за разные поражающие факторы. Простейшим примером огнеупора может считаться кирпич, сделанный из смеси оксидов и силикатов, обладающих высокой химической инертностью. Подобные материалы широко применяются в промышленности для строительства плавильных печей, котлов и прочего. На основе твердых оксидных материалов создаются и волокнистые огнеупоры, пригодные для изготовления пористых (минеральная вата) и гибких материалов (шнуры, одеяла, одежда). Другой веткой развития волокнистых огнеупорных материалов занимается химия полимеров, а наибольших успехов в этой области удалось добиться арамидным волокнам (больше известным под маркой Kevlar). Благодаря наличию в своей структуре бензольных колец и амидных связей, такие материалы обладают существенной термостойкостью, не плавятся и начинают разлагаться лишь при температурах около 500 градусов Цельсия. При соответствующей обработке арамидные волокна кратковременно выдерживают и более высокие температуры, а также открытое пламя. Именно арамидные ткани лежат в основе наиболее современных носимых огнезащитных материалов. Так, в НИТУ «МИСиС» недавно был создан костюм, предназначенный для пожарных и всех, кто работает в условиях чрезвычайной ситуации. Материал костюма представляет собой «сэндвич» из трех слоев, каждый из которых защищает от определенных поражающих факторов. Внешний слой — это арамидная ткань, дополнительно пропитанная составом для герметизации и придания водоотталкивающих свойств. Это материал обеспечивает защиту от пламени температурой до 1200 градусов Цельсия, а в случае попадания на костюм концентрированных кислот или щелочей препятствует их впитыванию за счет гидрофобного покрытия. Следующий слой отвечает за теплоизоляцию, благодаря чему костюм может использоваться как при низких, так и при высоких температурах, до 800 градусов в условиях пожара. Наконец, внутренний слой защищает человека в том случае, если работа ведется в присутствии сильных электромагнитных полей. Эта разработка практически не имеет аналогов в мире: материал основан на магнитных порошках из сплавов кобальта, никеля, железа и стронция. Эти дисперсии наносят на арамидные волокна, из которых изготавливаются вставки, защищающие жизненно-важные органы от внешних полей. Немалую роль здесь играет сочетание магнитожестких и магнитомягких соединений. Примером совершенно другого по характеру огнеупорного материала является графит. Несмотря на то, что по составу он представляет собой чистый углерод, который горит с образование углекислого газа, графит очень плохо поддерживает горение. Вместо того чтобы быстро вспыхнуть, он неторопливо тлеет, а интенсивно сгорает лишь при постоянных температурах около 1000 градусов Цельсия. Это свойство само по себе делает графит привлекательным материалом для огнеупоров. Кроме того, графит обладает уникальной структурой: в нем атомы углерода образуют массив шестиугольников, которые упакованы друг на друге слоями. Из-за этого графит очень хрупок и часто существует в виде порошков (чешуек). Этот же факт позволил создать на его основе высокопористый материал — пенографит. Способ его получения заслуживает отдельного разговора. Благодаря своему слоистому строению, графит способен удерживать внутри себя включения посторонних веществ. Такое соединение — интеркалированный графит — получается, например, при взаимодействии порошка графита с серной или азотной кислотами. Если полученное вещество резко нагреть, заключенные внутри кислотные остатки превратятся в газообразные продукты и в буквальном смысле разорвут слои графита на мелкие фрагменты. Эта реакция впечатляюще выглядит и чем-то напоминает извержение вулкана: из небольшого количества порошка при нагревании получается огромная шапка густой графитовой пены. Пенографит сочетает в себе сразу несколько свойств, идеально подходящих для огнеупоров: во-первых, он в большой степени химически инертен и плохо поддерживает горение. Во-вторых, за счет высокой пористости он работает как теплоизолятор благодаря заключенным в порах газам. Все эти свойства широко используются в огнезащитных покрытиях на основе пенографита. В простейшем случае в строительную краску добавляется порошок интеркалированного графита, который в случае пожара значительно расширяется и образует медленно тлеющую пену. Такой материал, конечно, одноразовый, однако в случае возгорания он надежно защищает конструкцию от пламени и температуры в течение длительного времени, за которое пожар можно успеть потушить. Чем дальше, тем все более сложными и «умными» становятся огнеупорные материалы. На смену кирпичам приходят волокнистые композиты, а вместо старых добрых огнезащитных пропиток разрабатываются продвинутые высокотехнологичные покрытия на основе очень непростой химии. По словам Андрея Игнатова, одного из разработчиков вышеупомянутого костюма для пожарного, созданию широко используемых огнезащитных материалов препятствует сегодня не нехватка современных технологий, а их высокая стоимость. Однако химики, физики и технологи неустанно работают над снижением их стоимости, а нам остается только ждать. Не горит. Что такое горение с точки зренияГОРЕНИЕ — физико химический процесс, при котором превращение вещества сопровождается интенсивным выделением энергии и тепло и массообменом с окружающей средой. Горение может начаться самопроизвольно в результате самовоспламенения либо быть инициированным… … Большой Энциклопедический словарь ГОРЕНИЕ — ГОРЕНИЕ, горения, мн. нет, ср. (книжн.). Действие и состояние по гл. гореть. Горение газа. Душевное горение. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова горение — блеск, переливы, энтузиазм, сияние, игра, взлет, душевный подъем, подъем духа, сверкание, блистание, одержимость, огонь, страсть, огонек, воодушевление, поблескивание, вдохновение, увлеченность, живинка, увлечение, сгорание, подъем Словарь… … Словарь синонимов Горение — ГОРЕНИЕ, химическое превращение, которое сопровождается интенсивным выделением тепла и тепло и массообменом с окружающей средой. Может начаться самопроизвольно (самовозгорание) или в результате зажигания. Характерное свойство горения способность… … Иллюстрированный энциклопедический словарь ГОРЕНИЕ — сложная хим. реакция, протекающая в условиях прогрессивного самоускорения, связанного с накоплением в системе теплоты или катализирующих продуктов реакции. При Г. могут достигаться высокие (до неск. тыс. К) темп ры, причём часто возникает… … Физическая энциклопедия Горение — физико химический процесс, при котором превращение вещества сопровождается интенсивным выделением энергии и тепло массообменом с окружающей средой. может начаться самопроизвольно в результате самовоспламенения либо может быть инициировано… … Словарь черезвычайных ситуаций горение — Экзотермическая реакция окисления вещества, сопровождающаяся по крайней мере одним из трех факторов: пламенем, свечением, выделением дыма. [СТ СЭВ 383 87] горение Экзотермическая реакция, протекающая в условиях ее прогрессивного самоускорения.… … Справочник технического переводчика горение — ГОРЕТЬ, рю, ришь; несов. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова Горение — (фр. и англ. combustion, нем. Verbrennung; хим.). Принятоназывать Г. такие случаи взаимодействия с кислородом воздуха каких бы тони было тел, которые сопровождаются значительным выделением тепла, аиногда и света. В более общем смысле можно… … Энциклопедия Брокгауза и Ефрона ГОРЕНИЕ — букс. Жарг. угол. 1. Неизбежная опасность. ТСУЖ, 42. 2. Сигнал тревоги, опасности. ББИ, 58. Скачинский, 29; Балдаев 1, 92 … Большой словарь русских поговорок Характеристика процесса горенияВсем нам практически ежедневно приходится сталкиваться с тем или иным проявлением процессом горения. В нашей статье мы хотим более подробно рассказать какие особенности включает в себя данный процесс с научной точки зрения. Горение является основной составляющим процессом на пожаре. Пожар начинается с возникновения горения, его интенсивность развития как правило путь пройденный огнем, то есть скорость горения, а тушение заканчивается прекращением горения. Под горением обычно понимают экзотермическую реакцию между горючим и окислителем, сопровождающуюся, по крайней мере, одним из трех следующих факторов: пламенем, свечением, дымообразованием. Из-за сложности процесса горения указанное определение не является исчерпывающим. В нем не учтены такие важнейшие особенности горения, как быстрое протекание лежащей в его основе экзотермической реакции, ее самоподдерживающийся характер и способность к самораспространению процесса по горючей смеси. Различие между медленной экзотермической окислительно-восстановительной реакцией (коррозия железа, гниение) и горением заключается в том, что последняя протекает настолько быстро, что теплота производится быстрее, чем рассеивается. Это приводит к повышению температуры в зоне реакции на сотни и даже тысячи градусов, к видимому свечению и образованию пламени. По сути так образуется пламенное горение.Если происходит выделение тепла но пламя при это отсутствует, то этот процесс называется тлением.И в том и в другом процессе происходит образование дыма – аэрозоля полного или неполного сгорания веществ. Стоит отметить, что при горении некоторых веществ пламени не видно, а также отсутствует и выделение дыма, к таким веществам относится водород. Слишком быстрые реакции (взрывчатое превращение) также не входят в понятие горения. Необходимым условием для возникновения горения является наличие горючего вещества, окислителя (при пожаре его роль выполняет кислород воздуха) и источника зажигания. Для непосредственного возгорания необходимо наличие критических условий по составу горючей смеси, геометрии и температуре горючего материала, давлению и др. После возникновения горения в качестве источника зажигания выступает уже само пламя или зона реакции. Например, метан способен окисляться кислородом с выделением тепла до метилового спирта и муравьиной кислоты при 500-700 К. Однако, чтобы реакция продолжилась, необходимо пополнение теплоты за счет внешнего подогрева. Горением это не является. При нагревании реакционной смеси до температуры выше 1000 К скорость окисления метана возрастает настолько, что выделяющегося тепла становится достаточно для дальнейшего продолжения реакции, необходимость в подводе теплоты извне исчезает, начинается горение. Таким образом, реакция горения, возникнув, способна сама себя поддерживать. Это главная отличительная особенность процесса горения. Другая, связанная с ней особенность — способность пламени, являющегося зоной химической реакции, самопроизвольно распространяться по горючей среде или горючему материалу со скоростью, определяемой природой и составом реакционной смеси, а также условиями процесса. Это основной механизм развития пожара. Типичная модель горения построена на реакции окисления органических веществ или углерода кислородом воздуха. Множество физических и химических процессов сопровождают горение. Физика это перенос тепла в систему. Окислительные и восстановительные реакции это составляющая природы горения со стороны химии. Отсюда из понятия горение вытекают самые разные химические превращения, включая разложение исходных соединений, диссоциации и ионизации продуктов. Совокупность горючего вещества или материала с окислителем представляет собой горючую среду. В результате разложения горючих веществ под воздействием источника зажигания происходит образование газопаровоздушной реакционной смеси. Горючие смеси, которые по составу (соотношению компонентов горючего и окислителя) отвечают уравнению химической реакции, называются смесями стехиометрического состава. Они наиболее опасны в пожарном отношении: легче воспламеняются, интенсивнее горят, обеспечивая полное сгорание вещества, в результате чего выделяют максимальное количество теплоты. Рис. 1. Формы диффузионных пламен а – горение реактивной струи, б – горение разлитой жидкости, в – горение лесной подстилки По соотношению количества горючего материала и объема окислителя различают бедные и богатые смеси: бедные содержат в изобилии окислитель, богатые — горючий материал. Минимальное количество окислителя, необходимое для полного сгорания единицы массы (объема) того или иного горючего вещества, определяется по уравнению химической реакции. При горении с участием кислорода требуемый (удельный) расход воздуха для большинства горючих веществ находится в пределах 4-15 м 3 /кг. Горение веществ и материалов возможно только при обусловленном содержании в воздухе их паров или газообразных продуктов, а также при концентрации кислорода не ниже заданного предела. Так, для картона и хлопка самопотухание наступает уже при 14 об. % кислорода, а полиэфирной ваты — при 16 об. %. В процессе горения, как и в других химических процессах, обязательны два этапа: создание молекулярного контакта между реагентами и само взаимодействие молекул горючего с окислителем с образованием продуктов реакции. Если скорость превращения исходных реагентов определяется диффузионными процессами, т.е. скоростью переноса (пары горючих газов и кислорода переносятся в зону реакции за счет градиента концентраций в соответствии с законами диффузии Фика), то такой режим горения называется диффузионным. На рис. 1 приведены различные формы диффузионных пламен. При диффузионном режиме зона горения размыта, и в ней образуется значительное количество продуктов неполного сгорания. Если же скорость горения зависит только от скорости химической реакции, которая значительно выше скорости диффузии, то режим горения называется кинетическим. Ему свойственны более высокие скорости и полнота сгорания и как следствие высокие скорости тепловыделения и температура пламени. Этот режим имеет место в предварительно перемешанных смесях горючего и окислителя. Отсюда, если реагенты в зоне химической реакции находятся в одинаковой (обычно газовой) фазе, то такое горение называют гомогенным, при нахождении горючего и окислителя в зоне реакции в разных фазах — гетерогенным. Гомогенным является горение не только газов, но и жидкостей, а также большинства твердых веществ и материалов. Объясняется это тем, что в зоне реакции горят не сами материалы, а их пары и газообразные продукты разложения. Наличие пламени является отличительным признаком гомогенного горения. Примерами гетерогенного горения служат горение углерода, углистых остатков древесины, нелетучих металлов, которые даже при высоких температурах остаются в твердом состоянии. Химическая реакция горения в этом случае будет происходить на поверхности раздела фаз (твердой и газообразной). Отметим, что конечными продуктами горения могут быть не только оксиды, но и фториды, хлориды, нитриды, сульфиды, карбиды и др. Характеристики процесса горения разнообразны. Их можно подразделить на следующие группы: форма, размер и структура пламени; температура пламени, его излучательная способность; тепловыделение и теплота сгорания; скорость горения и концентрационные пределы устойчивого горения и др. Всем известно, что при горении образуется свечение которое сопровождает пламя продукта горения. Рассмотрим две системы:
В первом случае при возникновении горения весь процесс будет происходить в пламени, во втором же случае часть реакций будет происходить в самом материале, либо его поверхности. Как упоминалось выше существуют газы которые могут гореть без пламени, но если рассматривать твердые вещества существуют также группы металлов которые также способны гореть без проявления пламени. Часть пламени с максимальным значением, где происходят интенсивные превращения, называется фронтом пламени. Теплообменные процессы и диффузия активных частиц из зоны горения которые являются ключевыми механизмами движения фронта пламени по горючей смеси. Скорость распространения пламени принято разделять на:
Рис. 2. Ламинарное диффузионное пламя В зависимости от характера скорости движения газового потока, создающего пламя, различают ламинарные и турбулентные пламена. В ламинарном пламени движение газов происходит в разных слоях, все процессы тепло-, массоообмена происходят путем молекулярной диффузии и конвекции. В турбулентных пламенах процессы тепло-, массообмена осуществляются в основном за счет макроскопического вихревого движения. Пламя свечи — пример ламинарного диффузионного пламени (рис. 2). Любое пламя высотой более 30 см будет уже обладать случайной газовой механической неустойчивостью, которая проявляется видимыми завихрениями дыма и пламени. Рис. 3. Переход ламинарного потока в турбулентный Очень наглядным примером перехода ламинарного потока в турбулентный является струйка сигаретного дыма (рис. 3), которая, поднявшись на высоту около 30 см, приобретает турбулентность. При пожарах пламена имеют диффузионный турбулентный характер. Присутствие турбулентности в пламени усиливает перенос тепла, а смешивание влияет на химические процессы. В турбулентном пламени выше также скорости горения. Это явление делает затруднительным перенос поведения мелкомасштабных пламен на крупномасштабные, имеющих большую глубину и высоту. Экспериментально доказано, что температура горения веществ в воздухе гораздо ниже температуры горения в атмосферной кислородной среде В воздухе температура будет колебаться от 650 до 3100 °С, а в кислородной показатели температуры возрастут на 500-800 °С. |
- http://studfiles.net/preview/6154100/page:8/
- http://forany.xyz/a-463
- http://dic.academic.ru/dic.nsf/ruwiki/75603
- http://fireman.club/statyi-polzovateley/xarakteristiki-processa-goreniya/