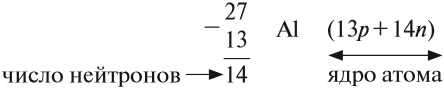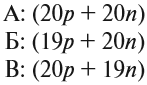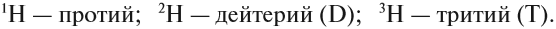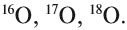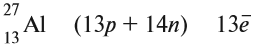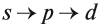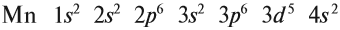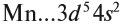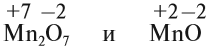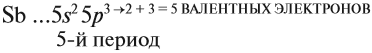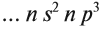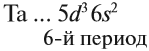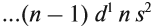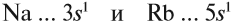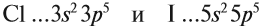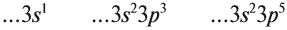К пемрвому перимоду периодимческой системмы относятся элементы первой строки (или первого периода) периодической системы химических элементов. Первый период содержит меньше всего элементов (их всего два: водород и гелий) по сравнению с другими строками таблицы. Данное положение объясняется современной теорией строения атома.
Порядковый номер: 1
Массовое число: 1
Число протонов: 1
число нейтронов: 0
Энергетических уровней: 1
Порядковый номер: 2
Массовое число: 4
Число протонов: 2
число нейтронов: 2
Энергетических уровней: 1
Ко второму периоду периодической системы относятся элементы второй строки (или второго периода) периодической системы химических элементов. Второй период содержит больше элементов, чем предыдущий, в него входят: литий, бериллий, бор, углерод, азот, кислород, фтор и неон.
Порядковый номер: 3
Массовое число: 7
Число протонов: 3
число нейтронов: 4
Энергетических уровней: 2
Порядковый номер: 4
Массовое число: 9
Число протонов: 4
число нейтронов: 5
Энергетических уровней: 2
Порядковый номер: 5
Массовое число: 11
Число протонов: 5
число нейтронов: 6
Энергетических уровней: 2
Порядковый номер: 6
Массовое число: 12
Число протонов: 6
число нейтронов: 6
Энергетических уровней: 2
Порядковый номер: 7
Массовое число: 14
Число протонов: 7
число нейтронов: 7
Энергетических уровней: 2
Порядковый номер: 8
Массовое число: 16
Число протонов: 8
число нейтронов: 8
Энергетических уровней: 2
Порядковый номер: 9
Массовое число: 19
Число протонов: 9
число нейтронов: 10
Энергетических уровней: 2
Порядковый номер: 10
Массовое число: 20
Число протонов: 10
число нейтронов: 10
Энергетических уровней: 2
К третьему периоду периодической системы относятся элементы третьей строки (или третьего периода) периодической системы химических элементов. Третий период содержит восемь элементов (как и предыдущий), в него входят: натрий, магний, алюминий, кремний, фосфор, сера, хлор и аргон. Первые два из них, натрий и магний, входят в s-блок периодической таблицы, тогда как остальные относятся к р-блоку. Следует обратить внимание, что 3d-орбитали у элементов не заполнены до 4 периода, что даёт периодам таблицы их характерный вид «две строки в одной».
Порядковый номер: 11
Массовое число: 23
Число протонов: 11
число нейтронов: 12
Энергетических уровней: 3
Порядковый номер: 12
Массовое число: 24
Число протонов: 12
число нейтронов: 12
Энергетических уровней: 3
3) Аллюминий — Al
Порядковый номер: 13
Массовое число: 27
Число протонов: 13
число нейтронов: 14
Энергетических уровней: 3
Порядковый номер: 14
Массовое число: 28
Число протонов: 14
число нейтронов: 14
Энергетических уровней: 3
Порядковый номер: 15
Массовое число: 31
Число протонов: 15
число нейтронов: 16
Энергетических уровней: 3
Порядковый номер: 16
Массовое число: 32
Число протонов: 16
число нейтронов: 16
Энергетических уровней: 3
Порядковый номер: 17
Массовое число: 35,5
Число протонов: 17
число нейтронов: 18,5
Энергетических уровней: 3
Порядковый номер: 18
Массовое число: 40
Число протонов: 18
число нейтронов: 22
Энергетических уровней: 3
К четвёртому периоду периодической системы относятся элементы четвёртой строки (или четвёртого периода) периодической системы химических элементов. Четвёртый период содержит восемнадцать элементов (на десять элементов больше, чем предыдущий), в него входят: калий, кальций, скандий, титан, ванадий, хром, марганец, железо, кобальт, никель, медь, цинк, галлий, германий, мышьяк, селен, бром и криптон. Первые два из них, калий и кальций, входят в s-блок периодической таблицы, десять следующих являются d-элементами, а остальные относятся к р-блоку. Следует обратить внимание, что заполненные 3d-орбитали появляются только у элементов 4 периода. Все элементы этого периода имеют стабильные изотопы, все они встречаются в природе.
Теперь установим более точно, в какой зависимости от строения электронных оболочек находятся химические свойства атомов. При этом необходимо учитывать не только число электронов в атомах и их распределение по слоям, но и относительные размеры атомов, о которых дает представление рис. 48.
Рассмотрим вначале изменение свойств в периодах. В пределах каждого периода (кроме первого) металлические свойства, наиболее резко выраженные у первого члена периода, при переходе к последующим членам постепенно ослабевают и уступают место металлоидным свойствам: в начале периода стоит типичный металл, в конце—типичный металлоид и за ним инертный газ.
Закономерное изменение свойств элементов в периодах может быть объяснено следующим образом. Как уже указывалось, наиболее характерным свойством металлов с химической точки зрения является способность их атомов легко отдавать внешние электроны и превращаться в положительно заряженные ионы, тогда как металлоиды, наоборот, характеризуются способностью присоединять электроны с образованием отрицательных ионов.
Рис. 48. Относительные размеры атомов.
Для отрыва электрона от атома с превращением последнего в положительный ион нужно затратить некоторую энергию, которая называется энергией ионизации и выражается обычно в килограммкалориях на грамматом элемента.
Энергию ионизации определяют путем бомбардировки атомов, находящихся в электрическом поле, быстро летящими электронами. То наименьшее напряжение поля, при котором скорость электронов становится достаточной для ионизации атомов, называется потенциалом ионизации атомов данного элемента и выражается в вольтах.
Энергия ионизации связана с потенциалом ионизации простым соотношением, что позволяет выражать легкость потери электронов атомами как в килограммкалориях на грамматом, так и в вольтах.
Потенциал ионизации имеет наименьшее значение у элементов, начинающих период, т. е. у водорода и щелочных металлов, и наибольшее — у элементов, заканчивающих период, т. е. инертных газов. Величина его может служить мерой большей или меньшей «металличности» элемента: чем меньше потенциал ионизации, чем легче оторвать электрон от атома, тем сильнее должны быть выражены металлические свойства элемента.
Величина потенциала ионизации зависит от трех причин: от величины заряда ядра, от радиуса атома и от особого рода взаимодействия между электронами в электрическом поле ядра, вызванного их волновыми свойствами. Очевидно, что чем больше заряд ядра и чем меньше радиус атома, тем сильнее притягивается электрон к- ядру, тем больше потенциал ионизации.
У элементов одного и того же периода при переходе от щелочного металла к инертному газу заряд ядра постепенно возрастает, а радиус атома уменьшается. Следствием этого и является постепенное увеличение потенциала ионизации и ослабление металлических свойств. У инертных газов, хотя радиусы их атомов больше, чем радиусы атомов галогенов, стоящих в том же периоде, потенциалы ионизации больше, чем у галогенов. В этом случае сильно сказывается действие третьего из вышеупомянутых факторов — взаимодействия между электронами, вследствие чего внешняя электронная оболочка атома инертного газа имеет особую энергетическую устойчивость и удаление из нее электрона требует значительно большей затраты энергии.
Присоединение электрона к атому металлоида, превращающее его электронную оболочку в устойчивую оболочку атома инертного газа, сопровождается выделением энергии. Величина этой энергии при расчете на 1 грамматом элемента служит мерой так называемого сродства к электрону. Чем больше сродство к электрону, тем легче атом присоединяет электрон. Сродство атомов металлов к электрону равно нулю, — атомы ме таллов неспособны присоединять электроны. У атомов же металлоидов сродство к электрону тем больше, чем ближе к инертному газу стоит металлоид в периодической системе. Поэтому в пределах периода металлоидные свойства усиливаются по мере приближения к концу периода.
Переход от металлических свойств к металлоидным у элементов малых периодов связан также с изменением числа наружных электронов в их атомах, которое равномерно растет, начиная с одного в первом члене периода и доходя до восьми в последнем. В то же время понижается способность атомов отдавать электроны (проявление металлических свойств) и появляется способность к присоединению электронов (металлоидные свойства).
Опыт показывает, что, начиная с лития, атомы, имеющие в наружном слое небольшое число электронов (меньше четырех), могут только отдавать электроны, но никогда не присоединяют их. Таковы атомы элементов, которые мы называем металлами. Наоборот, атомы с большим числом наружных электронов, хотя и могут отдавать электроны, но гораздо легче присоединяют их, и тем легче, чем больше электронов уже имеется в наружном слое. Этим свойством обладают атомы металлоидов.
В больших периодах изменение свойств в общем происходит так же, как и в малых, только металлические свойства ослабевают гораздо медленнее. Причина этого лежит в неравномерном росте наружного электронного слоя, так как, начиная с третьего члена периода и вплоть до конца первой его половины, идет пополнение электронами предпоследнего недостроенного слоя, а в атомах редкоземельных элементов, находящихся в шестом периоде, заполняется даже не предпоследний, а третий снаружи слой. Поэтому все элементы первой половины периода имеют в наружной оболочке атома не больше двух электронов и характеризуются преобладанием металлических свойств (сродство к электрону равно нулю). Радиусы атомов этих элементов уменьшаются на небольшую величину, а потенциалы ионизации почти не возрастают, вследствие чего и ослабление металлических свойств происходит медленно. Только во второй половине периода число наружных электронов растет так же последовательно, как и в малых периодах, и металлические свойства постепенно сменяются металлоидными. Период заканчивается инертным газом.
Указанные выше соотношения между строением атомов и их химическими свойствами представляют глубокий интерес. Мы видим, что на химические свойства атома оказывают влияние главным образом электроны наружного слоя. Строение предпоследнего слоя влияет на химические свойства значительно меньше. Так, например, элементы больших периодов, в атомах которых идет достройка предпоследнего электронного слоя, сравнительно
мало отличаются друг от друга по своему химическому характеру (например, Cr, Mn, Fe, Со, Ni). Ho все же по мере заполнения электронами предпоследнего слоя свойства элементов изменяются в определенном направлении. Наконец, почти полное сходство свойств редкоземельных элементов показывает, что изменение числа электронов в третьем снаружи слое атома оказывает лишь ничтожное влияние на его химические свойства. Однако и здесь увеличение числа электронов вызывает постепенное, хотя и небольшое изменение свойств, проявляющееся, например, в понижении силы оснований от элемента № 58 (церия) к элементу № 71 (лютецию).
Как известно, все элементы расположены в таблице так, что они образуют девять вертикальных столбцов (групп). Номер группы соответствует наибольшей положительной валентности (или так называемой валентности по кислороду), которую могут проявлять элементы данной группы. Сопоставляя эту величину с расположением электронов в атомах, нетрудно убедиться, что у всех элементов, стоящих в малых периодах (кроме кислорода и фтора), наибольшая валентность как раз равна числу электронов в наружном слое атома.
Несколько иначе обстоит дело в больших периодах. В атомах элементов, находящихся в малых периодах, число электронов в предпоследнем слое равно двум или восьми. Отдавая наружные электроны, эти атомы превращаются в ионы с устойчивой структурой инертных газов и, естественно, не могут больше терять электроны. В больших же периодах только первые два члена имеют по восемь электронов в предпоследнем слое. В атомах следующих за ними элементов число электронов в предпоследнем слое постепенно растет, пока не достигнет 18 (у первого члена второй половины периода). Но слой из 18 электронов оказывается почти таким же устойчивым, как и слой из восьми электронов. Поэтому атомы, имеющие восемнадцать электронов в предпоследнем слое (например, Сu, Zn, Ga и др.), потеряв наружные электроны, тоже превращаются в ионы с устойчивой оболочкой. Таким образом, максимальная валентность атомов второй половины каждого большого периода, имеющих в предпоследнем слое 18 электронов (так же как и валентность атомов с двумя или восьмью электронами в предпоследнем слое), равна числу электронов наружного слоя .
Что же касается остальных элементов больших периодов, содержащих в предпоследнем слое больше восьми, но меньше 18 электронов, то они могут отдавать, кроме наружных электро-нов еще и часть электронов предыдущего слоя, а именно столько,
Исключение составляют медь, серебро и золото, максимальная валентность которых равна двум и трем, хотя наружный слой содержит только один электрон.
чтобы остающиеся электроны образовали устойчивую восьми-электронную оболочку. Например, элемент скандий (№ 21) может отдать всего три электрона, титан — четыре, ванадий — пять и т. д. Общее число отдаваемых электронов и определяет максимальную валентность этих элементов, указываемую номером соответствующей группы .
Еще задолго до возникновения учения о строении атома было установлено, что между максимальной валентностью элемента по кислороду и его валентностью по водороду существует определенная зависимость: сумма валентностей по кислороду и по водороду всегда оказывается равной восьми.
Эта зависимость очень просто объясняется с точки зрения электронны представлений о валентности. Так как в соединениях с кислородом атомы всех элементов (за исключением фтора) заряжены положительно, а в соединениях с водородом — отрицательно, то валентность по кислороду есть не что иное, как положительная валентность, обусловленная потерей или смеще; нием валентных электронов; наоборот, валентность по водороду есть отрицательная валентность, которую атом проявляет, присоединяя к наружному слою недостающее до восьми число электронов. Понятно, что сумма этих двух валентностей должна равняться восьми.
Нужно, однако, заметить, что это правило распространяется только на металлоиды, образующие газообразные соединения с водородом.
Некоторые металлы тоже образуют соединения с водородом, но не газообразные, а твердые. В соединениях такого типа металл заряжен положительно, а водород отрицательно. В этом случае валентность по водороду является положительной валентностью и, конечно, одинакова с валентностью того же металла по кисло-
Как уже указывалось , элементы каждой, группы периодической системы, начиная с четвертого горизонтального ряда, делятся на две подгруппы: четную, составленную из элементов, у которых преобладают металлические свойства, и нечетную, образованную элементами, у которых металлические свойства ослаблены или преобладают металлоидные свойства.
Различие в свойствах элементов четных и нечетных подгрупп непосредственно вытекает из строения их атомов. В то время как в наружном слое атомов элементов четных подгрупп никогда не бывает больше двух электронов, в атомах элементов нечетных подгрупп число наружных электронов может доходить до семи. Поэтому элементы четных подгрупп не присоединяют электроны, что характеризует их как металлы.
Нечетные подгруппы тоже содержат металлы, но главным образом состоят из элементов, легко присоединяющих электроны, т. е. металлоидов.
Усиление металлических свойств с увеличением порядкового номера у элементов главных подгрупп тоже легко объясняется строением их атомов. Хотя с увеличением порядкового номера заряд ядра и увеличивается, но одновременно возрастает число электронных слоев в атоме и их отталкивающее действие на наружные электроны. Значительно увеличиваются также радиусы атомов, вследствие чего потенциалы ионизации, а следовательно, и металлоидные свойства элементов уменьшаются.
Вы читаете, статья на тему Свойства элементов от строения атомов
1.2. Строение атома. Периодическая система химических элементов д.И. Менделеева.
Периодичность свойств элементов и
Между положением элемента в периодической системе и строением атома этого элемента существует взаимно-однозначное соответствие, т.е. координаты элемента в периодической системе определяют строение атома и наоборот, по строению атома можно определить его положение в периодической системе.
Для каждого элемента в периодической системе существует пять характеристик: порядковый номер Z, атомная масса А, номер периода, номер группы и подгруппа (главная или побочная). С точки зрения строения атома порядковый номер показывает число протонов в ядре. Атомная масса даёт сумму масс всех частиц атома: протонов, нейтронов и электронов. Учитывая, что масса электрона мала по сравнению с массой протона и нейтрона округлённо можно определять атомную массу, как сумму масс протонов и нейтронов. Отсюда легко найти число нейтронов в ядре как разность атомной массы и числа протонов: А – Z. Атом электронейтрален, поэтому число электронов в электронной оболочке равно числу протонов в ядре, т.е. порядковому номеру элемента – Z.
Номер периода показывает число энергетических электронных уровней в атоме.
Номер группы показывает общее число «валентных» электронов, т.е. электронов, которые могут принимать участие в образовании химических связей. Положение элемента в подгруппе (главной или побочной) определяется распределением «валентных» электронов: если элемент расположен в главной подгруппе, то все его валентные электроны находятся на последнем энергетическом электронном уровне, а все предыдущие уровни заполнены. Если элемент расположен в побочной подгруппе, то все остальные валентные электроны находятся на предпоследнем энергетическом уровне.
Существует форма записи энергетических состояний электронов в атоме, которая называется электронной формулой. В ней главное квантовое число обозначается цифрой (1, 2, 3, 4…), орбитальное – буквой (s-, p-, d-, f-), а число электронов на каждом подуровне показывается индексом вверху, например, электронная формула атома азота 
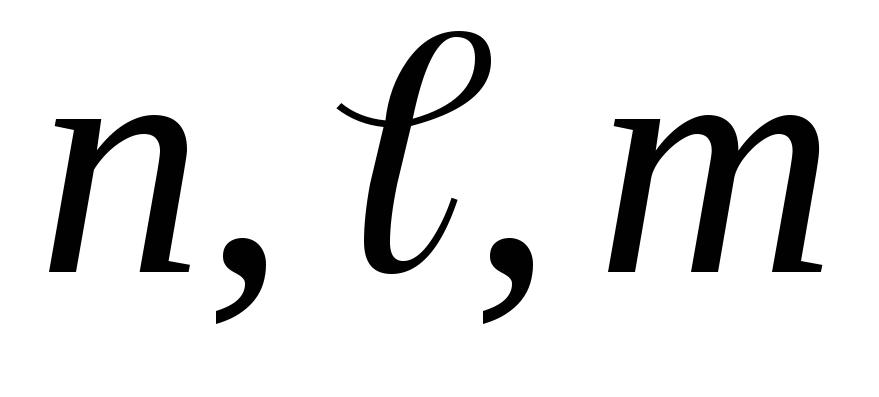
Основным или нормальным состоянием атома называется состояние, отвечающее минимальному запасу энергии, т.е. электроны занимают энергетические состояния с меньшей энергией. С небольшой затратой энергии (например, при воздействии светового излучения) электроны могут переходить в пределах одного энергетического уровня на более высокий энергетический подуровень. Атом переходит в «возбуждённое» состояние, например, для атома бериллия:
Строение внешних электронных уровней определяет формы и свойства его соединений. Например, для атома № 22 Ti имеем электронную формулу 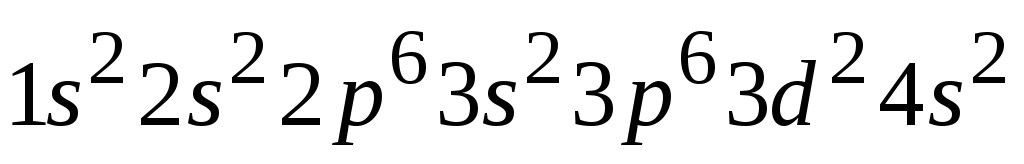
Ti имеет всего четыре валентных электрона, поэтому высшая степень окисления +4.
Оксид, отвечающий этой степени окисления – TiO2, имеет амфотерный характер (с преобладанием основных свойств), поэтому соответствующий ему гидроксид может быть записан в двух формах: Ti(OH)4 или H2TiO3, соответственно он образует соли при взаимодействии и с кислотами и со щелочами:
Ti(OH)4 + 2Н2SO4
Ti(OH)4 + 2НCl 
Низшая степень окисления Ti (как у большинства d–элементов) +2. Оксид TiО имеет основный характер, гидроксид Ti(OH)2 образует соли только с кислотами, например, TiSO4 или TiCl2.
Для характеристики любого элемента необходимо выполнить следующие действия:
Определить состав атома, т.е. указать число протонов, нейтронов и электронов.
Дать электронную формулу атома и распределение электронов внешних энергетических уровней по атомным орбиталям.
Определить высшую и низшую степень окисления и привести формулы и названия соединений, отвечающих данным степеням окисления.
Например, элемент № 34 Se.
Состав атома: (34 p, 46 n) 34 e.
Электронная формула: 1s 2 2s 2 2р 6 3s 2 3p 6 3d 10 4s 2 4p 4 – это p–элемент.
Высшая степень окисления +6, оксид селена (VI) SeO3 – кислотный, гидроксид H2SeO4 — селеновая кислота, соли: Na2SeO4 — cеленат натрия, K2SeO4 — селенат калия.
Низшая степень окисления -2, H2S — селеноводород, K2Se — селенид калия, Na2Se — селенид натрия.
Свойства элементов, определяемые строением внешних электронных слоев атомов, закономерно изменяются по периодам и группам периодической системы. При этом сходство электронных структур порождает сходство свойств элементов–аналогов, но не тождественность этих свойств. Поэтому при переходе от одного элемента к другому в группах и подгруппах наблюдается не простое повторение свойств, а их более или менее ярко выраженное закономерное изменение. В частности, химическое поведение атомов элементов проявляется в их способности терять и приобретать электроны, т.е. в их способности к окислению и восстановлению. Количественной мерой способности атома терять электроны является потенциал ионизации(Еи), а мерой способности их приобретать – сродство к электрону (Ес). Характер изменения этих величин при переходе от одного периода к другому повторяется, причем в основе этих изменений лежит изменение электронной конфигурации атома. Так, завершенные электронные слои, соответствующие атомам инертных газов, обнаруживают повышенную устойчивость и повышенное значение потенциалов ионизации в пределах периода. В то же время наименьшими значениями потенциала ионизации обладают s–элементы первой группы (Li, Na, K, Rb, Cs).
Электроотрицательность является мерой способности атома данного элемента оттягивать на себя электроны по сравнению с атомами других элементов в соединении. Согласно одному из определений (Малликен), электроотрицательность атома 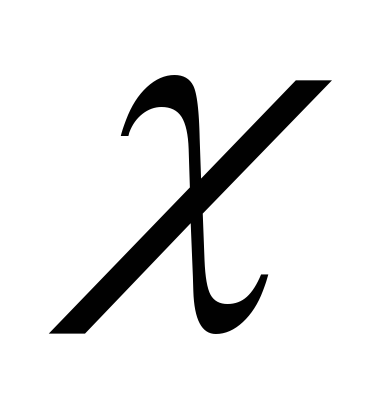
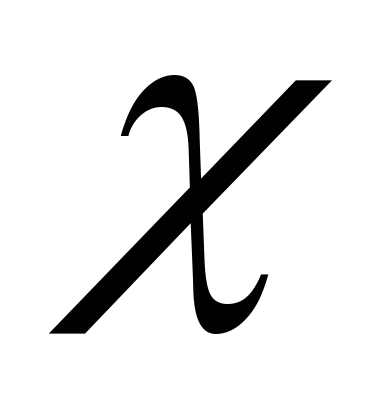

В периодах наблюдается общая тенденция роста электроотрицательности элемента, а в подгруппах – ее снижение. Наименьшими значениями электроотрицательности обладают s–элементы I группы, а наибольшими – р–элементы VII группы.
Электроотрицательность одного и того же элемента может меняться в зависимости от валентного состояния, гибридизации, степени окисления и пр. Электроотрицательность существенно влияет на характер изменения свойств соединений элементов. Так, например, серная кислота проявляет более сильные кислотные свойства, чем ее химический аналог – селеновая кислота, поскольку в последней центральный атом селена из-за меньшей по сравнению с атомом серы электроотрицательности не так сильно поляризует связи Н–О в кислоте, что и означает ослабление кислотности.
Н

Другой пример: гидроксид хрома (II) и гидроксид хрома (VI). Гидроксид хрома (II), Cr(OH)2, проявляет основные свойства в отличие от гидроксида хрома (VI), Н2CrO4, поскольку степень окисления хрома +2 обусловливает слабость кулоновского взаимодействия Cr 2+ с гидроксид-ионом и легкость отщепления этого иона, т.е. проявление основных свойств. В то же время высокая степень окисления хрома +6 в гидроксиде хрома (VI) обусловливает сильное кулоновское притяжение между гидроксид-ионом и центральным атомом хрома и невозможность диссоциации по связи 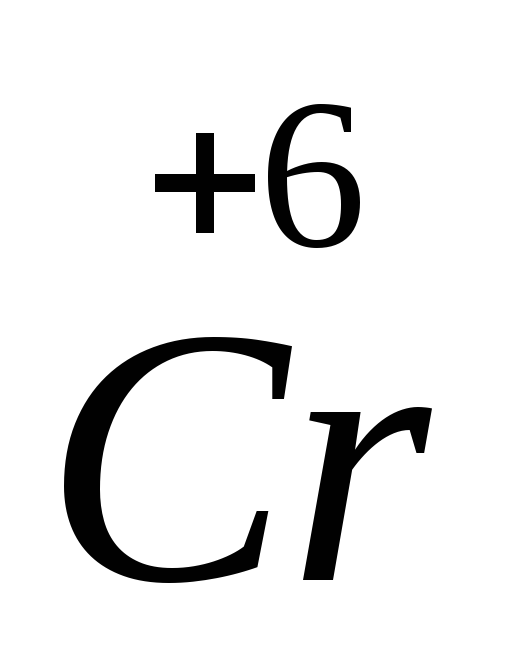
Н

Следующей важной характеристикой атомов является их радиусы. В периодах радиусы атомов металлов с ростом порядкового номера элемента уменьшаются, т.к. с ростом порядкового номера элемента в пределах периода возрастает заряд ядра, а следовательно и уравновешивающий его общий заряд электронов; как следствие, возрастает и кулоновское притяжение электронов, что приводит в конечном счете к уменьшению расстояния между ними и ядром. Наиболее рельефно снижение радиуса наблюдается у элементов малых периодов, у которых происходит заполнение электронами внешнего энергетического уровня.
В больших периодах у d- и f-элементов наблюдается более плавное снижение радиусов при увеличении заряда ядра атома. В пределах каждой подгруппы элементов радиусы атомов, как правило, увеличиваются сверху вниз, так как такое смещение означает переход на более высокий энергетический уровень.
Влияние радиусов ионов элементов на свойства образуемых ими соединений можно проиллюстрировать на примере возрастания кислотности галогенводородных кислот в газовой фазе: HI > HBr > HCl > HF.
В этих соединениях сила кулоновского притяжения зависит от кулоновского радиуса, представляющего собой сумму радиусов ионов галогена и водорода. Очевидно, что с ростом радиуса галогена сила кулоновского притяжения снижается, что делает отщепление протона более выгодным.
Примеры решения типовых задач.
Пример 1. Составление электронных и электронно-графических формул атомов элементов, молекулярных формул соответствующих оксидов и гидроксидов по номеру элемента в периодической системе.
Задача. Постройте электронные и электронно-графические формулы атомов элементов № 35 и № 73 и приведите молекулярные формулы образуемых ими оксидов, гидроксидов и солей.
Решение. Электронные формулы показывают распределение электронов в атоме по энергетическим уровням и подуровням. Электронная формула обозначается символами 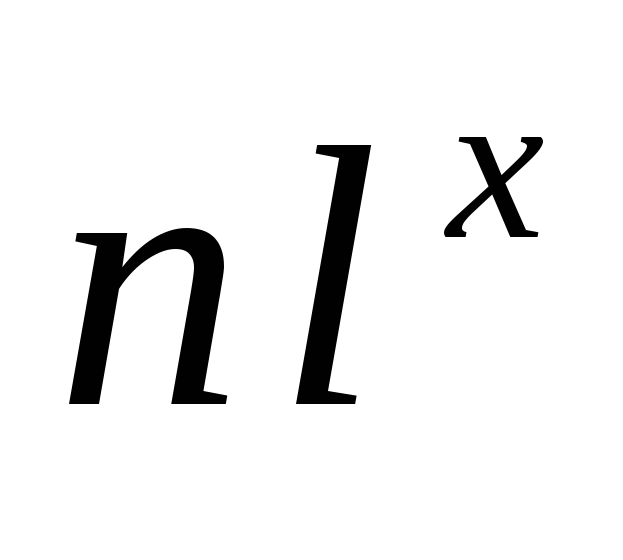
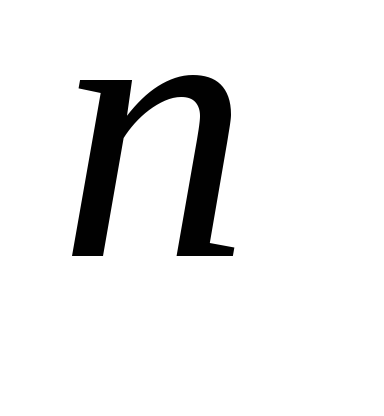
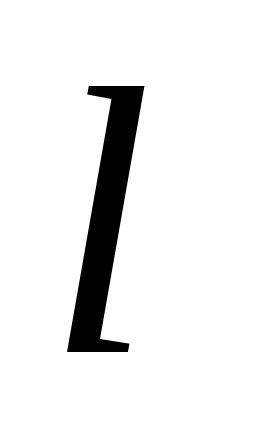
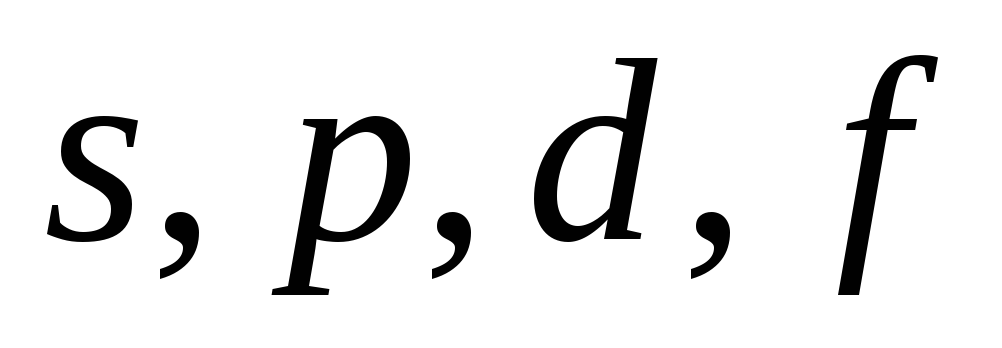

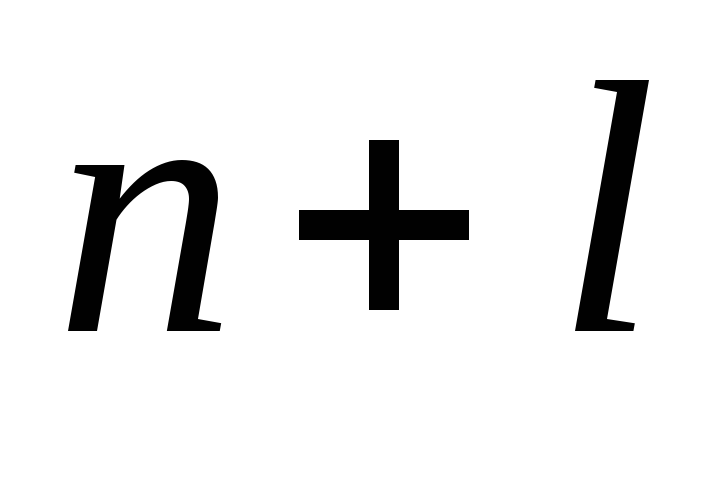
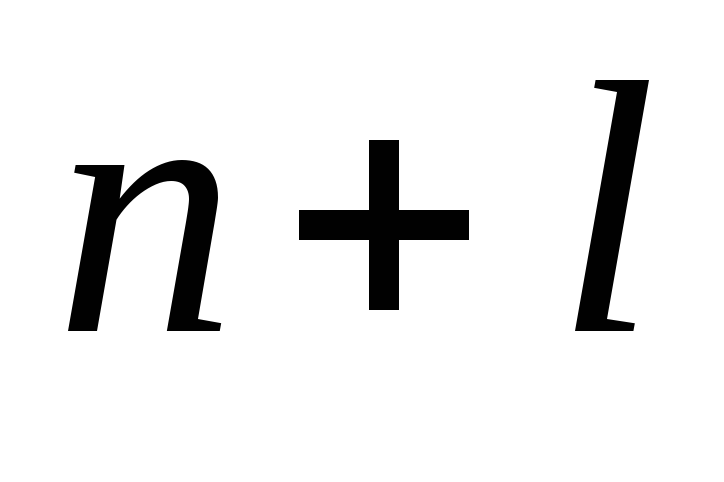
Приложение этих правил к многоэлектронному атому приводит к следующей последовательности заполнения его энергетических уровней и подуровней:
1s2s2p3s3p4s3d4p5s4d5p6s(5d 1 )4f
5d6p7s (6d 3-2 )5f6d7p.
Положение элементов в периодической системе дает для него следующие характеристики: порядковый номер элемента, номер периода, номер группы, подгруппа (главная или побочная). Каждая из этих характеристик однозначно связана со строением атома элемента.
Порядковый номер элемента указывает на число электронов, номер периода показывает на число энергетических уровней. Номер группы для элементов главных подгрупп указывает на число электронов на внешнем энергетическом уровне и на высшую положительную степень окисления. Для элементов побочных подгрупп номер группы указывает только на высшую положительную степень окисления, число же электронов на внешнем энергетическом уровне может быть 1 или 2.
В связи с выше сказанным, электронные формулы для элементов №35 (Br) и №73 (Та) имеют следующий вид:
35Br 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 5
73Ta 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 3 6s 2
Электронная структура атома может быть изображена также графическим образом с помощью энергетических, или квантовых ячеек, которые являются схематическим изображением атомных орбиталей (АО).
аждая такая ячейка обозначается в виде прямоугольника, а электроны в этих ячейках обозначаются стрелками. В каждой квантовой ячейке может быть не более двух электронов с противоположными спинами:
Согласно правилу Хунда орбитали данного подуровня заполняются сначала по одному электрону с одинаковыми спинами, а затем по второму электрону с противоположными спинами.
Графическая схема для указанных элементов имеет следующий вид:
Br находится в VIIA группе, т.к. все валентные электроны у него находятся на внешнем энергетическом уровне. Следовательно, Br – неметалл, оксид брома (VII) Br2O7 проявляет свойства кислотного оксида, соответствующий ему гидроксид – бромная кислота HBrO4, соль пербромат натрия NaBrO4. Так как на внешнем энергетическом уровне 7 электронов, то приобретая один электрон, бром имеет низкую степень окисления –1. Соединения, соответствующие 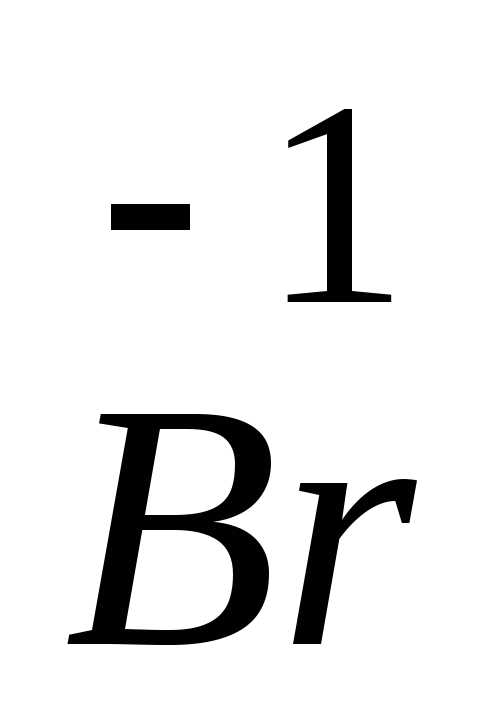
Тантал – d-элемент, поэтому он может проявлять переменную степень окисления и образует несколько оксидов и гидроксидов, причем характер их зависит от степени окисления. Для тантала наиболее типичны соединения, в которых их степень окисления равна +5. Оксид тантала (V) проявляет свойства кислотного оксида, его формула Та2О5, соответствующий ему гидроксид танталовая кислота НТаО3, соль КТаО3. Низшая степень окисления для тантала +2. Оксид и гидроксид Та(II) проявляет основные свойства. Соединения, соответствующие 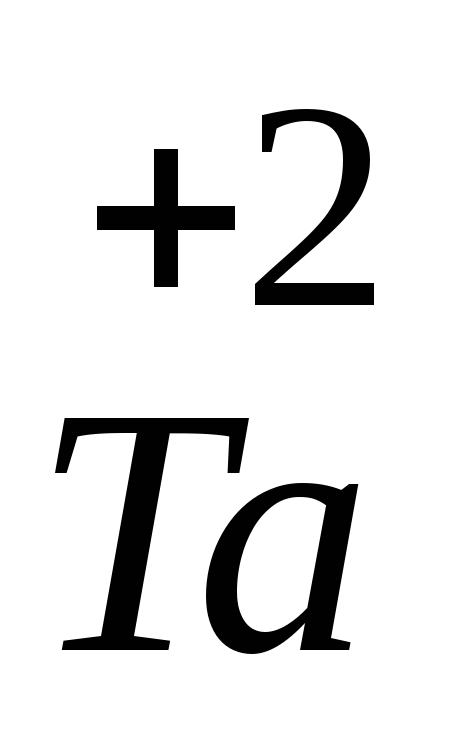
Пример 2. Определение местонахождения элемента в периодической системе химических элементов по его электронной формуле.
Задача. Определите элемент, его местонахождение в периодической системе, если его электронная формула имеет следующий вид: …5s 2 5p 2 .
Решение. Определить элемент и найти его местоположение в периодической системе можно двумя путями.
Первый путь: определить число электронов, а оно укажет на порядковый номер элемента. Электронная формула, соответствующая этому элементу, имеет следующий вид:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 2 ,
т.к. число электронов равно 50, следовательно, это олово. Оно находится в 5 периоде, четвертой группе, главной подгруппе.
Второй путь: этот элемент находится в 5 периоде, т.к. имеет строение внешнего энергетического уровня 5s 2 5р 2 . На внешнем энергетическом уровне находится 4 электрона, следовательно, он находится в IVA группе. Элемент, соответствующий этим координатам – олово.
Пример 3. Составление электронных формул атомов элементов на основе значений квантовых чисел электронов наружного слоя.
Решение. Состояние каждого электрона наружного энергетического уровня определяется следующим набором квантовых чисел:
Главное квантовое число равно четырем, следовательно, электроны находятся на 4-м энергетическом уровне. Орбитальное квантовое число определяет форму орбитали. Если l=1, то орбиталь называется р-орбиталью, следовательно, три электрона находятся на р-подуровне 4-го энергетического уровня. Магнитное квантовое число ml (-1, 0, +1) определяет ориентацию орбитали в пространстве. На всех трех р-орбиталях (px, py, pz) находится по одному электрону (ms=+1/2). Наружный энергетический уровень атома этого элемента содержит пять электронов: …4s 2 4p 3 . Такую электронную конфигурацию наружного энергетического уровня имеет атом мышьяка As, электронная формула которого следующая: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 3 .
Пример 4. Составление электронных формул вещества на основе значения порядкового номера элемента.
Задача. Составьте электронные формулы атома элемента с порядковым номером 40. Приведите распределение электронов атома этого элемента по квантовым (энергетическим) ячейкам.
Решение. Элемент с порядковым номером 40 – цирконий Zr. Соответственно, на электронных уровнях и соответствующих им подуровнях (орбиталях) необходимо разместить 40 электронов.
В соответствии с правилами заполнения многоэлектронного атома начинаем размещение электронов на нем с самого низкого энергетического уровня, n=1. Ему соответствует единственное значение орбитального числа l=0, определяющего сферическую форму орбитали (s-подуровень). Магнитное квантовое число, определяемое значением l (-l, . 0,…+l) также принимает для этого случая единственное значение ml=0, что демонстрирует наличие единственной орбитали (s-орбитали) на этом подуровне. Согласно правилу Паули на одной орбитали (и соответственно, на s-подуровне) может быт размещено максимум два электрона со спиновыми квантовыми числами ms=+1/2 и ms=-1/2. Поскольку рассматриваемый уровень (n=1) и соответствующий ему s-подуровень после размещения на нем двух электронов исчерпан (1s 2 ), переходим к следующему энергетическому уровню n=2. Этому уровню соответствуют два подуровня, характеризующегося значениями l=0 и l=1. Как указывалось выше, значение l=0 определяет s-подуровень, на котором может быть размещено максимум два электрона 2s 2 . Следующий подуровень, определяемый значением l=1, называется р-подуровнем. Ему соответствует гантелеобразная форма орбитали (p-орбиталь). Для l=1 магнитное квантовое число принимает три значения -1, 0 и +1. Эти три значения определяют наличие на р-подуровне трех орбиталей, каждая из которых может принять максимум два электрона. Это означает, что на р-подуровне (l=1) можно разместить максимум шесть электронов (2р 6 ). Итак, на двух первых энергетических уровнях (n=1, n=2) мы расположим 10 электронов: 1s 2 2s 2 2p 6 . Переходим к следующему уровню, n=3. На этом уровне находятся три подуровня, которым соответствуют значения l: 0, 1, 2 (l=0,1…..n-1). 3s-подуровень (l=0) этого уровня как любой s-подуровень содержит максимум 2 электрона (3s 2 ). 3р-подуровень (l=1) – 6 электронов (3р 6 ). При дальнейшем заполнении многоэлектронного атома возникает дилемма: куда размещать следующие электроны — на 3d (l=2) или 4s (l=0) подуровень? Здесь мы руководствуемся первым правилом Клечковского, согласно которому в первую очередь заполняется подуровень, которому соответствует меньшее значение суммы n+l. Для 3d-подуровня эта сумма равна 3+2=5, а для 4s она равна 4+0=4. Поэтому заполняем 4s-подуровень 4s 2 . Далее необходимо решить дилемму, на каком подуровне размещать следующие электроны: 3d или 4р. Обоим этим подуровням соответствует одинаковое значение n+l=5. Здесь мы руководствуемся вторым правилом Клечковского, согласно которому при равенстве суммы n+l в первую очередь заполняется подуровень, которому соответствует меньшее значение n. Поэтому заполняет 3d-подуровень. Любой d-подуровень (l=2) содержит 5 орбиталей, которым соответствует набор значений m: -2, -1, 0, +1, +2. Максимальное число электронов, размещенных на этом подуровне, равно 5·2=10 (3d 10 ). Таким образом, мы пришли к ситуации, когда полностью исчерпаны первые три уровня (n=1, n=2, n=3) и заполнен s-подуровень 4-го уровня: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 . При заполнении использовано 30 электронов, остается еще 10. Следующий подуровень, подлежащий заполнению, — 4р-подуровень (но не 5s – см. второе правило Клечковского). Ему соответствуют 3р-орбитали, на которых размещаем шесть электронов. Затем заполняем 5s-подуровень (два электрона) и приходим к ситуации 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 2 . Остающиеся два электрона размещаем (руководствуясь первым правилом Клечковского) на 4d-подуровне и приходим к электронной формуле атома циркония: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 2 5s 2 . Ей соответствует графическая электронная формула
что общего в строении атомов химических элементов?
Каждый из атомов химических элементов имеет ядро, состоящее из протонов и нейтронов, и электроны, вращающиеся вокруг этого ядра.
Электроны движутся по электронным слоям, количество которых определяется периодом элемента.
Другие вопросы из категории
вид Mg+2HCl=MgCl2+ H2
в чем отличие одноатомных спиртом от многоатомных приведите пример
Читайте также
а)бериллий,бор,литий
б)магний,кальций,бериллий
Расположите перечисленные химические элементы в порядке возрастания неметаллических свойств атомов:
а)селен,кислород,сера
б)хлор,фосфор,сера
Изобразите электронные схемы атомов кремния и фосфора.Укажите,что общего в строении атомов данных химических элементов,атомы какого из элементов проявляют неметаллические свойства в большей степени.
Укажите химический элемент третьего периода,атомы которого имеют наиболее выраженные металлические свойства.
2)Изобразите электронные схемы атомов кремния и фосфора.Укажите,что общего в строении атомов данных химических элементов,атомы какого их элементов проявляют неметаллические свойства в большей степени. 3)Укажите химический элемент третьего периода,атомы которого имеют наиболее выраженные металлические свойства.
группы, подгруппа 4. Строение атома химического элемента: а) заряд ядра; число протонов, число нейтронов б) число электронов в) количество энергетических уровней г) схема строение электронной оболочки атома химического элемента д) электронная формула атома
Благородные газы практически не образуют химических соединений. Что общего в строении атомов этих элементов? Является ли это причиной их химической инертности?
II. Положение химического элемента в периодической системе элементов Д.И. Менделеева:
1) порядковый номер;
2) номер периода;
4) подгруппа (главная или побочная).
III. Строение атома химического элемента:
1) заряд ядра атома;
2) относительная атомная масса химического элемента;
3) число протонов;
4) число электронов;
5) число нейтронов;
6) число электронных уровней в атоме.
IV. Электронная и электронно-графическая формулы атома, его валентные электроны.
V. Тип химического элемента (металл или неметалл, s-, p-, d-или f-элемент).
VI. Формулы высшего оксида и гидроксида химического элемента, характеристика их свойств (основные, кислотные или амфотерные).
VII. Сравнение металлических или неметаллических свойств химического элемента со свойствами элементов-соседей по периоду и подгруппой.
VIII. Максимальный и минимальный степень окисления атома.
ХИМИЯ. что общего с точки зрения строения атомов у элементов главной подгруппы |V группы периодической системы Д. И. Менделеева?
Ответ оставил Гуру
С точки зрения строения у элементов главной подгруппы lV группы периодической системы Д.И.Менделеева то, что у них 4 электрона на внешнем энергетической уровне
Если тебя не устраивает ответ или его нет, то попробуй воспользоваться поиском на сайте и найти похожие ответы по предмету Химия.
Определите число протонов, нейтронов и электронов в атоме азота с массовым числом 15.
Назовите химический элемент, расположенный в 4 периоде. Известно, что в атоме данного элемента на последнем энергетическом уровне находится 3 электрона.
Урок 3. Элементарные сведения о строении атома
- что такое атом;
- из чего состоит атом;
- изменяется ли атом в химических реакциях?
АТОМ — это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Число электронов в ходе химических процессов может изменяться, но заряд ядра всегда остается неизменным. Зная распределение электронов в атоме (строение атома), можно предсказать многие свойства данного химического элемента, а также простых и сложных веществ, в состав которых этот элемент входит.
Структура Периодической системы Менделеева
Строение атома, т. е. состав ядра, распределение электронов вокруг ядра, несложно определить по положению элемента в Периодической системе. В Периодической системе Менделеева химические элементы располагаются в определённой последовательности. Эта последовательность тесно связана со строением атома этих элементов. Каждому химическому элементу в системе присвоен порядковый номер, кроме того, для него можно указать:
- номер периода;
- номер группы;
- вид подгруппы.
Зная точный «адрес» химического элемента, т. е. его группу, подгруппу и номер периода, можно однозначно определить строение его атома.
Период — это горизонтальный ряд химических элементов. В современной Периодической системе семь периодов. Первые три — малые, так как они содержат 2 или 8 элементов:
- 1-й период — Н, Не — 2 элемента;
- 2-й период — Li…Nе — 8 элементов;
- 3-й период — Na…Аr — 8 элементов.
Остальные периоды — большие. Каждый из них содержит 2–3 ряда элементов:
- 4-й период (2 ряда) — К…Кr — 18 элементов;
- 6-й период (3 ряда) — Сs…Rn — 32 элемента. В этот период входит ряд лантаноидов.
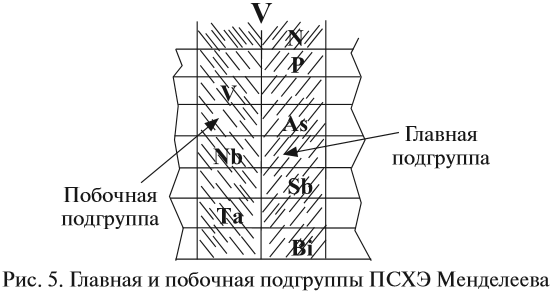
Группа — вертикальный ряд химических элементов. Всего групп восемь. Каждая группа состоит из двух подгрупп: главной подгруппы и побочной подгруппы (см. рис. 5).
Главную подгруппу (подгруппу А) образуют химические элементы малых периодов и больших периодов. На рисунке 5 показано, что главную подгруппу пятой группы составляют элементы малых периодов (N, P) и больших периодов (As, Sb, Bi).
Побочную подгруппу (подгруппу Б) образуют химические элементы только больших периодов. В нашем случае это V, Nb, Ta.
Визуально эти подгруппы различить легко: главная подгруппа «высокая», начинается с первого или второго периода. Побочная подгруппа — «низкая», начинается с 4-го периода.
Итак, каждый химический элемент Периодической системы имеет свой адрес:
Например, ванадий (V) — это химический элемент 4-го периода, V группы, побочной подгруппы, порядковый номер 23.
Задание 3.1. Укажите период, группу и подгруппу для химических элементов с порядковыми номерами 8, 26, 31, 35, 54.
Задание 3.2. Укажите порядковый номер и название химического элемента, если известно, что он находится:
- в 4-м периоде, VI группе, побочной подгруппе;
- в 5-м периоде, IV группе, главной подгруппе.
Каким образом можно связать эти сведения об элементе со строением его атома?
Ядро атома. Изотопы
Атом состоит из ядра, которое имеет положительный заряд, и электронов, которые имеют отрицательный заряд. В целом атом электронейтрален.
Положительный заряд ядра атома равен порядковому номеру химического элемента.
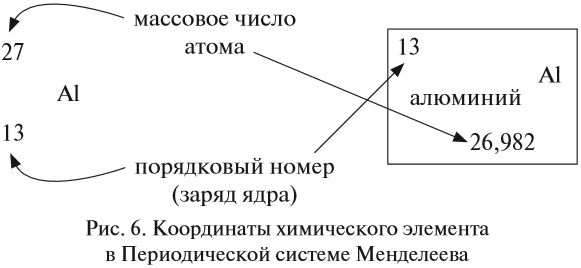
Ядро атома — сложная частица. В ней сосредоточена почти вся масса атома. Поскольку химический элемент — совокупность атомов с одинаковым зарядом ядра, то около символа элемента указывают (рис. 6).
По этим данным можно определить состав ядра. Ядро состоит из протонов и нейтронов.
- Протон (р) имеет массу, равную 1 (1,0073 а. е. м.) и заряд, равный +1.
- Нейтрон (n) заряда не имеет (нейтрален), а масса его приблизительно равна массе протона (1,0087 а. е. м.).
Какие частицы определяют заряд ядра? Протоны! Причём число протонов равно (по величине) заряду ядра атома, т. е. порядковому номеру:
Число нейтронов определяют по разности между величинами: «масса ядра» и «порядковый номер».
Задание 3.3. Определите состав ядер атомов, если химический элемент находится в:
- 3-м периоде, VII группе, главной подгруппе;
- 4-м периоде, IV группе, побочной подгруппе;
- 5-м периоде, I группе, главной подгруппе.
Обратите внимание, что при определении массового числа ядра атома приходится округлять атомную массу, указанную в Периодической системе! Почему? Ведь массы протона и нейтрона практически целочисленны, а массой электронов можно пренебречь.
Для того,чтобы ответить на этот вопрос, нужно понять:
- Что происходит с атомом в ходе химических процессов;
- Что такое «химический элемент».
В химических процессах обязательно изменяется распределение электронов вокруг ядра или даже изменяется их число. В последнем случае атом отдаёт или принимает электроны и превращается в заряженную частицу — ион. Но в химических реакциях никогда не меняется состав ядра атома, его заряд. Поэтому заряд ядра атома является своеобразным «паспортом» химического элемента.
Химический элемент — совокупность атомов или ионов с одинаковым зарядом ядра.
Для того чтобы разобраться, попробуйте определить, какие из ядер, состав которых указан ниже, принадлежат одному и тому же химическому элементу:
Атомам одного химического элемента принадлежат ядра А и В, так как они содержат одинаковое число протонов, т. е. заряд этих ядер одинаковый. Но ведь у них разная масса! Исследования показывают, что масса атома не оказывает существенного влияния на его химические свойства. Поэтому атомы одного и того же химического элемента (одинаковое число протонов), но с разной массой (разное число нейтронов) являются ИЗОТОПАМИ* этого элемента.
* Слово «изотоп» означает по смыслу «одно место», т. е. все изотопы данного химического элемента находятся в одной клетке ПСХЭ.
В таблице Менделеева указана средняя атомная масса всех природных изотопов данного элемента (Аr). Изотопы и их химические соединения отличаются друг от друга по физическим свойствам, но химические свойства у изотопов одного химического элемента одинаковы. Так, изотоп углерода-14 ( 14 С) имеет такие же химические свойства, как и углерод-12 ( 12 С), который входит в ткани любого живого организма, отличаясь от него только радиоактивностью. Поэтому изотопы применяют для диагностики и лечения различных заболеваний, для научных исследований.
Элемент «водород» встречается в природе в виде трёх изотопов:
Химический элемент «кислород» также представлен тремя природными изотопами:
Задание 3.4. Укажите состав ядер этих изотопов водорода и кислорода.
Если разные вещества содержат атомы одного и того же химического элемента, это не означает, что эти вещества имеют одни те же свойства. Например, химический элемент «хлор» в виде атомарного хлора Cl • разрушает метан, а также атмосферный озон. Тот же элемент в виде молекулярного хлора Cl2 ядовит, активно реагирует с водой, многими металлами, а ионы хлора (химический элемент — тот же!) в составе NaCl химически инертен, а с биологической точки зрения не только безвреден, но и полезен для нас. Эти ионы являются макроэлементами нашей пищи, которые входят в состав крови, желудочного сока. Суточная потребность — до 6 граммов.
Но вернемся к описанию строения атома.
Распределение электронов в поле ядра атома
Как известно, ядро атома в химических процессах не меняется. А что меняется? Общее число электронов и распределение электронов. Общее число электронов определить несложно: оно равно порядковому номеру, т. е. заряду ядра атома:
Электроны имеют отрицательный заряд –1, а масса их ничтожна: 1/1840 от массы протона.
Отрицательно заряженные электроны отталкиваются и поэтому находятся на разных расстояниях от ядра. При этом электроны, имеющие приблизительно равный запас энергии, образуют энергетический уровень.
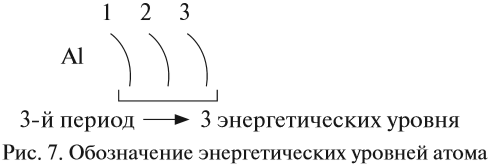
Число энергетических уровней в атоме равно номеру периода, в котором находится химический элемент. Энергетические уровни условно обозначают так (рис. 7).
Задание 3.5. Определите число энергетических уровней в атомах кислорода, магния, кальция, свинца.
На каждом энергетическом уровне может находиться ограниченное число электронов:
- на первом энергетическом уровне не более 2 электронов;
- на втором энергетическом уровне не более 8 электронов;
- на третьем энергетическом уровне не более 18 электронов.
ЗАПОМНИТЕ ЭТИ ЧИСЛА!
Они показывают, что, например, на втором энергетическом уровне может находиться 2 или 5 или 7 электронов, но не может быть 9 или 12 электронов.
Важно знать, что, независимо от номера энергетического уровня, на внешнем (последнем) уровне не может быть больше восьми электронов. Внешний восьмиэлектронный энергетический уровень является наиболее устойчивым и называется завершённым. Такие энергетические уровни имеются у самых неактивных элементов — благородных газов.
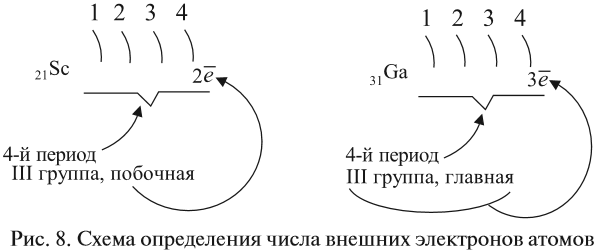
Как определить число электронов на внешнем уровне остальных атомов? Для этого существует простое правило – число внешних электронов равно:
- для элементов главных подгрупп — номеру группы;
- для элементов побочных подгрупп — оно не может быть больше двух (рис. 8).
Задание 3.6. Укажите число внешних электронов для химических элементов с порядковыми номерами 15, 25, 30, 53.
Задание 3.7. Найдите в Периодической системе химические элементы, в атомах которых имеется завершённый внешний уровень.
Очень важно правильно определять число внешних электронов, так как именно с ними связаны важнейшие свойства атома. Так, в химических реакциях атомы стремятся «приобрести» устойчивый, завершённый внешний уровень (8ē). Для этого атомы, на внешнем уровне которых мало электронов, «предпочитают» их отдать.
Химические элементы, атомы которых способны только отдавать электроны, относятся к МЕТАЛЛАМ. Очевидно, что на внешнем уровне атома металла должно быть мало электронов: 1, 2, 3.
Если на внешнем энергетическом уровне атома много электронов, то такие атомы стремятся принять электроны до завершения внешнего энергетического уровня, т. е. до восьми электронов. Такие элементы относятся к НЕМЕТАЛЛАМ.
Вопрос. К каким элементам (металлам или неметаллам) относятся химические элементы побочных подгрупп? Почему?
Металлы и неметаллы главных подгрупп в таблице Менделеева отделяет линия, которую можно провести от бора к астату. Выше этой линии (и на линии) располагаются неметаллы, ниже — металлы.
Задание 3.8. Определить, к металлам или неметаллам относятся: фосфор, ванадий, кобальт, селен, висмут. Вывод сделайте, определив положение элемента в Периодической системе химических элементов и число электронов на внешнем уровне.
Для того чтобы составить распределение электрона по остальным уровням и подуровням, следует воспользоваться следующим АЛГОРИТМОМ:
- Определить общее число электронов в атоме (по порядковому номеру).
- Определить число энергетических уровней (по номеру периода).
- Определить число внешних электронов (по виду подгруппы и номеру группы).
- Указать число электронов на всех уровнях, кроме предпоследнего.
- Рассчитать число электронов на предпоследнем уровне.
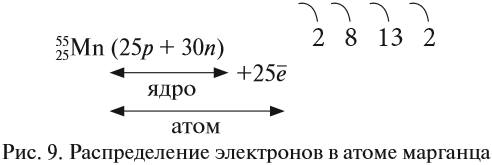
Например, согласно пунктам 1…4 для атома марганца определено:
Получили распределение электронов в атоме марганца (рис. 9):
Задание 3.9. Отработайте алгоритм, составив схемы строения атомов для элементов № 16, 26, 33, 37. Укажите: металлы это или неметаллы? Ответ поясните.
Составляя вышеприведенные схемы строения атома, мы не учитывали, что электроны в атоме занимают не только определённые уровни, но и определённые подуровни каждого уровня. Вид подуровня обозначается латинской буквой: s, p, d.
Число возможных подуровней равно номеру уровня, т. е.
- первый уровень состоит из одногоs-подуровня;
- второй уровень состоит из двух подуровней: s и р и т. д.
На каждом подуровне может находиться строго ограниченное число электронов:
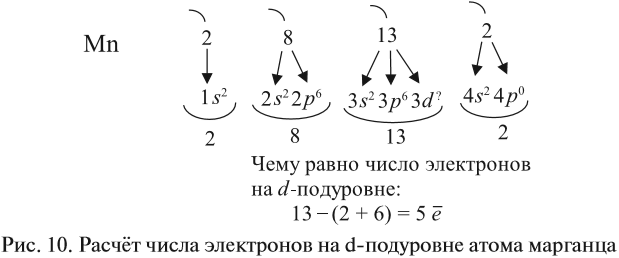
Подуровни одного уровня заполняются в строго определённом порядке:
Таким образом, р-подуровнь не может начать заполняться, если не заполнен s-подуровень данного энергетического уровня и т. д. Исходя из этого правила, несложно составить электронную конфигурацию атома марганца (рис. 10).
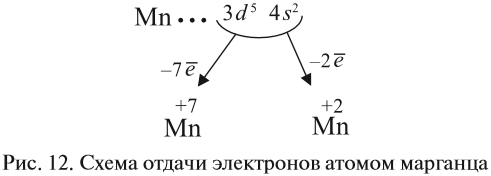
В целом электронная конфигурация атома марганца выглядит так:
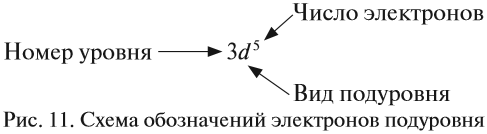
Здесь и далее приняты обозначения (рис. 11).
Задание 3.10. Составьте электронные конфигурации атомов для химических элементов № 16, 26, 33, 37.
Для чего необходимо составлять электронные конфигурации атомов? Для того чтобы определять свойства этих химических элементов!
Для этого следует помнить: в химических процессах участвуют только валентные электроны.
Валентные электроны находятся на внешнем энергетическом уровне и незавершённом d-подуровне предвнешнего уровня.
Определим число валентных электронов для марганца:
Строение атома и свойства элементов
Мы получили краткую электронную формулу атома марганца, которая отражает распределение его валентных электронов. Что можно определить по этой формуле?
1. Какие свойства — металла или неметалла — преобладают у этого элемента? Ответ: марганец — металл, так как на внешнем (четвёртом) уровне 2 электрона.
2. Какой процесс характерен для металла? Ответ: всегда только отдача электронов.
3. Какие электроны и сколько их будет отдавать атом марганца? Ответы:
- два внешних электрона (они дальше всех от ядра и слабее притягиваются им);
- семь (2+5) валентных электронов (так как в этом случае на третьем уровне атома останется восемь электронов, т. е. образуется завершённый уже внешний уровень).
Все эти рассуждения и заключения можно отразить при помощи схемы (рис. 12).
Полученные условные заряды атома называются степенью окисления.
Рассматривая строение атомов кислорода и водорода и рассуждая аналогично, можно показать, что типичными степенями окисления для кислорода является –2, а для водорода +1.
Вопрос. С каким из этих химических элементов может образовывать соединения марганец, если учесть полученные выше степени окисления его?
Только с кислородом, так как его атом имеет противоположную по заряду (знаку) степень окисления. В этом случае несложно составить формулы соответствующих оксидов марганца (здесь степени окисления соответствуют валентностям этих химических элементов):
Строение атома марганца подсказывает, что большей степени окисления, чем +7, у марганца быть не может, так как в этом случае пришлось бы затрагивать устойчивый, теперь уже завершённый предвнешний уровень. Поэтому степень окисления +7 является высшей, а соответствующий оксид Мn2О7 — высшим оксидом марганца.
Для закрепления всех этих понятий рассмотрим строение атома теллура и некоторые его свойства (см. рис. 13). Этот рисунок показывает, что теллур относится к неметаллам, так как, во-первых, у него на внешнем уровне шесть электронов и, во-вторых, его символ находится в главной подгруппе выше линии В — At. Поэтому его атом может и принимать (до завершения внешнего уровня, и отдавать электроны. В результате, в отличие от металлов, неметалл теллур может проявлять низшую степень окисления (–2) и образовывать летучие водородные соединения с водородом (Н2Те). Высшая степень окисления атома теллура (+6), как и у металлов соответствует номеру группы и, находясь в этой степени окисления, теллур образует высший оксид ТеО3.
Задание 3.11. Изобразить электронные конфигурации атомов Nа, Rb, Сl, I, Si, Sn. Определить свойства этих химических элементов, формулы их простейших соединений (с кислородом и с водородом).
- В химических реакциях участвуют только валентные электроны, которые могут находиться только на последних двух уровнях.
- Атомы металлов могут только отдавать эти электроны (все или несколько), принимая положительные степени окисления.
- Атомы неметаллов могут принимать (недостающие до восьми) электроны, получая при этом отрицательные степени окисления, и отдавать валентные электроны (все или несколько), принимая при этом положительные степени окисления.
Возникает вопрос: как составить краткую электронную формулу (распределение валентных электронов), сразу, не составляя длинных электронных конфигураций? Для этого нужно помнить несколько простых правил.
1. Номер периода соответствует числу энергетических уровней у атомов химических элементов этого периода.
2. Номер группы, как правило, совпадает с числом валентных электронов, (исключение составляют только подгруппы меди и железа).
3. Подгруппа (главная или побочная) включает химические элементы, у которых имеется одинаковое распределение валентных электронов, причём в атомах элементов главной и побочной подгруппы электроны распределяются по-разному.
3.1. У элементов главных подгрупп все валентные электроны находятся на внешнем уровне, например:
V группа, главная → 5 валентных электронов
Поэтому для всех химических элементов главной подгруппы пятой группы (пять валентных электронов) распределение этих электронов следующее:
3.2. У элементов побочных подгрупп число внешних электронов не превышает двух, например:
5 валентных электронов ← V группа, побочная → 2 электрона на внешнем уровне*.
* За счёт «провала электрона» число внешних электронов может быть меньше. Но число валентных электронов при этом не меняется, поэтому свойства элемента будут такими же. Эти случаи рассмотрены в Самоучителе второго уровня, часть 1.
Для большинства химических элементов побочных подгрупп, у которых на внешнем энергетическом уровне два электрона, остальные (N – 2) валентные электроны будут находиться на d-подуровне предвнешнего уровня (N – номер группы), например:
Вопрос. Для элементов какой группы составлена такая запись?
Задание 3.12. Составьте краткие электронные формулы для атомов химических элементов № 35 и 42, а затем составьте распределение электронов в этих атомах по алгоритму. Убедитесь, что ваше «предсказание» сбылось.
Сравним теперь свойства химических элементов одной подгруппы, например:
Что общего в строении атомов этих элементов? На внешнем уровне каждого атома по одному электрону — это активные металлы. Металлическая активность связана со способностью отдавать электроны: чем легче отдает электроны атом, тем сильнее выражены его металлические свойства.
Что удерживает электроны в атоме? Притяжение их к ядру. Чем ближе электроны к ядру, тем сильнее они притягиваются ядром атома, тем труднее их «оторвать».
Исходя из этого, сделаем вывод: какой элемент — Nа или Rb — легче отдает внешний электрон? Какой из них является более активным металлом? Очевидно, рубидий, так как его валентные электроны находятся дальше от ядра (и слабее удерживаются ядром).
Вывод. В главных подгруппах сверху вниз металлические свойства усиливаются, так как возрастает радиус атома и валентные электроны слабее притягиваются к ядру.
Оба химических элемента — неметаллы, так как до завершения внешнего уровня не хватает одного электрона, и эти атомы будут активно притягивать недостающий электрон. При этом, чем сильнее притягивает атом неметалла недостающий электрон, тем сильнее проявляются его неметаллические свойства (способность принимать электроны).
За счёт чего происходит притяжение электрона? За счёт положительного заряда ядра атома. Но в таком случае чем ближе электрон к ядру, тем сильнее их взаимное притяжение, тем активнее неметалл.
Сделаем вывод, у какого элемента сильнее выражены неметаллические свойства: у хлора или у йода? Очевидно, у хлора, так как его валентные электроны ближе к ядру.
Вывод. Активность неметаллов в подгруппах сверху вниз убывает, так как возрастает радиус атома и все труднее притянуть недостающие электроны.
Сравним свойства кремния и олова:
На внешнем уровне обоих атомов по четыре электрона. Тем не менее эти элементы в Периодической системе находятся по разные стороны от линии, соединяющей бор и астат (см. правило в уроке 2.1.). Поэтому:
- у кремния, символ которого находится выше линии В–At, сильнее проявляются неметаллические свойства;
- у олова, символ которого находится ниже линии В–At, сильнее проявляются металлические свойства;
Почему? Потому что в атоме олова четыре валентных электрона находятся так далеко от ядра, что присоединение недостающих четырех электронов затруднено, в то время как отдача электронов с пятого энергетического уровня происходит достаточно легко. Для кремния возможны оба процесса, причём первый (приём электронов) — преобладает.
- чем меньше электронов в атоме и чем дальше они от ядра, тем сильнее проявляются металлические свойства;
- чем больше внешних электронов в атоме, чем ближе они к ядру, тем сильнее проявляются неметаллические свойства.
Сравним строение атомов и свойства химических элементов одного периода:
Вопрос. О каком периоде и каких элементах идёт речь?
Видно, что металлические свойства убывают, так как увеличивается число внешних электронов, а неметаллические свойства — возрастают. Если речь идёт о большом периоде, где большинство элементов имеет 2 электрона на внешнем уровне (элементы побочных подгрупп), то в этом случае главной причиной убывания металлических свойств в периоде является уменьшение радиуса атома. Дело в том, что за счёт увеличения заряда ядра в периоде увеличивается сила притяжения электронов к нему и уменьшается радиус атома:
Сравните: r (Ca) = 0,197 нм и r (Zn) = 0,139 нм
Вопрос. Какой из металлов более активен?
Основываясь на этих и других выводах, сформулированных в этой главе, можно для любого химического элемента Периодической системы составить алгоритм описания свойств химического элемента по его положению в Периодической системе.
1. Составить схему строения атома, т. е. определить состав ядра, распределение электронов по энергетическим уровням и подуровням:
- определить общее число электронов в атоме (по порядковому номеру);
- определить число энергетических уровней (по номеру периода);
- определить число внешних электронов (по виду подгруппы и номеру группы);
- указать число электронов на всех энергетических уровнях, кроме предпоследнего;
- рассчитать число электронов на предпоследнем уровне.
2. Определить число валентных электронов и число внешних электронов.
3. Определить, какие свойства — металла или неметалла — сильнее проявляются у данного химического элемента (по положению в ПСХЭ).
4. Определить число отдаваемых (принимаемых) электронов.
5. Определить высшую и низшую степени окисления химического элемента.
6. Составить для этих степеней окисления химические формулы простейших соединений с кислородом и водородом.
7. Определить характер оксида (см. урок 2.1.) и составить уравнения его реакции с водой.
8. Для указанных (пункт 6) веществ составить уравнения характерных реакций (см. урок 2).
Задание 3.13. Составить по данной схеме описания атомов серы, селена, кальция и стронция и свойства этих химических элементов. Какие общие свойства имеют их оксиды? Гидроксиды?
Если вы выполнили упражнения 3.11 и 3.12, то легко заметить, что не только атомы элементов одной подгруппы, но и их соединения имеют общие свойства и похожий состав. Это отражено в Периодическом законе Менделеева: Свойства химических элементов, а также свойства простых и сложных веществ, образованных ими, находятся в периодической зависимости от ЗАРЯДА ЯДЕР ИХ АТОМОВ.
Физический смысл Периодического закона ясен: свойства химических элементов периодически повторяются потому, что периодически повторяются конфигурации валентных электронов (распределение электронов внешнего и предпоследнего уровней).
Так, у химических элементов одной и той же подгруппы одинаковое распределение валентных электронов и, значит, похожие свойства.
Строение атома связано с положением элемента в Периодической системе. Зная строение атома, можно предсказать свойства элемента и его соединений. Эти свойства находятся в периодической зависимости от заряда ядер атомов элементов, в соответствии с Периодическим законом Менделеева.
- http://znaesh-kak.com/x/x/%D1%81%D0%B2%D0%BE%D0%B9%D1%81%D1%82%D0%B2%D0%B0-%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D0%BE%D0%B2-%D1%81%D1%82%D1%80%D0%BE%D0%B5%D0%BD%D0%B8%D1%8F-%D0%B0%D1%82%D0%BE%D0%BC%D0%BE%D0%B2
- http://studfiles.net/preview/600151/page:4/
- http://himia.neznaka.ru/answer/3388772_cto-obsego-v-stroenii-atomov-himiceskih-elementov/
- http://zadachki.net/himiya/page5056988.html
- http://himi4ka.ru/samouchitel-po-himii/urok-3-jelementarnye-svedenija-o-stroenii-atoma.html